【题目】某同学用下图装置制取氧气(浓硫酸有吸水性且不与氧气反应),请回答:

(1)实验室制取气体的发生装置和收集装置类型的确定应根据________ (填序号)
A、药品的状态 B、生成气体的密度和在水中的溶解性
C、反应的条件 D、药品的价格
(2)检查装置②气密性的方法是________________;
(3)用高锰酸钾制取氧气的反应表达式是_______,所选用的发生和收集装置是_________(填序号)。
(4)用双氧水和二氧化锰制取氧气的反应表达式是___________________,发生和收集干燥氧气的装置及顺序应是______________(填序号);实验时若要控制液体滴下的速度,你的改进措施是____;检验氧气是否收满的方法是_________________。
(5)装置②试管口要略向下倾斜的原因是____________________ ;
(6)若用装置④收集的氧气不纯,其原因可能是:________________ 。
(7)你认为实验室选用上述仪器还可用来制取的气体有____________ (写一种)。
参考答案:
【答案】 ABC 把导管的一端放入水中,双手紧握试管的外壁,看导管口是否有气泡冒出 高锰酸钾![]() 锰酸钾+二氧化锰+氧气 ②④或②⑤或②③⑤ 过氧化氢
锰酸钾+二氧化锰+氧气 ②④或②⑤或②③⑤ 过氧化氢![]() 水+氧气 ①③⑤ 把长颈漏斗换成分液漏斗或注射器 把带火星的木条放在瓶口 防止冷凝的水回流使试管破裂 开始时集气瓶未装满水或开始冒气泡就收集了 H2或CO2
水+氧气 ①③⑤ 把长颈漏斗换成分液漏斗或注射器 把带火星的木条放在瓶口 防止冷凝的水回流使试管破裂 开始时集气瓶未装满水或开始冒气泡就收集了 H2或CO2
【解析】(1) 实验室制取气体的发生装置决定于药品的状态和反应条件,收集装置决定于生成气体的密度和在水中的溶解性;(2) 检查装置②气密性的方法是:把导管的一端放入水中,双手紧握试管的外壁,看导管口是否有气泡冒出;(3) 高锰酸钾分解生成锰酸钾、二氧化锰、氧气,反应表达式是:高锰酸钾![]() 锰酸钾+二氧化锰+氧气;因高锰酸钾制取氧气需要固体加热装置,则选装置②,因氧气的密度比空气的大且氧气不易溶于水,则可选④或⑤或③⑤来收集氧气;(4) 过氧化氢和二氧化锰混合时生成水和氧气,反应表达式是:过氧化氢
锰酸钾+二氧化锰+氧气;因高锰酸钾制取氧气需要固体加热装置,则选装置②,因氧气的密度比空气的大且氧气不易溶于水,则可选④或⑤或③⑤来收集氧气;(4) 过氧化氢和二氧化锰混合时生成水和氧气,反应表达式是:过氧化氢![]() 水+氧气;此反应不需加热,发生和收集干燥氧气的装置及顺序应是:①③⑤;实验时若要控制液体滴下的速度,可以把长颈漏斗换成分液漏斗或注射器;检验氧气是否收满的方法是:把带火星的木条放在瓶口;(5)因药品可能受潮,在加热时水分在试管口冷凝,若试管口未向下,则可能水倒流使热得试管骤冷而炸裂;(6) 若用排水法收集的氧气不纯,则有可能开始时集气瓶未装满水,有一部分空气存在导致不纯,也可能使装置中的空气未排干净,开始冒气泡就收集了导致氧气不纯;(7) 实验室选用上述仪器还可用来制取的气体有氢气或二氧化碳。
水+氧气;此反应不需加热,发生和收集干燥氧气的装置及顺序应是:①③⑤;实验时若要控制液体滴下的速度,可以把长颈漏斗换成分液漏斗或注射器;检验氧气是否收满的方法是:把带火星的木条放在瓶口;(5)因药品可能受潮,在加热时水分在试管口冷凝,若试管口未向下,则可能水倒流使热得试管骤冷而炸裂;(6) 若用排水法收集的氧气不纯,则有可能开始时集气瓶未装满水,有一部分空气存在导致不纯,也可能使装置中的空气未排干净,开始冒气泡就收集了导致氧气不纯;(7) 实验室选用上述仪器还可用来制取的气体有氢气或二氧化碳。
-
科目: 来源: 题型:
查看答案和解析>>【题目】用下图所示的装置进行电解水实验,有以下描述:
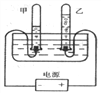
①向水中加入少量硫酸或氢氧化钠,能增强水的导电性,使水电解产生气体的速度变大
②甲、乙两试管内收集到的气体的体积比约为2:1
③甲试管内产生的气体能燃烧
④乙试管内产生的气体能使带火星的木条复燃。 以上描述中正确的是
A. ③ B. ①②③④ C. ①② D. ①②③
-
科目: 来源: 题型:
查看答案和解析>>【题目】小明用如图装置来测定空气中氧气的含量,对该实验认识正确的是
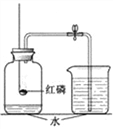
A. 使用红磷的量多或少,都不会影响实验结果
B. 燃烧足够的红磷可使进入集气瓶中的水约占容器体积的1/5
C. 若用硫粉或碳粉代替燃烧匙内的红磷,测定结果不准确
D. 红磷一燃烧完,就要立即观察,并记录水进入容器的刻度
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是元素周期表中的一部分。已知在元素周期表中,同一周期(横行)中的元素,除0族(最右纵行)元素外,从左到右原子序数依次增多,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强。请回答:
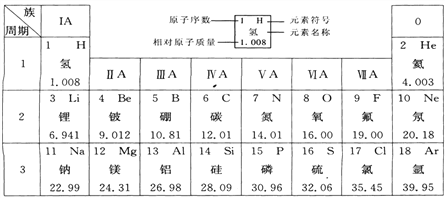
(1)从表中查出铝的相对原子质量为__________;原子序数为9的元素位于元素周期表的第_____周期,元素符号为_____,氟原子核内中子数为_______,它属于______(填“金属”或“非金属”)元素。
(2)表中不同种元素最本质的区别是_________(填序号)。
A、电子数不同 B、相对原子质量不同
C、中子数不同 D、质子数不同
(3)原子半径:钠________镁(填“>”或“==”或“<”,下同),原子得电子能力:硫________氯。
-
科目: 来源: 题型:
查看答案和解析>>【题目】环境问题是人类可持续发展必须解决的一个重要问题,温室效应被列为21世纪人类面临的最大威胁之一,已引起人们的广泛关注。旨在限制发达国家温室气体排放量、抑制全球范围内气候持续变暖的《京都议定书》,已于2005年2月16日正式生效。
(1)二氧化碳是大气中的主要温室气体,我国二氧化碳的排放量位居世界第二,为减缓温室效应,我们可以采取的措施有(只填2种):________________;_____________。
(2)为减缓二氧化碳使全球变暖的趋势,有科学家提出大胆设想:将排放到空气中的二氧化碳压缩使其液化,然后将其压入到冰冷的深海中。但也有科学家担心海水中富含二氧化碳后酸度会增加,可能会杀死一些海洋生物,甚至会溶解掉部分海床,同时气候变化也可能改变海洋环流,把海底的二氧化碳又带回海面,另外把二氧化碳压入海底所消耗的能源可能会再增加二氧化碳的排放。已知温度越高、压强越小,气体在水中溶解得越少。
A、 二氧化碳气体转变为液体时将会__________能量(填“释放”或“消耗”);
B、二氧化碳使海水酸度增加的原理的反应表达式为_________ ;
C、二氧化碳在深海中比在通常状况下的水中的溶解得(填“多”或“少”)_______,原因是_____________。
(3)二氧化碳在化学家的眼里是可以利用的重要资源,只要有合适的条件,可以像发生光合作用那样将二氧化碳转变为所需要的产物。二氧化碳可以为化工合成提供足够的碳元素,既可以减少化工产业对煤和石油的消耗,又可以缓解大气中二氧化碳含量的增加。
A、二氧化碳和水通过光合作用转变为葡萄糖和氧气的反应表达式为:_______________。
B、我国科学家陈乾旺等最新研究成果表明,在一定条件下,二氧化碳和金属钠反应产生金刚石和碳酸钠,请从人类生存的角度分析,金刚石与水相比谁更宝贵______,理由是_________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲和乙可以制备化工原料丙,微观过程如下图。下列说法错误的是( )

A. 丁的化学式为O2
B. 丙中C、H的质量比为12:1
C. 该反应体现无机物可转化为有机物
D. 若改变反应条件,甲和乙反应可生成一种重要的糖类物质
-
科目: 来源: 题型:
查看答案和解析>>【题目】在NaOH和Na2CO3的混合物9.3g中加入一定量的10.0%的稀盐酸,恰好完全反应, 将生成的气体全部通入足量的澄清石灰水中,产生5.0g沉淀。下列说法正确的是( )
A. 题中的一定量是7.3g
B. 反应共产生11.7gNaCl
C. 如用10%的稀盐酸将5.0g沉淀溶解,则所用稀盐酸的量与题中的一定量相等
D. Na2CO3消耗的稀盐酸比NaOH消耗的稀盐酸多
相关试题

