【题目】氯化钠是一种重要的化工原料。电解氯化钠溶液可制得氯气、氢氧化钠和氢气,反应的化学方程式为2NaCl+2H2O![]() Cl2↑+H2↑+2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠完全反应时,得到85.4g溶液,生成氢气的质量与时间的关系如图所示。请计算:
Cl2↑+H2↑+2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠完全反应时,得到85.4g溶液,生成氢气的质量与时间的关系如图所示。请计算:
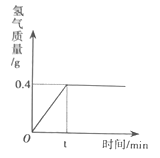
(1)氯化钠完全反应时生成氢气的质量是_________g。
(2)氯化钠完全反应时,生成氢氧化钠的质量是_________克?
(3)原氯化钠溶液中溶质的质量分数是_________?
参考答案:
【答案】 0.4 16 23.4%
【解析】根据反应的化学方程式及其提供的数据计算解答。(1)由图可知:氯化钠完全反应时,生成氢气的质量是0.4g;(2)设生成氢氧化钠的质量是x,生成氯气的质量为y,氯化钠的质量为z。
2NaCl+2H2O![]() Cl2↑+H2↑+2NaOH
Cl2↑+H2↑+2NaOH
117 71 2 80
z y 0.4g x
![]()
x=16g
y=14.2g
z=23.4g
(3)原氯化钠溶液中溶质的质量分数为![]() ×100% =23.4%
×100% =23.4%
答:(2)氯化钠完全反应时,生成氢氧化钠的质量是16克;(3)原氯化钠溶液中溶质的质量分数是23.4%。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是a、b、c三种固体物质的溶解度曲线图,请回答问题:
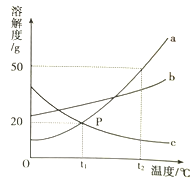
(1)t2℃时,a、b、c三种物质中,溶解度由大到小的顺序是_____________。
(2)将c物质的不饱和溶液转变成饱和溶液可采取的方法有_____________。(写出一种即可)。
(3) t2℃时,将30ga物质加入50g水中充分溶解后,所得溶液的质量是_____g.
(4)图中P点所表示的意义是______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知奥运五环中A、B、C、D、E为稀硫酸、氢氧化钠溶液、二氧化碳、氧化铁、水中的一种,且相连环内的两种物质能发生化学反应,E是常见的溶剂。请回答:
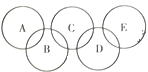
(1)B物质是__________。
(2)A与B反应的实验现象是______________。
(3)写出C与D反应的化学方程式________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后瓶中残留废液进行探究。
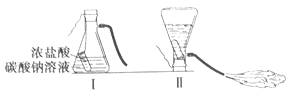
(提出问题)废液中所含溶质是什么?
(猜想与假设)
猜想1:废液中的溶质是NaCl、Na2CO3和HCl
猜想2:废液中的溶质只有NaCl
猜想3:废液中的溶质是NaCl、HCl
猜想4:废液中的溶质是______。
(讨论与交流)
小明认为猜想I无需验证就知道是错误的,他的理由是_____(请用化学方程式说明)。
(实验与结论)
(1)小亮同学为验证猜想3,取少量废液装入试管中,然后滴入酚酞溶液,发现溶液不变色,于是小亮认为猜想3正确。你认为他的结论____(填“正确”或“错误”),理由是______________。
请你另设计实验方案验证猜想3:
实验步骤
实验现象
实验结论
__________________
__________________
猜想3正确
(2)验证猜想4,可选择的试剂有____________。
A.酚酞溶液B.氢氧化钾溶液C.稀硫酸D.氯化钡溶液
(拓展与应用)若废液中的溶质是NaCl和HCl,根据盐酸的性质,无需另加试剂,只要对废液进行____操作,即可从废液中得到NaCl固体。
-
科目: 来源: 题型:
查看答案和解析>>【题目】锌是促进人体生长发育的必须微量元素。下图为锌元素在元素周期表中的相关信息及原子结构示意图。下列说法正确的是( )
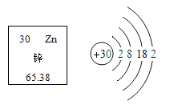
A. 锌属于非金属元素 B. 锌原子的中子数为30
C. 锌的相对原子质量为65.38g D. 锌原子在化学反应中易失去电子形成Zn2+
-
科目: 来源: 题型:
查看答案和解析>>【题目】最近,我国科学家成功合成新型催化剂,将CO2高效转化为甲醇(CH3OH)。这不仅可以缓解碳排放引起的温室效应,还将成为理想的能源补充形式。该化学反应的微观过程如下图所示。下列说法正确的是
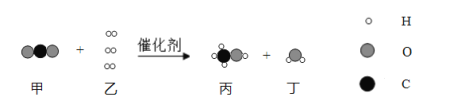
A. 该反应中四种物质均为化合物 B. 反应前后H元素的化合价不变
C. 参加反应的甲、乙分子个数比为1:3 D. 反应前后原子数目发生改变
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙两种物质(不含结晶水)的溶解度曲线如图所示,下列叙述正确的是( )

A. 甲和乙的溶解度相等且均为30g
B. 甲物质的溶解度随温度的升高而减小
C. a1℃时,乙的饱和溶液中溶质与溶剂的质量比为3:7
D. 将a2℃150g甲的饱和溶液降温到t1℃,有20g固体析出
相关试题

