【题目】利用超临界水技术处理废弃电路板,能得到由CuO和Cu2O组成的固体残渣,将残渣进行进一步处理可得硫酸铜晶体(CuSO45 H2O)等物质。处理流程如下图所示。下列说法正确的是 ( )
(已知:Cu2O + H2SO4 CuSO4 + Cu + H2O)
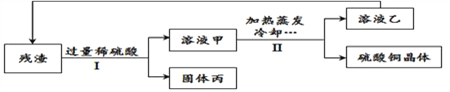
A. I中含过滤操作,II中不含过滤操作
B. 溶液甲和溶液乙一定为硫酸铜的饱和溶液
C. 残渣的处理流程中,H2SO4和CuSO4实现了循环利用
D. 经操作I后,残渣由22.4g减少为6.4g,则经过一次循环后能得到硫酸铜晶体50.0g
参考答案:
【答案】C
【解析】A、经过I、Ⅱ操作,得到了固体和液体,所以I、Ⅱ的操作中都有过滤,错误;B、溶液甲和溶液乙中均含硫酸铜,溶液甲不一定是硫酸铜的饱和溶液,溶液乙一定是硫酸铜的饱和溶液,错误;C、稀硫酸可以用于溶解滤渣,硫酸铜溶液可用于再次结晶,在流程中H2SO4和CuSO4实现了循环利用,正确;D、残渣由22.4g减少为6.4g,说明Cu2O 和 H2SO4反应生成6.4g的铜。设:生成6.4g的铜,同时生成的硫酸铜的质量为x,需要的质量为y
Cu2O + H2SO4 CuSO4 + Cu + H2O
144 160 64
Y x 6.4g
![]() x=16g
x=16g
![]() y=14.4g
y=14.4g
CuO和Cu2O组成的固体残渣中CuO的质量=22.4g-14.4g=8g,设:8g的CuO生成硫酸铜的质量为z
CuO+H2SO4=CuSO4+H2O
80 160
8g z
![]() z=16g
z=16g
经操作I后生成的硫酸铜的质量=16g+16g=32g,若硫酸铜全部转化为硫酸铜晶体,硫酸铜晶体的质量=32g÷![]() ×100%=50g,但在加热蒸发、冷却过程中有一部分硫酸铜在溶液乙中,所以经过一次循环后能得到硫酸铜晶体的质量小于50.0g,错误。故选C。
×100%=50g,但在加热蒸发、冷却过程中有一部分硫酸铜在溶液乙中,所以经过一次循环后能得到硫酸铜晶体的质量小于50.0g,错误。故选C。
-
科目: 来源: 题型:
查看答案和解析>>【题目】镁铜合金常用作飞机天线等导电材料,现取某镁铜合金3g放入烧杯中,加入50g稀硫酸恰好完全反应,反应后测得烧杯中剩余物的质量为52.8g。请计算:
(1)生成H2的质量为____________。
(2)该稀硫酸中溶质的质量分数为____________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是
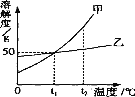
A.t1℃时,甲、乙两种物质的溶解度都是50g
B.t2℃时,在两种饱和溶液中,溶质的质量甲一定大于乙
C.t2℃时,将甲的饱和溶液降温至t1℃,其溶质的质量分数减小
D.t1℃时,将30g甲放到50g水中,所得溶液的溶质质量分数为37.5%
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列装置操作图不能用于检查气密性的是 ( )
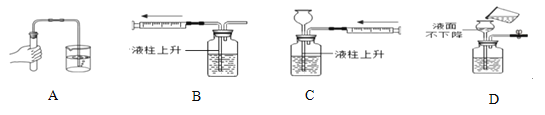
A. A B. B C. C D. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】葡萄糖存在于葡萄糖汁和其他带甜味的水果里,是一种重要的营养物质,是人类生命活动所需能量的重要来源之一,下列关于葡萄糖的说法正确的是
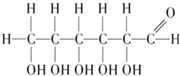
A. 葡萄糖分子中碳元素的质量分数最小
B. 葡萄糖的相对分子质量是180g
C. 葡萄糖分子中C、H、O三种元素的原子个数比为1 :2 :1
D. 葡萄糖是多原子分子构成的有机高分子化合物
-
科目: 来源: 题型:
查看答案和解析>>【题目】以甲为原料合成化工产品丁的微观过程如下图。下列说法正确的是

A. 每个丁分子由6个原子构成 B. 转化①中乙和丙的分子个数之比为1 : 1
C. 甲中氢元素的质量分数小于丁 D. 乙、丁都是氧化物
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据图示实验装置,回答下列问题。

(1)图中a仪器的名称:a________________,b_____。
(2)用高锰酸钾固体制氧气,该反应的化学方程式是___________________________。将装置A和D连接进行此实验,实验结束,停止加热前要先______,目的是______。
(3)写出实验室制取二氧化碳的化学方程式________________,其发生装置可用C(多孔隔板用来放块状固体)代替B的优点是________________,如用E装置收集CO2,则气体应从____________端通入(填“c”或“d”)。
相关试题

