【题目】用下列装置进行实验,请回答下列问题.
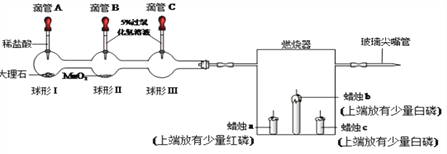
(1)同时挤压滴管B和C,控制滴入相同的液体量,下列说法正确的是____
a. 球形II中MnO2加快反应的速率
b.球形III中产生的气体少
c.反应过程中球形II比球形III内反应剧烈
(2)微热燃烧器,蜡烛b、c燃烧,a不燃烧,关于该步骤实验分析正确的是_______
a.可以探究燃烧需要温度达到着火点
b.可以探究燃烧需要氧气
c.说明白磷和红磷由同种元素组成
(3)挤压滴管A,滴入足量的稀盐酸到球形I中,一段时间后,蜡烛先熄灭,过一会蜡烛b也熄灭了,原因是______________________________
(4)蜡烛熄灭后,在玻璃尖嘴管处放内壁沾有澄清石灰水的烧杯,发现石灰水变浑浊,能否证明蜡烛含有碳元素,为什么_______________________
参考答案:
【答案】 a c a 二氧化碳隔绝氧气或二氧化碳不能燃烧也不能支持燃烧、密度比氧气大 不能,因为燃烧器中有球形I中产生的二氧化碳
【解析】(1)同时挤压滴管B和C,控制滴入相同的液体量。a、球形II中MnO2加快反应的速率,二氧化锰是该反应的催化剂,故a正确;b、球形III中产生的气体不少,只是产生的气体速率慢,故b错误;c、反应过程中球形II比球形III内反应剧烈,II中有催化剂,III中没有催化剂。故选ac。(2)微热燃烧器,蜡烛b、c燃烧,a不燃烧。a、可以探究燃烧需要温度达到着火点,故a正确;b、不可以探究燃烧需要氧气,故b错误;c、不能说明白磷和红磷由同种元素组成,故c错误。(3)挤压滴管A,滴入足量的稀盐酸到球形I中,一段时间后,蜡烛先熄灭,过一会蜡烛b也熄灭了,原因是二氧化碳隔绝氧气或二氧化碳不能燃烧也不能支持燃烧、密度比氧气大。(4)蜡烛熄灭后,在玻璃尖嘴管处放内壁沾有澄清石灰水的烧杯,发现石灰水变浑浊,不能证明蜡烛含有碳元素,原因是因为燃烧器中有球形I中产生的二氧化碳。
点睛∶充分利用控制变量法设计对比实验,是实验探究的重要方法。二氧化碳不能燃烧也不能支持燃烧、密度比氧气大,可以用来灭火。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列四个坐标图分别表示四个实验过程中某些量的变化,其中不正确的是( )


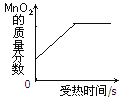
过氧化氢
溶液分解
B.向盐酸和氯化钙的混合溶液中滴加
碳酸钠溶液
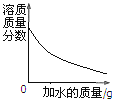
C.在一定温度下,向有氯化钠固体的氯化钠溶液中加入水搅拌
D.给氯酸钾和二氧化锰的混合物加热
A. A B. B C. C D. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学就在我们身边,它与我们的生活息息相关。当今社会,随着汽车数量的急剧增加,能源和环保问题日趋严峻,用电力驱动代替燃油的电动汽车被称为“未来汽车”。请回答下列问题:

(1)图中标示物属于金属材料的是_____ (填序号),属于合成材料的是______(填序号)
(2)汽车制造要使用大量的钢铁,请写出以赤铁矿为原料炼铁的化学方程式_________。
(3) 铬(Cr)为不锈钢主要的添加的元素。比较Cr的金属活动性强弱。相同温度下,取大小相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别投入________________相同的足量稀盐酸中(生成物中Cr显+2价),现象如下:
金属
Cr
Mg
与盐酸反应现象
放出气泡速率缓慢
放出气泡速率较快
①上述三种金属的活动性由强到弱的顺序是_______________。
②从上述实验可知,Cr能跟CuSO4溶液反应,方程式是____________
-
科目: 来源: 题型:
查看答案和解析>>【题目】A、B、C三个烧杯中盛有相同质量的水(其中A、C烧杯中水温为10 ℃,B烧杯中水温为30 ℃,不考虑溶解过程中温度的变化),分别加入甲、乙两物质各10 g,充分溶解后所得现象如图1所示,试回答:
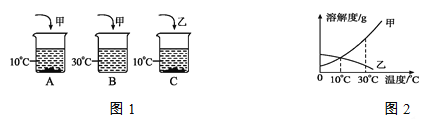
(1)你认为____烧杯中的溶液可能是不饱和溶液。
(2)图2是甲、乙两种物质的溶解度曲线图,按图分析,10 ℃时,A、C两烧杯中未溶解的溶质质量关系是____ (填“相等”或“不相等”)。其他条件不变,将C烧杯中的温度升到30 ℃时,C烧杯中的溶液是______ (填“饱和”或“不饱和”)溶液。
(3)若将A烧杯中的溶质全部溶解,可采用的方法有:_______________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】控制变量法是实验探究的重要方法.利用如图所示的实验不能实现的探究目的是( )
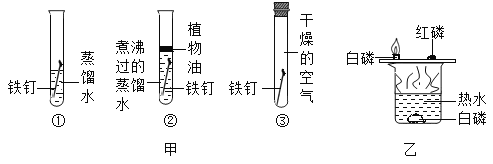
A.甲图中①②对比可探究铁的锈蚀与植物油是否有关
B.甲图中①③对比可探究铁的锈蚀与水是否有关
C.乙可探究可燃物的燃烧是否需要达到一定温度
D.乙可探究可燃物的燃烧是否需要与氧气接触
-
科目: 来源: 题型:
查看答案和解析>>【题目】(7分)四氧化三铁可用于医疗器械、电子等工业。某实验兴趣小组从工厂采集废液(含FeSO4和少量ZnSO4、MgSO4),进行四氧化三铁的制备实验。
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH范围如表所示。
Zn(OH)2
Fe(OH)2
Mg(OH)2
开始沉淀的pH
5.7
7.6
10.4
沉淀完全的pH
8.0
9.6
12.4
(2)25℃时,Zn(OH)2可溶于pH>10.5的碱溶液。
(3)制备Fe3O4的实验流程如下:
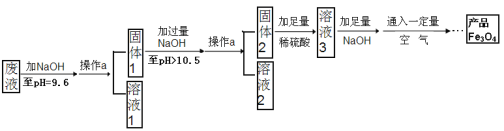
【回答问题】
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为 (写出其中一个)。
(2)操作a的名称为 。该操作需要的玻璃仪器有烧杯、玻璃棒、 等。玻璃棒在此操作中的主要作用是 。
(3)溶液1所含溶质有 (至少写两种成分的化学式);溶液3所含溶质的主要成分为 (写名称)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图甲、乙两种物质(不含结晶水)的溶解度曲线。下列有关说法正确的是( )
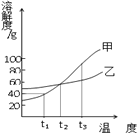
A. t2℃时,甲、乙溶液中溶质的质量分数一定相等
B. t1℃时,甲的溶解度为40
C. t3℃时,甲、乙的饱和溶液分别恒温蒸发相同的水,甲析出的晶体的质量比乙多
D. 甲的溶解度大于乙的溶解度
相关试题

