【题目】某化学小组将刚制取的二氧化碳气体通入含有少量过氧化钠(Na2O2)粉末(过氧化钠为淡黄色固体)的玻璃管中,看到玻璃管另一端有气泡冒出,同时粉末由淡黄色变为白色。
【提出问题】
过氧化钠与二氧化碳是否反生反应?生成了什么物质?
【作出猜想】
甲同学:没反应,冒出的还是二氧化碳气体
乙同学:发生反应,生成碳酸钠
丙同学:发生反应,生成一氧化碳
丁同学:发生反应,生成氧气
(1)大家一致认为甲同学的推测不正确,理由是________________________。
【实验探究】

__________________ __________________ ________________
【得出结论】
(5)过氧化钠与二氧化碳反应的化学方程式为____________________________________。
【反思拓展】
(6)根据过氧化钠的这一性质,请你设想过氧化钠的一种用途___________________。
参考答案:
【答案】 因为通入二氧化碳后,粉末由淡黄色变成了白色,生成了新物质 没有生成一氧化碳 带火星的木条复燃 滴加无色酚酞溶液 2Na2O2+2CO2 =2Na2CO3+O2 可以在缺氧的场所,将人们呼出的二氧化碳转换为氧气
【解析】将二氧化碳气体通入过氧化钠(Na2O2)粉末(过氧化钠为淡黄色固体)的玻璃管中,有气泡冒出,同时粉末由淡黄色变为白色。【提出问题】过氧化钠与二氧化碳是否反生反应?生成了什么物质?【作出猜想】甲:没反应,冒出的还是二氧化碳气体;乙:发生反应,生成碳酸钠;丙:发生反应,生成一氧化碳;丁:发生反应,生成氧气。(1)甲推测不正确,理由是因为通入二氧化碳后,粉末由淡黄色变成了白色,生成了新物质,发生了反应。【实验探究】实验方法:①用试管收集生成的气体,堵住试管口,移近酒精灯火焰,点燃;②实验现象:无现象;③实验结论:没有生成一氧化碳,一氧化碳具有可燃性,可以燃烧。实验方法:①试管收集生成的气体,用带火星的木条伸入试管内;②实验现象:带火星的木条复燃;③实验结论:有氧气生成,氧气可以使带火星的木条复燃。实验方法:①把反应后的固体配成溶液,向溶液中滴加无色酚酞溶液;②实验现象:溶液变红;③实验结论:溶液显碱性,碱性溶液可以使无色酚酞溶液变红。【得出结论】(5)过氧化钠与二氧化碳反应的化学方程式为2Na2O2+2CO2 =2Na2CO3+O2。【反思拓展】(6)根据过氧化钠的这一性质,设想过氧化钠的一种用途是可以在缺氧的场所,将人们呼出的二氧化碳转换为氧气,物质的性质决定物质的用途。
点睛∶这是一道实验探究题,二氧化碳气体与过氧化钠粉末(过氧化钠为淡黄色固体)反应生成氧气和白色的碳酸钠。一氧化碳具有可燃性,使带火星的木条复燃是我们检验氧气常用的方法。
-
科目: 来源: 题型:
查看答案和解析>>【题目】过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用。某学生为了验证这一实验,以足量的大理石、足量的盐酸和过氧化钠样品为原料,制取O2,设计出如下实验装置:(提示:无水硫酸铜遇水变蓝)
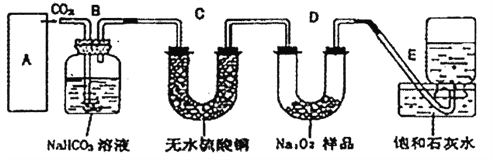
(1)B装置的作用________,C装置内可能出现的现象是________。
(2)为了检验E中收集到的气体,在取出集气瓶后,接下来应如何操作,请你说出检验的方法和相应的现象__。
(3)E中饱和石灰水的作用是________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知金属钠和水能发生下列反应:2Na+2H2O=2NaOH+H2↑。现取金属钠9.2g投入到100g水中,充分反应后,冷却到室温(20℃),得到一种不饱和溶液,向所得溶液中逐滴滴入MgSO4溶液,实验测得溶液的总质量与滴入MgSO4溶液的质量关系曲线如图所示。
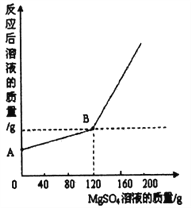
根据题意回答下列问题
(1)金属钠和水充分反应后,生成氢气的质量为________g。
(2)图中A点的纵坐标表示的溶液的质量是________g。
(3)通过计算求出当滴入120 g MgSO4溶液时,所得溶液中溶质的质量分数是多少_____?(计算结果精确至1%)
-
科目: 来源: 题型:
查看答案和解析>>【题目】请结合下列实验装置,回答问题

(l)写出仪器b的名称:b________。
(2)实验室制取气体时,组装好仪器后,应先_________,再添加药品。
(3)用石灰石和稀盐酸制取并收集二氧化碳,选用的装置为________(填字母)。反应的化学方程式:__________________________。
(4)用装置C收集氧气时,下列实验操作不正确的是______(填序号)。
a.加热前,将集气瓶装满水,用玻璃片盖住瓶口,倒立在盛水的水槽中
b.加热后,观察到水中导管口开始有气泡时,立即收集气体
c.待集气瓶里的水排完后,在水面下用玻璃片盖住瓶口,移出水槽正放在桌面上
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组对某假黄金(铜锌合金)样品进行实验探究,称取样品10.0克于烧杯中,再将100.0克稀硫酸逐滴滴入,实验情况如下图所示。求:
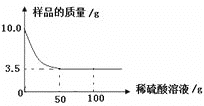
(1)铜锌合金中,锌的质量是__________。
(2)所用稀硫酸中溶质的质量分数是_______?
-
科目: 来源: 题型:
查看答案和解析>>【题目】以下归纳和总结完全正确的一组是
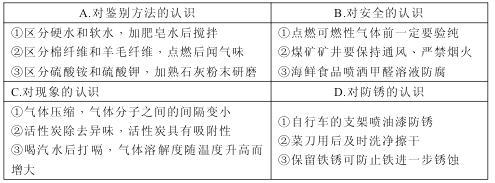
A. A B. B C. C D. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙两种固体物质的溶解度曲线如右图所示。下列说法正确的是
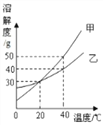
A. 20℃时,甲溶液中溶质的质量分数一定等于乙溶液的中溶质的质量分数
B. 将40℃时甲的一定量饱和溶液降温至20℃,溶液质量不变
C. 甲的溶解度大于乙的溶解度
D. 40℃时,分别在100g水中各加入30g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液
相关试题

