【题目】溶解度可表示物质溶解性的大小。
①左下图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。
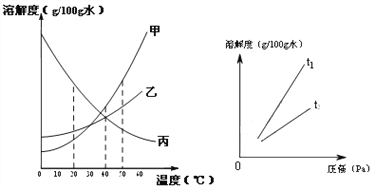
Ⅰ.20℃时,甲的溶解度________(填“>”、“<”或“=”)乙的溶解度。
Ⅱ.40℃时,乙和丙________(填“能”或“不能”)形成溶质质量分数相同的饱和溶液。
Ⅲ.20℃时,烧杯中分别盛有相同质量甲、乙、丙的饱和溶液,各加入等质量的对应固体,并升温至50℃。请填写下表。
烧杯中的溶质 | 烧杯中固体的变化 |
甲 | __________________ |
乙 | 固体逐渐减少至全部溶解 |
丙 | __________________ |
②气体的溶解度也有一定的变化规律。
Ⅰ.打开可乐瓶,逸出大量气泡。由此可见,压强越小,CO2的溶解度越_________。为增大CO2的溶解度,可采用的一种方法是________。
Ⅱ.不同温度下,氧气的溶解度随压强的变化如右图所示,图中t1对应的温度为40℃,则t2对应的温度________(填编号)。
a.大于40℃ b.小于40℃ c.无法确定
参考答案:
【答案】 < 能 固体逐渐减少,至全部溶解 固体逐渐增加 小 降温(或加压) a
【解析】①Ⅰ、根据溶解度曲线可知:甲的溶解度<乙的溶解度;
Ⅱ、40℃时,乙和丙的溶解度相同,并根据饱和溶液中质量分数的计算式![]() ×100%可知:40℃时,可形成两种物质的溶质质量分数相同的饱和溶液;
×100%可知:40℃时,可形成两种物质的溶质质量分数相同的饱和溶液;
Ⅲ、甲和乙的溶解度随温度的升高而逐渐增大,所以升高温度烧杯中的固体将逐渐减少,至全部溶解;丙的溶解度随温度的升高而逐渐减小,所以升高温度,丙烧杯中固体的质量将逐渐增加;
故答案为:
Ⅰ、<;
Ⅱ、能;
Ⅲ、
烧杯中的溶质 | 烧杯中固体的变化 |
甲 | 固体逐渐减少,至全部溶解 |
乙 | 固体逐渐减少至全部溶解 |
丙 | 固体逐渐增加 |
Ⅱ、气体的溶解度随温度的升高而逐渐减小,由图2可知:t1时的溶解度要大于t2时的溶解度;所以t2对应的温度对应的温度要大于40℃;
故选a.
-
科目: 来源: 题型:
查看答案和解析>>【题目】把某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入等质量的甲、乙两种金属,反应后金属都没有剩余.产生H2的质量随时间变化的趋势如图.下列说法正确的是( )
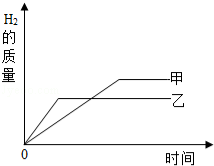
A.甲的活动性比乙强
B.甲的相对原子质量一定比乙小
C.反应消耗等质量的硫酸
D.反应消耗等质量的金属
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列图中能正确反映其对应关系的是 ( )

A. 向氢氧化钠溶液中不断加水,溶液pH与加入水的质量的关系
B. 向盛有氧化铜的烧杯中加入稀盐酸至过量,生成氯化铜质量与加入稀盐酸质量的关系
C. 一定量的稀硫酸与锌粒反应,溶液的质量与反应时间的关系
D. 向氯化铜和硝酸铜的混合溶液中滴加氢氧化钠溶液,生成沉淀与加入氢氧化钠溶液的质量关系
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化工厂排放的废液中含有大量的硫酸锌和硫酸铜,化学兴趣小组的同学根据所学知识设计了一个方案,用来回收金属铜并得到硫酸锌晶体,主要过程如下图所示:

请回答下列问题:
(1)步骤②中分离物质的方法是_________。
(2)固体A的成分是_________。
(3)步骤②中发生反应的化学方程式为__________________,
(4)步骤③中加入的B物质是____________。
-
科目: 来源: 题型:
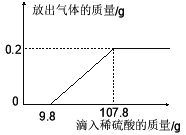
查看答案和解析>>【题目】在烧杯中加入2.14g久置的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如右图所示。请回答下列问题:
(1)产生氢气 g,刚开始滴加稀硫酸没有氢气放出的原因是 。
(2)所滴加的稀硫酸中溶质的质量分数。
(3)铝箔中铝元素的质量。
-
科目: 来源: 题型:
查看答案和解析>>【题目】“过碳酸钠”(2Na2CO3·3H2O2)俗称固体双氧水,它既有碳酸盐的性质,又有双氧水的不稳定性和氧化性,是很好的消毒剂和供氧剂,广泛应用于洗涤、印染和医药等领域。“过碳酸钠”的制备流程如下:
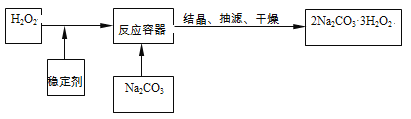
请回答下列问题:
⑴H2O2在催化或受热条件下易分解,其化学方程式为______________________;在上述流程中,向反应前的H2O2中加入稳定剂的作用是______________________。
⑵在“过碳酸钠”中加入下列物质时,不会导致“过碳酸钠”变质的是_______(填序号)。
A.二氧化锰 B.稀盐酸 C.硫酸钠 D.石灰水
⑶“过碳酸钠”极易分解,得到碳酸钠、水和氧气,其反应方程式可表示为
2(2Na2CO3·3H2O2)
 4Na2CO3+6H2O+3O2↑
4Na2CO3+6H2O+3O2↑请通过计算说明:①若“过碳酸钠”分解产生氧气12g,则同时产生碳酸钠的质量是____?
②若将上述产生的碳酸钠全部配制成溶质质量分数为10.6%的溶液,需加水的质量是________?
-
科目: 来源: 题型:
查看答案和解析>>【题目】镍在元素周期表中的信息如下图所示,下列有关镍元素的说法不正确的是
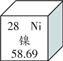
A. 原子序数是28 B. 属于金属元素
C. 原子中的质子数是28 D. 相对原子质量为58.69 g
相关试题

