【题目】高纯氧化钙是用于电子工业的重要无机化工原料,用生石灰(主要成分为CaO)制备高纯氧化钙的工艺流程如下:
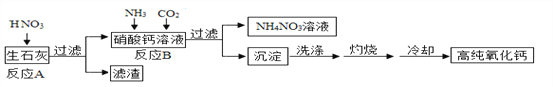
请回答下列问题:
(1)过滤操作中玻璃棒的作用是_______________;
(2)反应B的化学方程式为________________________;
(3)灼烧时发生反应的化学方程式为_________,该工艺流程中可循环使用的物质是_________;
(4)冷却需在密闭和干燥的环境中进行,否则制得的高纯氧化钙中会混有的两种杂质名称分别是___________和__________。
参考答案:
【答案】 引流 Ca(NO3)2+2NH3+CO2+H2O==CaCO3↓+2NH4Cl CaCO3 ![]() CaO+CO2↑ CO2 氢氧化钙 碳酸钙
CaO+CO2↑ CO2 氢氧化钙 碳酸钙
【解析】(1)过滤操作中玻璃棒的作用是引流;
(2)反应B中发生反应的化学方程式为:CO2+2NH3H2O+Ca(NO3)2═2NH4NO3+CaCO3↓+H2O;
(3)反应物是碳酸钙,生成物是氧化钙和二氧化碳,反应条件是高温,二氧化碳后面标上上升符号,所以化学方程式是:CaCO3 ![]() CaO+CO2↑;因为碳酸钙受热分解能生成二氧化碳,二氧化碳在前边的反应中是反应物,所以该工艺流程中可循环使用的物质是二氧化碳;
CaO+CO2↑;因为碳酸钙受热分解能生成二氧化碳,二氧化碳在前边的反应中是反应物,所以该工艺流程中可循环使用的物质是二氧化碳;
(5)冷却需在密闭和干燥的环境中进行,否则制得的高纯氧化钙能和水反应生成氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙和水。
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学用语是学习化学的重要工具。
(1)用化学符号表示:
①2个铁原子__________; ②3个二氧化硫分子________;③氯酸钾中氯元素的化合价________; ④镁离子__________。
(2)用字母序号填空:a.活性炭 b.生石灰 c.干冰 d.葡萄糖
①可用于人工降雨的是_______; ②可直接进入血液补充能量的是___;③可以用来吸附色素等物质的是_______;④可用食品干燥剂的是___________。
(3)写出下列反应的化学方程式:
①红磷在空气中燃烧_________; ②氯化钡溶液与硫酸钠溶液反应_________;③用少量稀盐酸除去铁器表面的“锈迹”__________;④电解饱和食盐水制烧碱,同时生成氢气和氯气(Cl2)_________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学与生活密切相关
(1)改善空气质量、保护水土资源是实现美丽中国的基础。
①下列气体的排放会导致形成酸雨的是______(填字母序号,下同)。
a.CH4 b.SO2 c.CO2 d.NO2
②下列处理方法属于中和反应的是_______。
a.用氨水处理废水中的硫酸 b. 用小苏打治疗胃酸过多
c.用铁粉从废水中的硫酸铜中回收铜 d.用硫酸铜和熟石灰配制波尔多液
③下列做法会造成土壤重金属污染的是_______。
a.作物秸杆露天焚烧 b. 废旧电池就地填埋
c.废旧塑料随意丢弃 d. 生活污水任意排放
(2)改善生活水平、提高生活质量是实现美丽中国的保障。
①下列食物中富含淀粉的是______(填字母序号);

②饼干中常添加碳酸钙,目的是补充钙元素,可以预防____(填字母序号);
a.甲状腺疾病 b.贫血病 c.骨质疏松,佝偻病 d.智力低下,侏儒症
③材料的发展与应用促进了人类社会的进步。碳晶地暖环保、节能、安全,其构造如图所示。
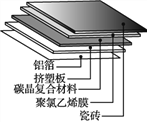
其中属于金属材料的是______;属于有机高分子合成材料的是挤塑板和_______。
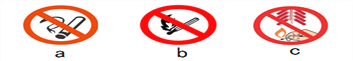
④为减轻大气污染,我市已经在主城区禁止燃放烟花爆竹。“禁止燃放烟花爆竹”的标识是______(填字母)。
(3)创新发展材料技术科推动人类社会的进步。
①石墨烯(见下图)可用作太阳能电池的电极,这里主要利用了石墨烯的_________性。

②LiMn2O4是锂离子电池的一种正极材料,可通过MnO2与Li2CO3煅烧制备,同时还生成CO2和一种单质。写出该反应的化学方程式:_________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】草酸镍晶体(NiC2O4·2H2O)可用于制镍催化剂。某小组用废镍催化剂(成分为Fe2O3、Ni、Fe、SiO2等)制备草酸镍晶体的部分实验流程如下:
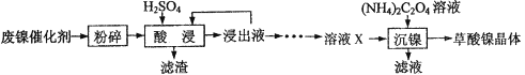
已知:①Ni能和稀H2SO4反应。
②相关金属离子生成氢氧化物沉淀的pH如下表:
金属离子
开始沉淀的pH
完全沉淀的pH
Fe3+
1.1
3.2
Fe2+
5.8
8.8
Ni2+
6.7
9.5
③H2O2能将Fe2+氧化为Fe3+
(1)废镍催化剂“粉碎”的目的是______。
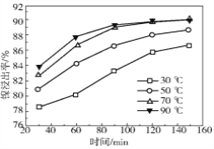
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图,“酸浸”的适宜温度与时间分别为 _______(填字母)。
A.30℃、30min B.90℃、150min C.70℃、120min D.90℃、120min
(3)“酸浸”中发生的复分解反应方程式为________。
(4)“浸出液”得到“溶液x”过程中,加入试剂先后顺序是_____(填字母)。
A.先加H2O2溶液,再加NaOH溶液 B.先加NaOH溶液,再加H2O2溶液
加NaOH溶液调节pH_____(填范围),充分反应后得到滤渣的操作是______,该操作中所用到的玻璃仪器有玻璃棒、烧杯和_________。
(5)将“沉镍”工序:①主要过程为:蒸发浓缩、_____ 、过滤,所得固体用75%乙醇洗涤、110℃下烘干,得草酸镍晶体。
②用75%乙醇洗涤的目的是洗去杂质、___________;
③烘干温度不超过110℃的原因是______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】工业废料石膏(CaSO42H2O)可以“变废为宝”,用于生产氧化钙、硫酸钾、电石(化学名称为碳化钙)等。某研究性学习小组展开了如下系列研究。
一、高纯CaO的制备
【资料一】
Ⅰ.石膏(CaSO42H2O)与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。
Ⅱ.SO2能使品红溶液褪色,也能使澄清石灰水变浑浊。
甲同学用如图1装置制备CaO并验证石膏与焦炭高温反应的其他产物。
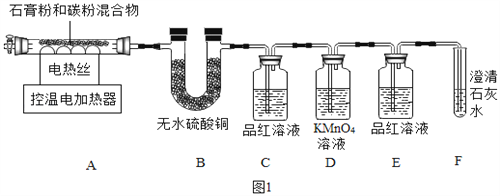
实验过程中发现:B中无水硫酸铜变蓝;C中产生__现象证明有SO2生成;装置__中无明显变化和装置F中__现象证明有CO2生成。写出石膏与碳粉在高温条件下反应的化学方程式:____。
二、硫酸钾和电石的制备
乙同学模拟生产化肥硫酸钾和电石的流程如图2:
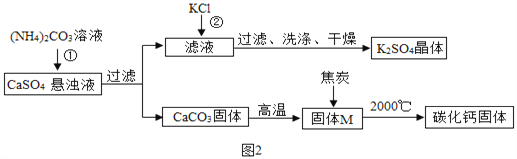
【资料二】CaO与C在高温下反应生成碳化钙(化学式为CaCx)和CO。
(1)反应①的化学方程式为___。证明固体M中不含CaCO3的方法是____(写出实验的方法、现象)。
(2)反应②的化学方程式为(NH4)2SO4+2KCl═K2SO4↓+2NH4Cl,该反应能析出K2SO4晶体的原因是__。
三、假设上述流程中制得的碳化钙(化学式为CaCx)固体中只含杂质CaO,乙小组同学为测定CaCx中x的值进行如下实验。
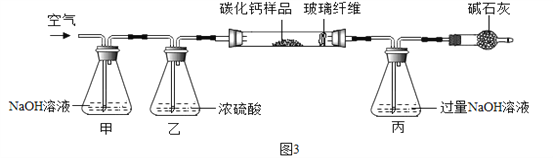
【资料三】CaCx在空气中灼烧生成CaO和CO2。
步骤一:称取3.76g样品于图3所示石英管中(测定装置图如图3,夹持及加热装置省略),反应前缓缓通入空气,高温灼烧石英管中的样品至反应完全后继续缓缓通入空气,测得丙溶液的质量比反应前增重了4.4g。(玻璃纤维可防止固体粉末进入导管)
步骤二:将石英管内剩余固体全部转移到水中,加入足量碳酸钠溶液,经搅拌、过滤、洗涤、干燥等操作得到碳酸钙固体6克。试回答下列问题:
(1)装置甲的作用是__。反应完全后继续缓缓通入空气的目的是__。
(2)根据步骤一、二计算该样品中钙、碳、氧的质量比为___,
计算确定CaCx的化学式(请写出计算过程)______________。
(3)若碳酸钙未能完全干燥,则会导致CaCX中的x的值____(填“偏大”、“偏小”、“无影响”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是某化学反应的微观示意图,图中不同的圆球代表不同的原子。下列叙述正确的是( )
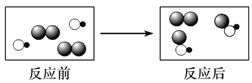
A. 该反应的生成物有2种
B. 该反应的基本类型是化合反应
C. 反应前后分子种类和原子种类均不变
D. 参加反应的两种物质的分子个数比为1∶1
-
科目: 来源: 题型:
查看答案和解析>>【题目】纳米材料常常具有一些特殊性质,纳米铁粉在隐形材料喷涂方面有着球形铁粉无可比拟的优越性,广泛用于国防军工领域,某化学小组通过动手实验制备纳米铁粉。
(查阅资料)
(1)用硫酸亚铁、草酸(H2C2O4)两溶液发生复分解反应来制备草酸亚铁(FeC2O4)。
常温下,草酸亚铁的溶解度较小。
(2)焙烧草酸亚铁: FeC2O4
 Fe+2CO2↑。
Fe+2CO2↑。(3)纳米铁粉在空气容易被氧化生成氧化铁。
(实验步骤)
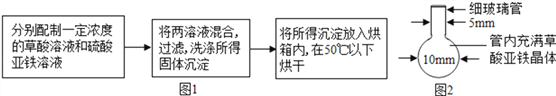
(1)草酸亚铁晶体的制备如图1
①若配制的硫酸亚铁溶液略呈黄色,可能原因是___________________;
②写出硫酸亚铁与草酸溶液反应的化学方程式_________________;
③为了分离所得固体沉淀物,需要的玻璃仪器有烧杯、玻璃棒_______;
④用冰水洗涤固体沉淀物到 pH =7为止的目的是_________________;
(2)纳米铁粉的制备如图2
将一根玻璃管在酒精喷灯上烧制成如图2所示形状,向其中加入黄色草酸亚铁晶体.当草酸亚铁粉末受热完全变黑,立即将管口部分放在火焰烧熔封闭,这样便得到了高纯度的纳米铁粉。
①分解草酸亚铁的实验中所产生的CO2对于该实验步骤所起的作用是________。
②指导老师提醒同学们应准确把握玻璃管的烧熔封闭时间.你认为烧熔过早、过晚的后果分别是______________________,___________。
相关试题

