【题目】海洋中蕴含着丰富的资源。
(1)海水淡化是解决淡水资源不足的重要方法。下列方法中,可以使海水淡化的是____(填字母序号)。
A.滤纸过滤 B.吸附 C.沉降 D.蒸馏
(2)从海水中提炼出来的重水(D2O)可作原子能反应堆中的减速剂和传热介质。重水中重氢原子(D)的相对原子质量是2,则重水中氧元素的质量分数为_________。
(3)利用海水制取纯碱和金属镁的流程如下图所示,试回答问题:
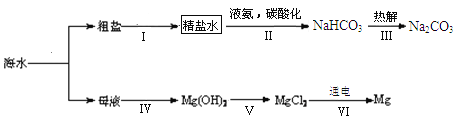
①1926年我国化学家______创立了联合制碱法,促进了世界制碱技术的发展,其第Ⅲ步反应的化学方程式为_________;
②步骤Ⅴ中所加试剂是__________。
参考答案:
【答案】 D 80% 侯德榜 2NaHCO3△ Na2CO3 + H2O + CO2↑ 稀盐酸(HCl)
【解析】(1)海水淡化是解决淡水资源不足的重要方法。使海水淡化的是蒸馏,滤纸过滤和沉淀是除去水中不溶物质,吸附色素和异味。(2) 重水(D2O) 中重氢原子(D)的相对原子质量是2,则重水中氧元素的质量分数为∶![]() ×100%=80%。(3)利用海水制取纯碱和金属镁。①1926年我国化学家侯德榜创立了联合制碱法,促进了世界制碱技术的发展,其第Ⅲ步反应的化学方程式为∶2NaHCO3
×100%=80%。(3)利用海水制取纯碱和金属镁。①1926年我国化学家侯德榜创立了联合制碱法,促进了世界制碱技术的发展,其第Ⅲ步反应的化学方程式为∶2NaHCO3![]() Na2CO3 + H2O + CO2↑。②步骤Ⅴ中所加试剂是稀盐酸(HCl),与氢氧化镁反应生成氯化镁。
Na2CO3 + H2O + CO2↑。②步骤Ⅴ中所加试剂是稀盐酸(HCl),与氢氧化镁反应生成氯化镁。
-
科目: 来源: 题型:
查看答案和解析>>【题目】为了研究炼铁的主要反应原理,某化学兴趣小组的同学用一氧化碳还原氧化铁做实验。装置如下图所示。请回答下列问题:
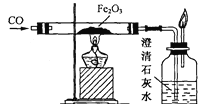
(1)在实验开始后可观察到如下现象:玻璃管中的粉末由_______色逐渐变为_______色,这说明了氧化铁在反应中失去了_______而被还原,这种粉末就是被还原出来的_______;澄清石灰水中出现_______,这说明一氧化碳夺取了氧化铁中的_______而被氧化,产生了_______气体。
(2)若一氧化碳是足量的,要制得56 g铁,至少需要氧化铁_______g,同时能产生二氧化碳_______g。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某工厂欲从只含有硫酸铜的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如下:
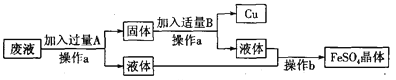
(1)操作a、b的名称分别是_______、_______。
(2)写出流程中有关反应的化学方程式:_______、_______。以上两个反应能够发生的原因是____________________________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列图像能正确反映其对应操作中各量变化关系的是( )
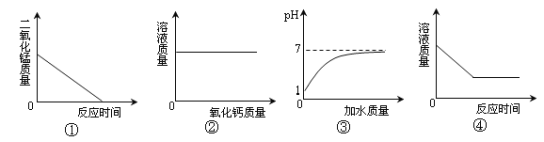
A.图①是给氯酸钾和二氧化锰的混合物加热
B.图②是向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体
C.图③是向pH=1的酸溶液中不断加水
D.图④是向一定质量的稀硫酸中加入锌粒
-
科目: 来源: 题型:
查看答案和解析>>【题目】分析下图内容回答问题。

(1)左图中海水属于_______(填“纯净物”或“混合物”)。海水中含有大量氯化钠,氯化钠是由______(填离子符号)和Cl-构成。
(2)右图试管A中气体的化学式为_______,试管B所对应的是电源的_____(填“正”或“负”)极。
(3)在水蒸发的过程中,下列说法正确的是__________(填字母序号,下同)。
A.水分子不断运动 B.水分子之间间隔不变
C.水分子大小不发生变化 D.水分子可以保持水的物理性质
(4)在电解水的过程中,下列说法正确的是___________。
A.水分子本身发生了改变 B.氢原子和氧原子数目没有发生变化
C.氢原子和氧原子种类发生了改变 D.氢原子和氧原子质量发生了变化
-
科目: 来源: 题型:
查看答案和解析>>【题目】某校化学课外兴趣小组的同学模仿物理课上学到的“串联电路”,设计了如下气体制备与性质验证的组合实验。试看图回答问题:
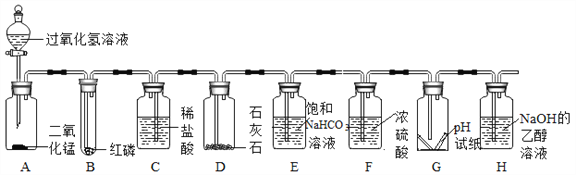
资料卡片:①红磷的着火点为260℃;②饱和NaHCO3溶液可用于吸收HCl气体;③20℃时,碳酸钠在乙醇中几乎不溶解;④氯化钙溶液呈中性。
(1)装置A可作为氧气或二氧化碳的发生装置是因为________且反应条件均不需要加热;
(2)反应开始后,B中充满氧气,但红磷仍未燃烧,原因是____________;
(3)装置G中有干和湿的pH试纸各一张,当通入二氧化碳一段时间后,湿的pH试纸显示pH约为6,干的pH试纸显示pH为7,同学们可得到的结论是____________;
(4)若装置H中溶液为饱和状态,反应一段时间后出现的现象是______________;
(5)反应完成后同学们对装置D中所得溶液的溶质成分展开探究:
【提出问题】装置D中溶液的溶质是什么?
【猜想与假设】小滨认为溶质只有CaCl2;
小崔认为除CaCl2外,可能还含有___________;
【实验与结论】小滨取反应后装置D中部分溶液于试管中,滴加酚酞试液,发现溶液颜色呈无色,于是小滨认为自己的猜想是正确的。
【反思与评价】小崔认为小滨的实验方案是错误的,理由是_________,为验证后一种物质是否存在,小崔同学可采用_________(填字母序号:A.碳酸钠溶液 B.石蕊试液 C.锌粒)来代替酚酞试液。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图为几种常见物质之间的转化关系(各字母代表一种物质,部分反应物,生成物及反应条件略去)。已知:①五种物质中均含铜元素,且化合物中铜元素的化合价均为+2;②A为单质,在空气中加热后生成黑色固体B;③X溶液与铁反应可得到A;④X溶液与氯化钡溶液反应可得到D,同时有白色沉淀生成;⑤D溶液中加入少量氢氧化钠溶液可得到蓝色沉淀E。试推断:
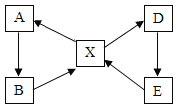
(1)E的化学式为_______,E与某种酸反应可实现E→X转化,该酸的名称是_______;
(2)试写出下列反应的化学方程式。
①A→B的化学方程式:________________;②X→A的化学方程式:________________。
相关试题

