【题目】(7分)某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组设计了如下实验方案:在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO2来进行分析测定。
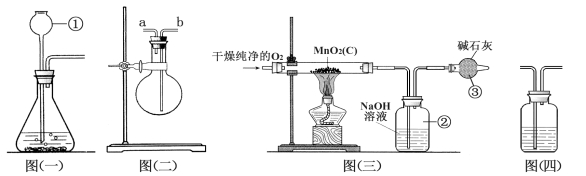
(1)仪器①的名称是 。如果该实验选择图㈠装置来制取氧气,反应的化学方程式为 。
(2)用图㈡装置可收集和干燥氧气:若烧瓶充满水来收集氧气,气体应从 (填“a”或“b”,下同)端通入;若在烧瓶内装入浓硫酸进行干燥气体,气体应从 端通入。
(3)图㈢是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰,其作用是____________________________。
(4)为验证图㈢中装置②已将CO2吸收完全,可在装置②与③之间加入图㈣装置进行证明,则图㈣装置中加入的试剂为______(填字母)。
A. NaOH溶液 B. 澄清石灰水 C. 浓硫酸
(5)称取5.0 g二氧化锰样品进行实验,图㈢中装置②反应前后的质量差为1.1 g,则样品中二氧化锰的质量分数为____________(填计算结果)
参考答案:
【答案】(1)长颈漏斗 2H2O2 MnO2 2H2O+ O2↑
(2)a b
(3)防止空气中的水和二氧化碳进入氢氧化钠溶液中
(4)B
(5)94%
【解析】
试题分析:(1)常见仪器的识记:长颈漏斗;气体发生装置的选择依据:反应物的状态和反应条件,选择图㈠装置来制取氧气,说明是固体和液体在常温下反应,故反应的化学方程式:2H2O2 MnO22H2O+O2↑
(2)用图㈡装置可收集和干燥氧气:若烧瓶充满水来收集氧气,则气体应从短管,即a端端通入;若在烧瓶内装入浓硫酸进行干燥气体,气体应从长管,即b端通入
(3)图㈢是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,即利用氧气与二氧化锰中的碳反应生成二氧化碳,然后利用装置②中的NaOH溶液来吸收,然后通过装置②的质量差,即反应生成的二氧化碳质量,故装置③中装有碱石灰,其作用是防止空气中的水和二氧化碳进入氢氧化钠溶液中 ,防止二氧化碳的质量偏大
(4)利用二氧化碳能使澄清石灰水变浑浊,为验证图㈢中装置②已将CO2吸收完全,可在装置②与③之间加入图㈣装置进行证明,则图㈣装置中加入的试剂为澄清石灰水,选B
(5)根据图㈢中装置②反应前后的质量差为1.1 g,即二氧化碳的质量为1.1 g ,故碳的质量=1.1g×12/44×100%=0.3g,故样品中二氧化锰的质量分数=(5.g-0.3g)/5.0g×100%=94%
-
科目: 来源: 题型:
查看答案和解析>>【题目】分别向Na2CO3、(NH4)2SO4、NaCl、NH4Cl四种溶液中加入下列试剂中的一种,便可将它们鉴别出来,这种试剂是( )
A.盐酸
B.氯化钙
C.氢氧化钠溶液
D.氢氧化钡溶液
-
科目: 来源: 题型:
查看答案和解析>>【题目】地壳中含量最多的元素是
A.铝 B.铁 C.硅 D.氧
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列是四种实验操作中各量变化关系的图像,能正确反映其对应操作的图像有
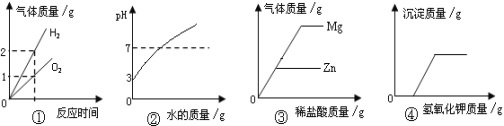
①电解水
②向一定量pH=3的盐酸溶液中不断加水稀释
③向等质量的镁和锌中分别加入溶质质量分数相同的稀盐酸至过量
④向盐酸和氯化铜的混合溶液中不断滴加氢氧化钾溶液
A.4个 B.3个 C.2个 D.1个
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是
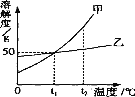
A.t1℃时,甲、乙两种物质的溶解度都是50g
B.t2℃时,在两种饱和溶液中,溶质的质量甲一定大于乙
C.t2℃时,将甲的饱和溶液降温至t1℃,其溶质的质量分数减小
D.t1℃时,将30g甲放到50g水中,所得溶液的溶质质量分数为37.5%
-
科目: 来源: 题型:
查看答案和解析>>【题目】(8分)钓鱼岛及其附属海域是我国固有领土,蕴藏着丰富的海洋资源。
(1)海水制盐。从海水制取的粗盐中含有泥沙、硫酸镁和氯化钙等杂质,为得到较纯的氯化钠,将粗盐溶于水,然后进行如下操作:a.加过量的Ba(OH)2溶液;b.加适量的盐酸;c.加过量的Na2CO3溶液;d.过滤;e.蒸发。正确的操作顺序是___________(填字母)。加Na2CO3溶液的作用是除去________。
用提纯的NaCl配制200g0.9%的生理盐水,需要NaCl的质量为 g。
①配制该溶液时所需要的玻璃仪器有:
②如果配制后溶液溶质的质量分数低于0. 9%,你认为可能的原因是 (写一个即可)
(2)海水制镁。从海水中提取金属镁的过程如下图所示:

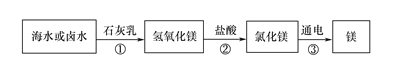
在上述转化过程中发生中和反应的方程式是 ________________ 。海水中本身就含有氯化镁,则①、②两步的作用是_______________
(3)海水“制碱”。氨碱法制纯碱中生成NaHCO3和NH4Cl的化学方程式为 _____
-
科目: 来源: 题型:
查看答案和解析>>【题目】(6分)石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到25g该石灰石样品中,得到如下部分数据和图象:
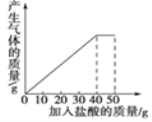
次数
第1次
第2次
第3次
加入盐酸的质量/g
10
10
10
剩余固体的质量/g
20
15
10
请计算:(1)石灰石样品中杂质的质量为 g。
(2)所加盐酸的溶质质量分数.
相关试题

