【题目】某同学进行中和反应实验:取适量氢氧化钠溶液于烧杯中,滴加几滴紫色石蕊试液,然后逐渐滴入稀硫酸,测得溶液的pH及颜色变化情况如下表。

(1)从表中获得的信息有:紫色石蕊试液遇碱变蓝,遇酸变红。请再写出两点。
①________________________________________________________________ 。
②________________________________________________________________ 。
(2)当加入7 mL稀硫酸时,溶液中的溶质为________________。
参考答案:
【答案】 加入4 mL稀H2SO4时,溶液显中性(或稀H2SO4,与NaOH溶液恰好完全反应或溶液显紫色或溶质为Na2SO4等)在溶液的pH接近7时,少量的酸即可使pH发生较大的变化 此NaOH溶液的pH=13.0(合理答案均可) Na2SO4、H2SO4
【解析】(1)表中还可以看出,在未加入稀硫酸时,氢氧化钠溶液的pH=13;随着稀硫酸的滴加,溶液的酸碱度越来越小;当滴加稀硫酸的量为4mL时,溶液的pH=7,此时恰好完全反应;继续滴加稀硫酸,溶液的pH继续减小;在接近恰好完全反应时,溶液的pH发生较大变化;(2)当加入4mL稀硫酸时,恰好完全反应,此时溶液为硫酸钠溶液;当加入7mL稀硫酸时,硫酸过量,此时溶液为硫酸钠和硫酸的混合溶液。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列实验现象中,描述正确的是( )
A.木炭在氧气中燃烧,有无色刺激性气味气体生成
B.镁条在盐酸中剧烈反应,产生大量气泡,试管壁发热
C.红磷在氧气中剧烈燃烧,放出热量,有大量白色气体生成
D.铁丝在空气中剧烈燃烧,放出大量的热,火星四射,有黑色熔融物溅落瓶底
-
科目: 来源: 题型:
查看答案和解析>>【题目】U形管中是滴有酚酞试液的蒸馏水,向左、右两管中分别同时逐滴滴加一定量的氢氧化钠稀溶液和稀盐酸(如图所示)。下列说法正确的是
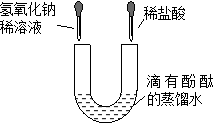
A.开始时左边溶液呈蓝色,右边溶液呈红色
B.开始时左边溶液呈无色,右边溶液呈红色
C.充分反应后U形管中溶液可能呈红色
D.充分反应后U形管中溶液一定呈无色
-
科目: 来源: 题型:
查看答案和解析>>【题目】小青同学为了制作叶脉书签,打算配制125 g 10%的NaOH溶液。
(1)计算小青需要称取NaOH的质量。
(2)小青将洗净的树叶放在配制好的溶液中煮沸后取出,溶液的质量减少5g,溶质质量分数也有所减小。为了测定剩下溶液中NaOH的质量分数,小青向溶液中逐滴加入7.3%的稀盐酸,当溶液pH=7时,消耗盐酸50 g。计算:
①生成NaCl的质量。
②剩下溶液中NaOH的质量分数。
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知甲、乙分别是盐酸和氢氧化钠溶液中的一种,如图所示表示向甲中加入乙时溶液pH的变化曲线。请写出你从曲线图中所获取的信息:
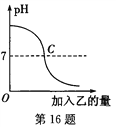
(1)甲是________。
(2)乙是________。
(3) ________________________________________________________。
(4) ________________________________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】除去二氧化碳中混有少量一氧化碳的方法正确的是( )
A.点燃混合气体
B.将混合气体通入水中
C.将混合气体通入澄清石灰水中
D.将混合气体通过灼热的氧化铜
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列实验现象记录正确且完整的是( )
A.镁在空气中燃烧,发出耀眼的白光,产生白烟,放出大量的热,生成白色固体物质
B.铁在空气中燃烧,火星四射,放出大量热,生成黑色固体
C.氢氧化铜使无色的酚酞试液变红色
D.硫在空气中燃烧,产生蓝色的光,放出大量的热
相关试题

