【题目】向Mg(HCO3)2溶液中加入一定量NaOH溶液,出现白色沉淀.某同学经过过滤、洗涤、低温烘干得白色固体,并作如下探究:
【猜测】
白色固体可能是:①Mg(OH)2;②MgCO3;③Mg(OH)2、MgCO3混合物.
【资料】
MgCO3、Mg(OH)2加热易分解,生成对应的两种氧化物.
【实验1】
(1)取适量白色固体,溶于___________________,出现_________(填现象),则猜测①不成立.
(2)另取适量白色固体,充分加热,产生的气体使无水CuSO4粉末变蓝,则猜测______(选填“②”或“③”)成立.
有同学查阅资料得知上述固体应为碱式碳酸镁[xMgCO3yMg(OH)23H2O],其不溶于水,加热易分解.
【实验2】
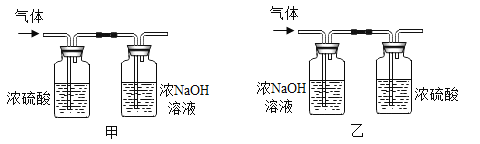
(3)为进一步确定白色固体的组成,该同学取适量白色固体,充分加热至质量不再改变,并使产生的气体全部缓缓通过如图_______(选填“甲”或“乙”)装置,测得生成气体的质量.
实验数据:
①加热后剩余固体质量1.60g;
②浓硫酸增重0.72g;
③浓NaOH溶液增重1.32g.
则:x:y=___________.
【延伸】
(4)将该碱式碳酸镁长期浸泡在浓NaOH溶液中,固体全部转化为Mg(OH)2.写出此反应的化学方程式_____________________________________________.
(5)工业上碱式碳酸镁可作阻燃剂,其可能的原因是__________(选填序号).
a、分解时吸热,降低可燃物的着火点
b、生成的固体覆盖燃烧物,隔绝氧气
c、生成的气体稀释了可燃物周围的氧气浓度.
参考答案:
【答案】 稀盐酸(或稀硫酸或稀硝酸等) 气泡 ③ 甲 3:1 3MgCO3Mg(OH)23H2O+6NaOH=4Mg(OH)2↓+3Na2CO3+3H2O bc
【解析】(1)猜想①不成立,也就是白色固体中含有碳酸镁,作为一种碳酸盐能与酸反应生成二氧化碳气体;(2)因为MgCO3、Mg(OH)2加热易分解,生成对应的两种氧化物,也就是碳酸镁加热分解为氧化镁和二氧化碳;氢氧化镁加热分解为氧化镁和水;充分加热,产生的气体使无水CuSO4粉末变蓝,这说明有水蒸气生成,也就是白色固体中一定含有氢氧化镁,则猜想③成立;(3)因为加热后生成了水蒸气和二氧化碳,所以要将生成气体先通过浓硫酸吸收生成的水蒸气;然后再通过浓氢氧化钠溶液吸收二氧化碳,否则会导致从氢氧化钠溶液中又带出部分水蒸气,造成误差;所以选择甲装置;
xMgCO3yMg(OH)23H2O![]() (x+y)MgO+(y+3)H2O+xCO2↑
(x+y)MgO+(y+3)H2O+xCO2↑
40(x+y) 44x
1.60g 1.32g
![]() ,故x:y=3:1;(4)碱式碳酸镁与氢氧化钠反应生成氢氧化镁沉淀、碳酸钠和水,此反应的化学方程式:3MgCO3Mg(OH)23H2O+6NaOH=4Mg(OH)2↓+3Na2CO3+3H2O;(4)a、可燃物的着火点是物质本身的属性,不会降低,故错误;b、生成的固体覆盖燃烧物,隔绝氧气,故正确;c、生成的气体稀释了可燃物周围的氧气浓度,故正确。故选bc。
,故x:y=3:1;(4)碱式碳酸镁与氢氧化钠反应生成氢氧化镁沉淀、碳酸钠和水,此反应的化学方程式:3MgCO3Mg(OH)23H2O+6NaOH=4Mg(OH)2↓+3Na2CO3+3H2O;(4)a、可燃物的着火点是物质本身的属性,不会降低,故错误;b、生成的固体覆盖燃烧物,隔绝氧气,故正确;c、生成的气体稀释了可燃物周围的氧气浓度,故正确。故选bc。
-
科目: 来源: 题型:
查看答案和解析>>【题目】请结合图1回答问题:
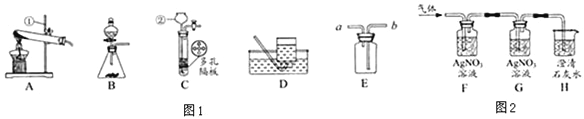
(1)仪器名称:①__________,②_________.
(2)用氯酸钾和二氧化锰制取氧气,可选用装置_______(选填序号)和D组合,反应的化学方程式为_________________________________,二氧化锰的作用是__________________.
(3)实验室可用装置B或C制H2,C装置相对于B的优点有___________.用E装置收集H2,气体应从_______(选填“a”或“b”)端通入.
(4)有同学将实验室制得的CO2通入澄清石灰水,石灰水未变浑浊,于是作如图2探究:
①实验室制CO2反应的化学方程式_______________________.
②装置F、H中溶液变浑浊,G中溶液不变浑浊,则原石灰水未变浑浊的原因是___________.
③装置G的作用是_________________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】铜、铁是人类使用最早、应用广泛的金属.
(一)对古代制品的认识
青铜铸件、丝绸织品、陶瓷器皿是我国古代劳动人民创造的辉煌成就.
(1)上述制品不涉及到的材料是______(选填序号).
A、金属材料 B、无机非金属材料 C、复合材料
(2)如图1为出土文物古代青铜铸件“马踏飞燕”.该文物能保存至今的原因可能是_____(选填序号).
A、铜的活泼性弱 B、铜不会生锈 C、深埋于地下,隔绝空气
(二)铁、铜的冶炼
①我国古代曾用孔雀石炼铜,涉及主要反应的化学方程式:_________,2CuO+C
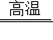 2Cu+CO2↑.
2Cu+CO2↑.②铁、铜矿石有赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、黄铁矿(FeS2)、黄铜矿(CuFeS2)等.CuFeS2为二硫化亚铁铜,其中S元素的化合价为______.
(1)工业炼铁大多采用赤铁矿、磁铁矿.以磁铁矿为原料炼铁反应的化学方程式为______________.
炼铁不采用黄铁矿、黄铜矿,可能的原因是:
①黄铁矿、黄铜矿含铁量相对低;②________________________________.
(2)以黄铜矿为原料,采用生物炼铜是现代炼铜的新工艺,原理为:4CuFeS2+17O2+2H2SO4
 4CuSO4+2Fe2(SO4)3+2H2O.
4CuSO4+2Fe2(SO4)3+2H2O.向上述反应后的溶液中加入Fe粉,得到FeSO4溶液和Cu.
①发生主要反应的化学方程式:Fe+Fe2(SO4)3=3FeSO4,________________________.
②FeSO4溶液经蒸发浓缩、___________、过滤等操作得到FeSO47H2O晶体.
(三)黄铜矿中铁、铜含量的测定
在科研人员指导下,兴趣小组称取25.00g黄铜矿(含少量Fe2O3和其它不含金属元素的杂质)模拟生物炼铜,使其全部转化为CuSO4、Fe2(SO4)3溶液.向溶液中加入过量NaOH溶液得到Cu(OH)2、Fe(OH)3固体.
(1)证明NaOH溶液过量的方法:静置,向上层清液中滴加________溶液,无现象.
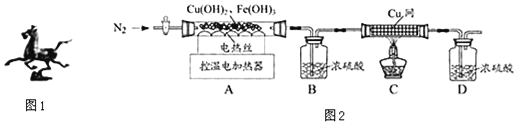
(2)用图2装置对固体进行热分解实验.
【资料】
①在68℃时,Cu(OH)2分解为CuO;在500℃时,Fe(OH)3分解为Fe2O3.
②在1400℃时,CuO分解为Cu2O和O2,Fe2O3分解为复杂的铁的氧化物和O2.
(1)装配好实验装置后,先要________________.
(2)停止加热后仍需继续通N2,可防止倒吸和______________________________.
(3)控制不同的温度对A中固体加热,测得装置B和C中铜网的质量变化如表.
温度/℃
室温
100
550
1400
B装置/g
200.00
201.80
205.04
205.04
C中铜网/g
100.00
100.00
100.00
101.28
①此黄铜矿中铜、铁元素的质量分数:ω(Cu)%=________;ω(Fe)%=__________.
②复杂的铁的氧化物化学式为__________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图为某些物质间的转化关系.E为常见的碱,F常作食品干燥剂,M为石膏的主要成分.部分反应物和生成物已略去.
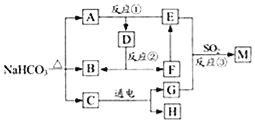
(1)化学式:C________,F_________.
(2)反应①、③的化学方程式:
①_____________________________________________,
③_____________________________________________.
(3)能体现明代《天工开物》中“煤饼烧石成灰”的反应是_____(选填反应序号).
(4)工业上可用B和H合成乙醇(C2H6O),反应中B和H的质量比为______.
-
科目: 来源: 题型:
查看答案和解析>>【题目】以下为制备纳米CaCO3的一种流程:
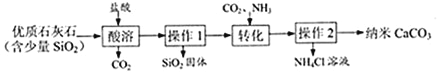
(1)实验室中进行操作1、2时,所用玻璃仪器有_____、玻璃棒和烧杯.
(2)过程中的生成物可直接应用于流程的是________.
(3)为了提高“转化”速率,可采取的措施有______(选填序号).
a、搅拌溶液 b、适当增大通入气体的速率 c、加热溶液至100℃
(4)操作2所得固体用蒸馏水洗涤.检验固体已洗净的方法是________________________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】加热一定量的高锰酸钾固体制氧气,下图所示的四个图象,能正确表示对应变化关系的是( )
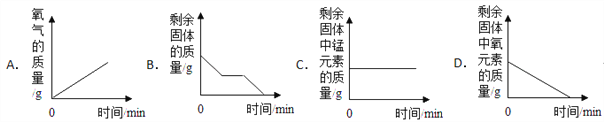
A. A B. B C. C D. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】用化学符号表示:
(1)两个氦原子 _____
(2)3个氯分子 _____
(3)硝酸根离子 _____
(4)+2价的镁元素 _____
(5)硫酸铝 _____
(6)氯化亚铁 _____
相关试题

