【题目】早在春秋战国时期,我国就开始生产和使用铁器。工业炼铁把铁矿石和焦炭、石灰石一起加入高炉,在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来。
一氧化碳还原氧化铁的化学方程式为: 。其中,石灰石起的作用是 。
(一)甲组同学在学习炼铁的相关内容时,对炼铁时还原剂的选择进行了如下探究。
【提出问题】
单质碳也具有还原性,碳还原氧化铁的化学方程式为 。为什么工业上不用焦炭作为还原剂直接还原铁矿石?
【猜想与假设】
焦炭和铁矿石都是固体,接触面积小,反应不易完全。
【进行实验】
①称取两份相同质量的氧化铁粉末。一份与足量的碳粉均匀混合放入图1装置A的试管中;另一份放入图1装置B的玻璃管中。
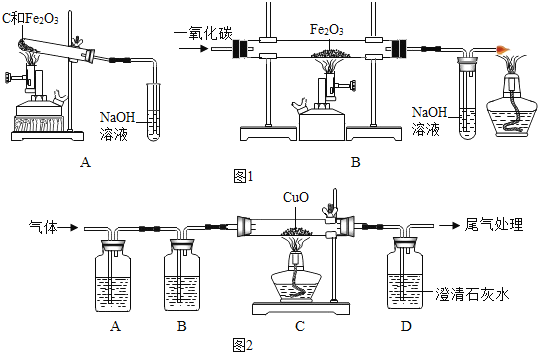
②图1装置A和B两组实验同时开始进行。在图1装置B的反应中,实验开始前应先 (选填“通CO”或“加热”); 实验结束后应继续通入CO直至冷却至室温,其原因是 。
【实验现象】
当图1装置B的玻璃管中固体完全由 时(选填“红色变为黑色”或“黑色变为红色”),图1装置A的试管中仍有 。
【解释与结论】
焦炭和铁矿石都是固体,接触面积小,反应确实不易完全,这可能是工业上不用焦炭作为还原剂直接还原铁矿石的一个原因。
【完善实验】
联想到单质碳的一些化学性质,甲同学认为在碳还原氧化铁的反应中可能还会有CO产生。为了证明碳还原氧化铁所得的气体中含有CO和CO2,将该气体通过图2的检验装置。图2A装置中的试剂是(写名称,下同) ,图2B装置中的试剂是氢氧化钠溶液,用以吸收二氧化碳(2NaOH+CO2═Na2CO3+H2O );证明原混合气体中CO2存在的化学方程式 ;证明原混合气体中CO存在的实验现象是 ;经过检验,证实碳还原氧化铁所得的气体中确实含有CO和CO2。
(二)精还原铁粉是一种重要的化工原料,某兴趣小组对其进行下列研究:
【物质制备】
利用绿矾制备精还原铁粉的工艺流程如下:
![]()
粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为
FexOy+yH2![]() xFe+yH2O,Fe3C+2H2
xFe+yH2O,Fe3C+2H2![]() 3Fe+CH4。
3Fe+CH4。
【含量测定】
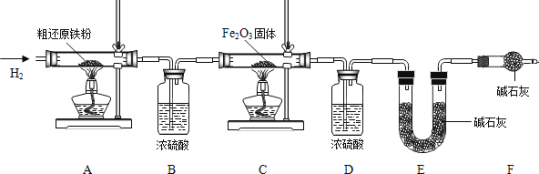
为得到精还原铁粉并测定粗还原铁粉中氧和碳元素的质量分数,按图装置进行实验。
已知3CH4+4Fe2O3![]() 3CO2+6H2O+8Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。
3CO2+6H2O+8Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。
(1)主要实验步骤如下:
①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;
②缓缓通入纯净干燥的H2;
③点燃酒精灯, (填“先点A处,后点C处”或“先点C处,后点A处”);
④分别熄灭A处、C处酒精灯;
⑤再缓缓通入少量H2;
⑥再次称量必要装置的质量
(2)步骤②的目的是 ,验证该步骤目的达到的实验方法是 ;
(3)若缺少装置D,则所测氧元素的质量分数将 (填“偏大”,“偏小”或“不变”)。
(4)粗还原铁粉样品的质量为15.000g,装置B、E分别增重0.270g和0.330g,则计算样品出中碳、氧元素的质量分数分别是 。(列出计算过程,2分)
参考答案:
【答案】3CO+Fe2O3![]() 2Fe+3CO2;将矿石中的二氧化硅等杂质转变为炉渣而除去的。
2Fe+3CO2;将矿石中的二氧化硅等杂质转变为炉渣而除去的。
(一)【提出问题】3C+2Fe2O3高温4Fe+3CO2↑
【进行实验】②通CO;防止液体倒吸进入硬质粗玻璃管,造成炸裂且防止高温下铁又被进入的空气氧化。
【实验现象】红色变为黑色;红色物质。
【完善实验】澄清石灰水;Ca(OH)2+CO2=CaCO3↓+H2O;黑色粉末变成红色。
(二)(1)③先点C处,后点A处。(2)排尽空气,防止爆炸;收集尾气,进行验纯。
(3)不变(4)w(C)=0.6%;w(O)=1.6%。
【解析】
试题分析∶根据所学知识和题中信息知,工业炼铁把铁矿石和焦炭、石灰石一起加入高炉,在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来。一氧化碳还原氧化铁的化学方程式为:3CO+Fe2O3高温2Fe+3CO2;其中,石灰石起的作用是将矿石中的二氧化硅等杂质转变为炉渣而除去的。(一)甲组同学在学习炼铁的相关内容时,对炼铁时还原剂的选择进行了如下探究。【提出问题】单质碳也具有还原性,碳还原氧化铁的化学方程式为3C+2Fe2O3高温4Fe+3CO2↑。为什么工业上不用焦炭作为还原剂直接还原铁矿石?【猜想与假设】焦炭和铁矿石都是固体,接触面积小,反应不易完全。【进行实验】①称取两份相同质量的氧化铁粉末。一份与足量的碳粉均匀混合放入图1装置A的试管中;另一份放入图1装置B的玻璃管中。②图1装置A和B两组实验同时开始进行。在图1装置B的反应中,实验开始前应先通CO;实验结束后应继续通入CO直至冷却至室温,其原因是防止液体倒吸进入硬质粗玻璃管,造成炸裂且防止高温下铁又被进入的空气氧化。【实验现象】当图1装置B的玻璃管中固体完全由红色变为黑色时;图1装置A的试管中仍有红色物质。【解释与结论】焦炭和铁矿石都是固体,接触面积小,反应确实不易完全,这可能是工业上不用焦炭作为还原剂直接还原铁矿石的一个原因。【完善实验】甲同学认为在碳还原氧化铁的反应中可能还会有CO产生。为了证明碳还原氧化铁所得的气体中含有CO和CO2,将该气体通过图2的检验装置。图2A装置中的试剂是澄清石灰水;图2B装置中的试剂是氢氧化钠溶液,用以吸收二氧化碳(2NaOH+CO2═Na2CO3+H2O );证明原混合气体中CO2存在的化学方程式是Ca(OH﹚2+CO2=CaCO3↓+H2O;证明原混合气体中CO存在的实验现象是黑色粉末变成红色。经过检验,证实碳还原氧化铁所得的气体中确实含有CO和CO2。(二)精还原铁粉是一种重要的化工原料,某兴趣小组对其进行下列研究:【物质制备】利用绿矾制备精还原铁粉的工艺流程如下:粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为FexOy+yH2高温xFe+yH2O,Fe3C+2H2高温3Fe+CH4。【含量测定】为得到精还原铁粉并测定粗还原铁粉中氧和碳元素的质量分数,按图装置进行实验。已知3CH4+4Fe2O3高温3CO2+6H2O+8Fe(1)主要实验步骤如下:①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;②缓缓通入纯净干燥的H2;③点燃酒精灯,先点C处,后点A处。④分别熄灭A处、C处酒精灯;⑤再缓缓通入少量H2;⑥再次称量必要装置的质量。(2)步骤②的目的是排尽空气,防止爆炸;验证该步骤目的达到的实验方法是收集尾气,进行验纯。(3)若缺少装置D,则所测氧元素的质量分数将不变。(4)粗还原铁粉样品的质量为15.000g,装置B、E分别增重0.270g和0.330g,则计算样品出中碳、氧元素的质量分数分别是∶0.330g×﹙12/44×100%﹚/15.0g×100%=0.6%;0.270g×﹙16/18×100%﹚/15.0g×100%=1.6%。
考点∶考查实验探究的基本思路和方法。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在宏观、微观和符号之间建立联系是化学学科的特点。
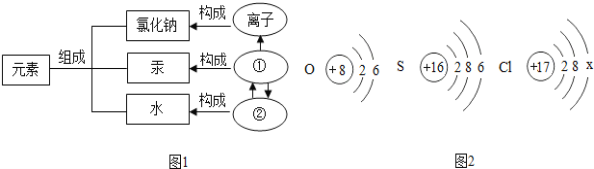
(1)物质的组成及构成关系如图1所示,图中①表示的是 ,②表示的是 。
(2)图2是氧、硫、氯三种元素的原子结构示意图。
①氯原子的结构示意图中x的数值是 ,达到稳定结构易 (填“得”或“失”)电子。
②氧和硫两种元素的化学性质具有相似性的原因是它们原子的 相同。
③氧和氯两种元素最本质的区别是它们原子中的 不同。
(3)甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下表所示:
物质
甲烷
氧气
水
二氧化碳
一氧化碳
反应前质量/g
3.2
11.2
0
0
0
反应后质量/g
0
0
7.2
4.4
a
则a的值为 ,根据表格中数据,请完成相关的化学方程式4CH4+7O2= 。(反应条件略)
-
科目: 来源: 题型:
查看答案和解析>>【题目】用化学用语表示:
(1)①2个氖原子 ;②水瓶内壁镀的金属是 ;
③海洋中含量最多的阳离子 ;④缺少 元素会得侏儒症。
(2)选用符合要求的物质的字母填空:
A氯化钠 B干冰 C氧气 D氮气 E石墨
①常用作电池电极的是 ;
②常用作食品保护气的是 ;
③常用作厨房调味剂的是 ;
④常用于人工降雨的是 。
(3)写出下列反应的化学方程式:
①曾青得铁则化为铜 ;
②铁丝在氧气中燃烧 ;
③铝和稀硫酸的反应 ;
④硅是信息技术的关键材料。高温下氢气与四氯化硅(SiCl4)反应可制得高纯度的硅,同时生成氯化氢,该反应的化学方程式为 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】同学们利用如图所示装置进行气体的制备实验(A~F为装置编号)。
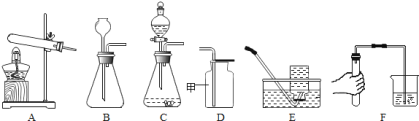
(1)写出图D装置中甲仪器的名称 。
(2)用A装置加热氯酸钾和二氧化锰的混合物制取氧气,化学方程式为 ,其中二氧化锰起 作用;收集氧气可以选择 (填装置编号)。
(3)实验室制取H2通常选择下列药品中的 (填药品序号)。
a、浓盐酸 b.锌粒 c.铁块 d.稀硫酸
实验室制取氢气应选择的发生和收集装置的组合可以是 (填装置编号)。
(4)常温下,可用固体硫化亚铁(FeS)和稀硫酸反应制取硫化氢(H2S)气体,若要控制滴加液体的速率,可选择的发生装置是 (填装置编号)。
(5)制取气体前应先检查装置的气密性,若按F图所示操作,结果在导管口未看到气泡,其可能原因与下列因素有关的是 (填序号)。
a.将烧杯换成水槽
b.导管深入水中位置过深,气体无法逸出
c.将水换成冰水
d.先用手捂住试管壁,再将导管另一端插入水中
-
科目: 来源: 题型:
查看答案和解析>>【题目】高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
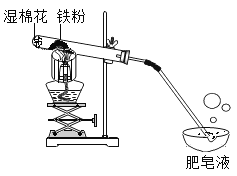
(1)试管尾部放一团湿棉花的目的是 。
(2)探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是 。写出该反应的化学方程式 。
(3)探究试管中剩余固体成分是什么?
【查阅资料】
常见铁的氧化物
FeO
Fe2O3
Fe3O4
颜色、状态
黑色粉末
红棕色粉末
黑色晶体
能否被磁铁吸引
否
否
能
与盐酸反应
FeCl2+H2O
FeCl3+H2O
FeCl2+FeCl3+H2O
【初步验证】
试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】
猜想一:剩余固体是 ;猜想二:剩余固体是 。
【实验探究】
实验操作
实验现象及结论
【实验结论】铁和水蒸气反应的化学方程式为 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】掌握化学用语是学好化学的关键。下列化学用语与所表述的意义相符合的是( )
A. H2O —— 1个水分子 B.
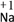 —— 1个钠离子
—— 1个钠离子C. 3Fe3+ ——3个铁原子 D. 2H —— 2个氢元素
-
科目: 来源: 题型:
查看答案和解析>>【题目】食醋是厨房中的一种调味品,其中含有少量醋酸下列有关醋酸的说法不正确的是( )
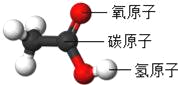
A. 醋酸分子是由碳、氢、氧三种原子构成的
B. 醋酸中碳元素的质量分数为40%
C. 醋酸是由碳、氢、氧三种元素构成的
D. 每个醋酸分子中有8个原子核
相关试题

