【题目】如下图是一个“珠漏“,A首先漏下,A﹣F分别代表6种初中化学的常见物质:氧气、木炭、碳的某种氧化物、铁、氧化铁、硝酸银。
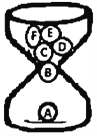
珠子漏下的规律:
①相对分子质量最大的第一个漏下;
②先漏下的珠子带动下一颗相互间能反应的珠子漏下,从而实现按A﹣B﹣C﹣D﹣E﹣F的顺序漏下。
(1)请写出以下物质的化学式A_____E_____。
(2)“碳的某种氧化物”是_____,它是A~F中的_____。
(3)请写出A与B反应的化学方程式_____。
参考答案:
【答案】 AgNO3 Fe2O3 CO D 2AgNO3+Fe=Fe(NO3)2+2Ag
【解析】本题是框图型推断题。在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。
(1)A首先漏下,A﹣F分别代表6种初中化学的常见物质:氧气、木炭、碳的某种氧化物、铁、氧化铁、硝酸银,珠子漏下的规律:①相对分子质量最大的第一个漏下;氧气的相对分子质量是32,木炭的相对原子质量是12,一氧化碳的相对分子质量是28,二氧化碳的相对分子质量是44,铁的相对原子质量是56,氧化铁的相对分子质量是160,硝酸银的相对分子质量是170,所以A是硝酸银,②先漏下的珠子带动下一颗相互间能反应的珠子漏下,从而实现按A﹣B﹣C﹣D﹣E﹣F的顺序漏下,硝酸银会与铁反应,所以B是铁,铁会与氧气反应,所以C是氧气,氧气会与一氧化碳反应,所以D是一氧化碳,一氧化碳会与氧化铁反应,所以E是氧化铁,F是木炭,经过验证,推导正确,所以A是AgNO3,E是Fe2O3;
(2)“碳的某种氧化物”是:CO,它是A~F中的D;
(3)A与B的反应是铁和硝酸银反应生成硝酸亚铁和银,化学方程式为:2AgNO3+Fe=Fe(NO3)2+2Ag。
-
科目: 来源: 题型:
查看答案和解析>>【题目】变废为宝好处多
(1)秸秆再生利用
①我市一企业将秸秆经系列处理后,开发出可降解秸秆塑料,优点为________;
A.节约能源 B.减少白色污染 C.减少因焚烧秸秆产生的PM2.5
②秸秆可制沼气,沼气燃烧的化学方程式为_________;
(2)草木灰中可溶物含K2CO3、K2SO4和 KCl,下左图是这三种物质的溶解度曲线。回答:
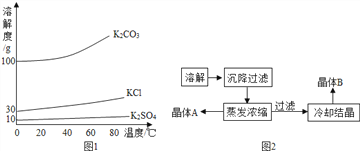
①农业上,草木灰可作_______肥,_________(填“能”或“不能”)和NH4Cl混用;
②KCl 是________溶(填“易”、“可”、“微”、“难”)物质;
③提取草木灰中K2CO3 的步骤如上右图所示:则晶体 A 主要是________和_________(填 化学式)。
(3)废旧电路板(PCB)回收利用
①PCB 中含:a.Cu、Ag、Pb(铅)、Fe 等;b.塑料聚合物;c.陶瓷和玻璃纤维。
其中属于无机材料的是________(填字母序号,下同),属于合成材料的是________;
②用溶蚀法回收 PCB 中的 Cu,原理如下:
a.溶蚀:将 Cu 溶解在CuCl2溶液中,生成 CuCl;
b.再生:将O2鼓入 CuCl 溶液,加入稀 HCl,生成CuCl2和H2O,反应的化学方程式为__________;
c.置换:在再生液中加入铁粉,得到 Cu,反应的化学方程式为_______,属于_______反
应(填基本反应类型)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】结合如图,回答有关问题:
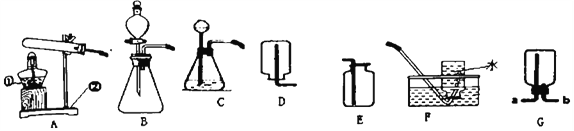
(1)写出编号所指仪器的名称:①_____,②_____;
(2)甲同学用氯酸钾和二氧化锰固体制取并收集比较纯净的氧气,选择上述装置中的_____(填字母)
进行组装,化学反应方程式为_____。
(3)乙同学在实验中误把高锰酸钾当成二氧化锰加入氯酸钾中进行实验,通过观察对比_____,他认
定氯酸钾的分解速率明显比甲同学的快,原因是_____。
(4)在实验室制取二氧化碳,若没有块状大理石,只有粉末状碳酸钠,为了控制反应速度,可选上述装
置中的_____(填字母)作为发生装置,收集二氧化碳气体若选择G装置,则由_____端通入气体,
检验是否收集满二氧化碳的方法为_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】小明用蜡烛进行了下列活动。
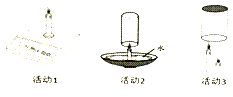
(1)活动1:点燃蜡烛后,电子秤示数逐渐减小。蜡烛减小的质量_____(填“大于”“等于”或“小于”)燃烧后生成物的总质量。
(2)活动2:用玻璃杯扣住燃烧的蜡烛,并使杯口始终浸没在水中。下列说法正确的是_____(填序号)
A.可观察到蜡烛熄灭 B.最终杯中液面高于碗中液面
C.该方法能准确侧测定空气中氧气的含量 D.蜡烛不会熄灭。
(3)活动3:把玻璃杯扣住高低两只燃烧的蜡烛,现象是_____(填序号)
A.两只蜡烛同时熄灭 B.高的蜡烛先熄灭 C.低的蜡烛先熄灭 D.蜡烛不会熄灭
产生该现象的原因是_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。CuCl 制备流程如下:
已知:CuCl 难溶于水和乙醇,在潮湿空气中易变质。
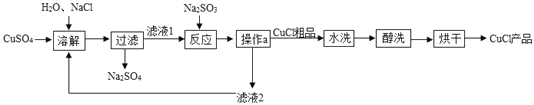
(1)“反应”中发生的化学变化是2CuCl2+ Na2SO3= 2CuCl↓+ 2NaCl + SO3,产生的SO3迅速与水化合生成一种酸,该反应的化学方程式为________。
(2)“操作 a”的名称是_________。本流程中可以循环利用的物质(水除外)是_________填化学式)。
(3)可用“水洗”的原因是_________,检验水洗是否干净可选用试剂为________(填化 学式)溶液。“醇洗”的目的是_________。
(4)160g CuSO4与足量 NaCl 经上述制备流程,可生成的 CuCl 最多是_________g。
-
科目: 来源: 题型:
查看答案和解析>>【题目】蛇纹石矿可以看做MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如图所示:
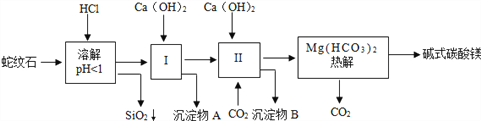
查阅资料:A.几种物质沉淀和溶解时的 pH 如下表
氢氧化物
溶液 pH
开始沉淀
沉淀完全
沉淀开始溶解
沉淀完全溶解
Fe(OH)3
2.3
3.4
沉淀不溶
沉淀不溶
Al(OH)3
3.3
5.2
7.8
12.8
Mg(OH)2
8.6
11.1
沉淀不溶
沉淀不溶
B.难溶性碱加热会生成两种氧化物,各元素化合价都不变。
探究一:制取碱式碳酸镁
(1)在操作Ⅰ中发生的中和反应是________(用化学方程式表示)。
(2)进行操作Ⅰ时,需控制溶液pH=6~7,Ca(OH)2不能过量。若Ca(OH)2过量, 可能导致_______溶解、________沉淀。
(3)从沉淀混合物 A 中提取红色氧化物作颜料,先向沉淀物 A 中加入________(填物质的化学式),然后_________、________、灼烧(依次填写实验操作名称)。
(4)物质循环使用,能节约资源。上述实验中,可以循环使用的物质是______。
探究二:确定产品碱式碳酸镁(mMgCO3·nMg(OH)2·xH2O)的组成,组装如图 1 仪器:
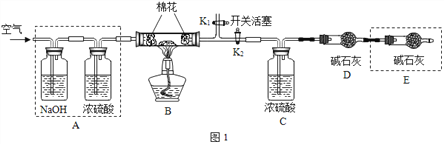
实验测得:硬质玻璃管中剩余的固体质量为 2.0g,C 处浓H2SO4增重 0.9g,D 处碱石灰增 重 1.76g。
(1)在装好试剂后,加热前应进行的操作是_______;
(2)A 框中装置的作用是________;
(3)通过计算写出碱式碳酸镁的化学式__________。(请写出计算过程)
【交流与反思】
(1)若将 E 框中的装置去掉,对实验结果的影响是 m
值________,x 值_______ (填“偏 大”、“偏小”或“不变”) (2)已知碳酸镁和氢氧化镁在不同的温度下受热易分解为氧化物。为精确测定此碱式碳酸镁受热分解过程中时间与剩余固体质量的关系,结合以上数据,作出图 2 坐标系,试回答。
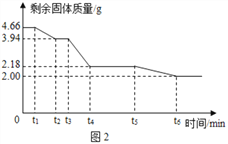
①t4~t5时间段固体的化学式为__________;
②t5~t6时间段发生反应的方程式为___________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列各组变化中,每个转化在一定条件下均能一步实现的是
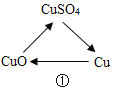
A.①④ B.①②④ C.①③④ D.①②③④
相关试题

