【题目】乳酸亚铁片可用于治疗缺铁性贫血.下图为乳酸亚铁片说明书上的部分文字.

请仔细阅读后回答以下问题:
(1)乳酸亚铁的相对分子质量为_____,碳、铁两种元素的质量比为_____。
(2)144g乳酸亚铁中铁元素的质量为_____g。
(3)某人每天分二次服药,一次最多服用_____片,服药时不能喝茶的原因是_____。
参考答案:
【答案】288 72:56或9:7 28 3 生成鞣质沉淀失效
【解析】
(1)由乳酸亚铁的化学式,乳酸亚铁的相对分子质量为:12×6+1×10+56+16×6+3×18=288;C、Fe元素的质量比为(12×6):56=9:7;
(2)144g乳酸亚铁中铁元素的质量为144g×![]() ×100%=28g;
×100%=28g;
(3)每片0.1g,成人一天用量最多为0.6g,则每天服用![]() =6片,每天分二次服药,则每次服用3片,根据注意事项可知,服时忌茶,以免生成鞣质沉淀,所以服药时不能喝茶。
=6片,每天分二次服药,则每次服用3片,根据注意事项可知,服时忌茶,以免生成鞣质沉淀,所以服药时不能喝茶。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图为生活中常见“暖贴”的部分标签。暖贴可以贴于身体的某个部位,自行发热,用于取暖或热敷。

(1)任意写出暖贴中两种主要成分的化学式_____、_____(铁粉、水、氯化钠、活性炭中任写两个)。
(2)暖贴中活性炭具有_____作用,使用时空气进入暖贴,空气中的氧气与暖贴中的_____发生反应而使暖贴放热。
(3)使用后,发现暖贴内有的物质变为红色,该红色固体主要成分的化学式为_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】A~H表示初中化学常见物质,它们之间转化关系如图所示(部分生成物已略去)
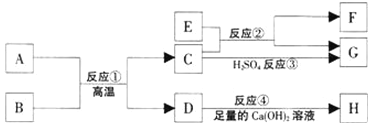
其中A为红棕色固体,反应①为冶金工业的重要反应,且B、D组成元素相同,C、F为金属单质,其它物质为化合物,其中F为紫红色,H为白色沉淀。
请按要求填空:
(1)写出下列物质的化学式:A D E
(2)①~④的反应中属于置换反应的是 (填序号)。
(3)反应①的化学方程式为 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(6分)某化工厂排放的废液中含有大量的硫酸锌和硫酸铜,兴趣小组根据所学知识设计了一个方案来回收金属铜并得到硫酸锌晶体,主要过程如图所示,请回答下列问题:
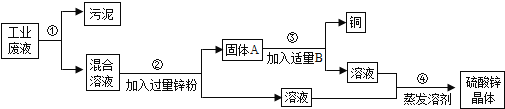
(1)步骤②中分离物质的方法是 。
(2)步骤②中发生反应的化学方程式为 ,基本类型为 反应。
(3)固体A的成分是 。
(4)步骤③中加入的B物质是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】通过一学期的化学学习,你已经掌握了实验室制取气体的一些规律,以下是老师提供的一些实验装置,请你结合如图回答问题:
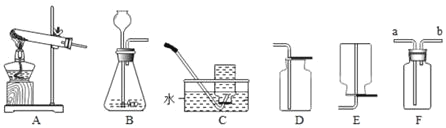
(1)写出实验室用氯酸钾和二氧化锰的混合物制备氧气的化学方程式_____,反应后二氧化锰的质量分数_____(填“增大”、“减少”或“不变”),实验完毕后发现试管已经炸裂,请分析炸裂原因:_____(答一种情况即可)。
(2)实验室用B装置可以制取的气体是_____,写出该反应的化学方程式_____。
(3)已知氨气是一种密度比空气小且极易溶于水的气体,其实验室制法的一种原理是氯化铵和氢氧化钠溶液在加热的情况下生成氯化钠、水、氨气,据此设计出的发生装置可以是_____,收集装置可以是_____(填“C”、“D”或“E”)。若用F装置进行密封收集氨气,气流应从_____端(“a”或“b”)流入集气瓶。
-
科目: 来源: 题型:
查看答案和解析>>【题目】为了探究木炭在高温条件下还原氧化铜所生成的气体产物是什么,课外兴趣小组进行了如下实验探究:
【提出问题】生成的气体产物是什么?
①【实验猜想】猜想1:只有CO2;
猜想2:只有________________(填化学式);
猜想3:含有CO和CO2。
若猜想1成立,木炭与氧化铜反应的化学方程式为____________________。
②【实验探究】基于猜想3,根据CO和CO2的性质,兴趣小组同学设计了下图装置进行探究。
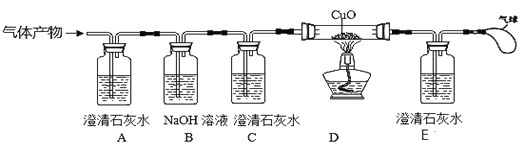
(提示:NaOH溶液能吸收CO2)
(Ⅰ)观察到A装置中的澄清石灰水变浑浊,证明气体产物中有CO2,A装置中的化学方程式是
___________________。
(Ⅱ)有两种实验现象都能分别证明气体产物中含有CO。
现象1:C装置中澄清石灰水___________________,E装置中出现浑浊的现象。
现象2:D装置中出现________________________________的现象。
(Ⅲ)C装置的作用是_________________________________。
(Ⅳ)图中气球的作用是____________________________。
【实验结论】通过实验探究,猜想3成立。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某中学化学兴趣小组通过实验测定某大理石中碳酸钙的质量分数,将盛有20.0g该样品的烧杯放在电子秤上,倒入100.0g稀盐酸(假设大理石样品中的杂质不与稀盐酸反应,也不溶于水),使该样品恰好完全反应,实验过程中的有关数据如下表所示:
时间/s
0
20
40
60
80
100
烧杯与所盛物质质量/g
174.0
171.0
169.0
168.0
167.4
167.4
计算:
(1)生成二氧化碳的质量;
(2)该大理石中碳酸钙的质量分数;
(3)反应完成所得溶液中溶质的质量分数(精确到0.1%)
相关试题

