【题目】甲、乙、丙是初中化学常见物质。这些物质之间的转化关系如下图所示。
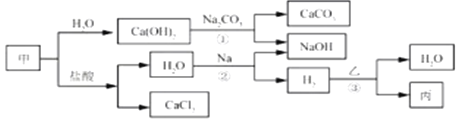
根据以上信息,请回答下列问题。
(1)写出甲的化学式__________。
(2)写出反应①的化学方程式_______________。
(3)写出反应②的化学方程式_______________。该反应属于_____反应(填基本反应类型)。
(4)反应③在一定温度下进行,若乙为Fe2O3,则丙为Fe;若丙为Cu,则乙为_______(填化学式)。
(5)请完成下列表格,证明Fe的金属活动性比Cu的强。
实验方案 | 实验现象 |
将铁片浸入_______(填化学式)溶液中 | 铁片表明析出______固体 |
参考答案:
【答案】(1)CaO;(2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)2Na+2H2O=2NaOH+H2↑;置换;(4)CuO;(5)CuSO4(或CuCl2);红色。
【解析】(1)根据转化关系,甲能与水反应生成氢氧化钙,还能与盐酸反应生成氯化钙和水,故甲是氧化钙,氧化钙表示为CaO;(2)氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式表示为Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;(3)根据转化关系,钠与水反应生成氢氧化钠和氢气,反应的化学方程式表示为2Na+2H2O=2NaOH+H2↑,该反应的反应物是一种单质和一种化合物,生成物也是一种单质和一种化合物,属置换反应;(4)在加热的条件下,氢气还原氧化铜生成铜和水,即乙是氧化铜,氧化铜表示为CuO;(5)根据金属活动性顺序的应用:位于前面的金属能把位于后面的金属从化合物的溶液中置换出来,故要证明铁的活动性比铜强,可将铁片浸入到硫酸铜溶液中,观察到铁片的表面出现一层红色的固体,说明铁的活动性比铜强。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列做法不符合“节能减排”的是( )
A.加大对核能的利用 B.在田野里焚烧秸秆
C.用水后,随手关闭水龙头 D.推广使用以电池提供动力的客车
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列食物中富含蛋白质的是( )
A.煮鸡蛋 B.小米粥 C.凉拌黄瓜 D.白面馒头
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列关于一氧化碳和二氧化碳的说法正确的是
A.密度都比空气大 B.都可以用碳和氧气反应得到
C.都有还原性 D.都能和澄清石灰水发生反应
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列溶液在空气中敞口放置后,溶液质量因发生化学反应而减小的是
A.石灰水 B.浓硫酸 C.浓盐酸 D.烧碱溶液
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列各物质按照单质、氧化物、混合物的顺序排列的是
A.冰、干冰、食醋 B.氮气、氧气、空气
C.水银、水、矿泉水 D.金、氯酸钾、石油
-
科目: 来源: 题型:
查看答案和解析>>【题目】我国矿物种类齐全,储量丰富。工业上从从含有金属元素的矿石中提炼金属。其中赤铁矿是炼铁的主要原料。请回答下列问题:
I.铁制品广泛应用于生产、生活中。
(1)下列不属于铁合金的是_____________(选填字母)。
A.Fe(OH)3 B.生铁 C.不锈钢
(2)铁钉生锈,属于_____变化(选填“物理”“化学”):右图是探究铁钉在不同条件下发生生锈的实验,其中铁锈蚀最快的是______(选填字母)。
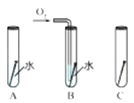
II.赤铁矿(主要成分为Fe2O3)可用于生产催化剂。
(3)在Fe2O3中,氧元素的质量分数为_____________。
(4)赤铁矿经提纯后得到的纯净Fe2O3可用于生产某种工业催化剂(主要成分为FeO和Fe2O3),其反应原理为:2 Fe2O3+C
 4FeO+CO2↑。现将焦炭和过量的Fe2O3混合均匀,按上述原理充分反应,右图为固体混合物的质量随反应时间的变化曲线。
4FeO+CO2↑。现将焦炭和过量的Fe2O3混合均匀,按上述原理充分反应,右图为固体混合物的质量随反应时间的变化曲线。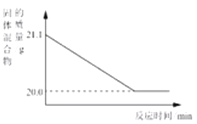
①由图可知:生成CO2气体的质量为_____g。
②计算反应后固体混合物中FeO的质量分数(请根据化学方程式写出完整的计算步骤)。
相关试题

