【题目】碳酸钠从溶液里结晶析出时,晶体里总是结合着一定数目的水分子(结晶水),随着温度的变化可分别得到Na2CO3·10H2O、Na2CO3·7H2O和Na2CO3·H2O三种晶体。分析碳酸钠溶解度随温度变化曲线(见右图)得到的下列说法,正确的是( )

A.随温度升高,碳酸钠的溶解度逐渐增大
B.碳酸钠从溶液结晶析出时,没有发生化学反应
C.碳酸钠溶液在高温条件下晶体,析出的晶体是Na2CO3·H2O
D.碳酸钠溶液在低温条件下结晶,析出的晶体主要是Na2CO3·7H2O
参考答案:
【答案】C
【解析】
试题分析:A.根据图示可知:在温度为35℃时,碳酸钠的溶解度达到了最大。当温度再升高时其溶解度反而有所下降。此项不正确。B.根据题意可知:碳酸钠从溶液里结晶析出时,晶体里总是结合着一定数目的水分子(结晶水)。所以碳酸钠从溶液结晶析出时,发生了化学反应。此项不正确。C.根据图示可知:在温度大于35℃时,碳酸钠溶液中析出的晶体是Na2CO3·H2O。此项正确。D. 根据图示可知:碳酸钠溶液在低温条件下结晶,析出的晶体主要是Na2CO3·10H2O。此项不正确。所以应选C项。
-
科目: 来源: 题型:
查看答案和解析>>【题目】现有四种物质,选择相应物质的字母填空:
A、活性炭 B、钛合金 C、石墨 D、不锈钢
(1)可用于吸附冰箱内异味的是 。
(2)可用于制造人造骨的是 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】清明时节,同学们相约外出踏青野炊.请用化学知识分析小丽问题:
(1)野炊食谱人表所示:

从合理膳食角度来看,你认为食谱中还应添加 (填字母);
A.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉
(2)野炊后同学们准备将垃圾分类处理,其中属于不可回收垃圾的是 (填字母);
A.废纸 B.果皮 C.易拉罐 D.塑料桶
(3)小滨用洗涤剂洗去手上的油迹,是利用了洗涤剂的 作用;
(4)大家在田边看到农民正在使用化肥NH4NO3,于是联想到NH4NO3不能和熟石灰混合施用,请用化学方程式解释原因 .
-
科目: 来源: 题型:
查看答案和解析>>【题目】某实验小组在探究金属的化学性质的时,得到金属与酸反应制取氢气的质量关系(见下图)。请根据图像信息判断,下列说法正确的是( )
A.四种金属与酸反应的速率:Al > Mg > Fe > Zn
B.四种金属的活动性顺序:Mg > Al > Zn > Fe
C.同质量的四种金属与足量酸反应得到氢气的质量:Al > Mg > Fe > Zn
D.Al 、Mg 、Fe、 Zn四种金属与酸反应得到氢气的质量比:
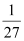 :
: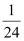 :
: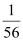 :
: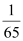
-
科目: 来源: 题型:
查看答案和解析>>【题目】(4分)济宁是山东省重要的煤炭能源基地,然而矿区废水中Fe2+、Cu2+、Zn2+等严重影响着当地水质。某污水处理厂采用下图工艺(见下图)净化这种酸性废水并回收Fe2+、Cu2+、Zn2+三种离子。请读识流程图并回答:

(1)矿区废水经氧化池后再进入沉淀池Ⅰ,目的是____________________________________;
(2)利用氢氧化钠调节沉淀池Ⅰ、沉淀池Ⅱ和沉淀池Ⅲ的pH,目的是_____________________;
(3)出水前,中和池中加入硫酸的作用___________________;
(4)若矿区废水中主要含有硫酸盐,请写出沉淀池Ⅲ中发生反应的化学方程式__________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】有一瓶密封保存长期放置的氯化钠溶液,下列说法正确的是( )
A.瓶口附近的溶液较稀
B.瓶底附近的溶液较浓
C.瓶底会有固体析出
D.瓶内各部分溶液的浓度都相同
-
科目: 来源: 题型:
查看答案和解析>>【题目】(2分)合理膳食可促进我们的身体健康。一碟青菜搭一个馒头、一个汉堡配一份薯条、一袋方
便面加一根火腿肠······这些“经典”搭配,是很多人餐桌上的常客,也是年青人简单生活的表现这样的饮食搭配健康吗?请以一餐“一碟青菜搭一个馒头”的食谱为例,参阅右图和自己的生活经历回答下面问题:
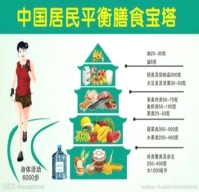
(1)“一碟青菜搭一个馒头”饮食搭配主要补充的营养成分是__________________;
(2)从均衡膳食角度考虑,应对该搭配做哪些调______________________________________________________。
相关试题

