【题目】金属是生活中常用的一类物质.
(1)铝能制成很薄的铝箔用于包装,这是利用铝的性.
(2)铁丝在氧气中燃烧的实验,集气瓶底要留有少量的水,目的是 , 请写出铁丝在氧气中燃烧的化学方程式 . 铁丝还能在氯气中燃烧:2Fe+3Cl2 ![]() 2X,方程式中X的化学式为 .
2X,方程式中X的化学式为 .
(3)硫酸亚铁溶液中含有少量硫酸铜,可加入铁粉除去杂质,请写出该反应化学方程式: .
参考答案:
【答案】
(1)延展
(2)防止生成的熔化物溅落炸裂集气瓶,3Fe+2O2 ![]() Fe3O4,FeCl3
Fe3O4,FeCl3
(3)Fe+CuSO4═FeSO4+Cu
【解析】解:(1)铝能制成很薄的铝箔用于包装,这是利用铝的延展性.
故填:延展.(2)铁丝在氧气中燃烧的实验,集气瓶底要留有少量的水,目的是防止生成的熔化物溅落炸裂集气瓶;
铁丝在氧气中燃烧的化学方程式为:3Fe+2O2 ![]() Fe3O4;
Fe3O4;
铁丝在氯气中燃烧的化学方程式为:2Fe+3Cl2 ![]() 2FeCl3.
2FeCl3.
故填:防止生成的熔化物溅落炸裂集气瓶; 3Fe+2O2 ![]() Fe3O4;FeCl3.(3)铁和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu.
Fe3O4;FeCl3.(3)铁和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu.
故填:Fe+CuSO4═FeSO4+Cu.
【考点精析】掌握金属的物理性质及用途和金属材料的选择依据是解答本题的根本,需要知道金属的物理性质: (1)常温下一般为固态(汞为液态),有金属光泽.(2)大多数呈银白色(铜为紫红色,金为黄色)(3)有良好的导热性、导电性、延展性;黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属.
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列各组物质中,前者属于单质、后者属于混合物的是( )
A.氮气、蒸馏水
B.高锰酸钾、食盐水
C.氢气、稀有气体
D.二氧化碳、洁净的空气
-
科目: 来源: 题型:
查看答案和解析>>【题目】水是重要的自然资源,我们应该了解有关水的一些知识.
(1)硬水给生活和生产带来很多麻烦,生活中可用区别硬水和软水,常用的方法来降低水的硬度.
(2)如图为电解水的装置,试管2中的气体为 , 验证该气体的方法是 . (操作、现象、结论)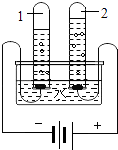
(3)请写出电解水反应的化学反应方程式 .
(4)有的化学反应中,水也作为反应物参加反应.过氧化钙(CaO2)常用于鱼池供氧剂,它能与水反应,生成氧气和氢氧化钙,该反应的化学方程式为 . -
科目: 来源: 题型:
查看答案和解析>>【题目】(1)实验室制氧气的两种方法如下:
方法一:2H2O2
 2H2O+ O2↑ 方法二:2KMnO4
2H2O+ O2↑ 方法二:2KMnO4  K2MnO4 + MnO2 + O2↑
K2MnO4 + MnO2 + O2↑ 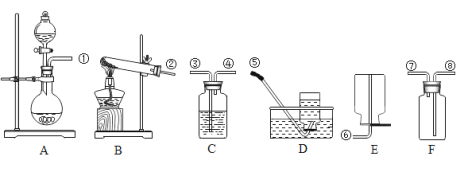
Ⅰ.用方法二制取氧气选择的反应装置为 ;
Ⅱ.设计A装置时使用分液漏斗的目的是 ;
Ⅲ.现用方法一制取并收集一瓶干燥的氧气,若用C装置干燥氧气,此干燥瓶中装有的物质为 ;在实验室中制取、干燥和收集氧气,请按气体流向,用导管的编号将装置连接好 。
(2)(7分)生石灰是一种传统的建筑材料,俗称“石灰”。工业上通过在石灰窑中煅烧石灰石制得“石灰”,其反应原理是:CaCO3
 CaO+CO2↑。兴趣小组的同学对某地刚出窑的“石灰”的成分进行探究。
CaO+CO2↑。兴趣小组的同学对某地刚出窑的“石灰”的成分进行探究。【提出问题】
刚出窑的“石灰”有那些成分?
【猜想】
I.只有氧化钙 II.只有碳酸钙 III.既有氧化钙也有碳酸钙
【实验探究】
⑴甲同学从样品中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物。甲同学据此认为试管中的固体为碳酸钙,即猜想II成立。乙同学认为上述实验不足以证明猜想II成立,其理由是
。
⑵乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生。乙同学据此认为试管中的固体只有氧化钙,即猜想I成立。丙同学认为乙的实验不足以证明猜想I成立,理由是
。
⑶丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想III成立,请完成他的实验报告。
实验步骤
实验现象
实验结论
①
②
猜想III成立
【思考】使用“石灰”的建筑工地上常有一个大的石灰池,使用“石灰”时,先将生石灰倒入池内水中,一段时间后,再取用其中的石灰浆使用。长期使用的石灰池内壁会逐渐增厚,其主要原因是 。
-
科目: 来源: 题型:
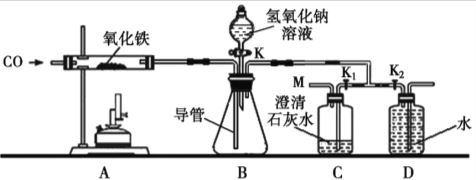
查看答案和解析>>【题目】利用下图装置在实验室模拟炼铁,并将得到的尾气中的一氧化碳和二氧化碳进行分离和收集。(提示:NaOH溶液可以吸收CO2气体。)
实验步骤如下:(说明:M去掉,导管口加个气球,我不会加,让印刷厂给加上的)
(1)检查装置气密性。
(2) 取一定质量的氧化铁加入硬质玻璃管中,其它容器中各加入适量试剂(如图所示)。
(3)关闭分液漏斗开关和K1,打开K2,通入CO气体一段时间,排除装置内的空气。
(4)打开分液漏斗开关K,将足量的氢氧化钠溶液放入锥形瓶中,使液面没过导管下端,关闭开关K。关闭K2,打开K1,继续通CO,点燃酒精喷灯,装置A的玻璃管中反应的化学方程是 。当装置C中的现象是 时,说明装置B中的反应是充分的,立即关闭K1,打开K2,装置D中收集到的气体是CO。
(5)一段时间后,停止加热,继续通CO气体至装置A的药品冷却。经称量氢氧化钠溶液增重2.64 g,此时生成Fe的质量是__________g(结果精确到0.1g)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】请用所学知识回答下列问题:
(1)举一个实例说明温度升高,分子运动速率加快_____;
(2)CO2和CO的化学性质不同,原因是_____;
(3)石蜡在空气中燃烧和在氧气中燃烧的现象不同,原因是_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】请回答下列与氧气有关的问题。
(1)排空气法收集氧气,检验气体是否集满的方法是_____;
(2)医疗上用纯度较高的氧气进行急救,是因为氧气能_____。
相关试题

