【题目】如图,A、B、C、D是四种粒子的结构示意图,E是铈元素在元素周期表中的信息。
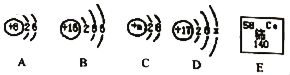
(1)若D为原子,则D中x的值为______;
(2)写出A、B两粒子对应的元素形成化合物的化学式______;
(3)根据E中提供的信息,可知铈原子的中子数为______;
(4)C粒子中,若m>10,则阳离子的符号可能为______(至少写一种)
参考答案:
【答案】7 SO2 82 Al3+、Mg2+、Na+
【解析】
元素周期表中,每种元素占据的空格中,左上角是原子序数,右上角是元素符号,中间是元素名称,下面是相对原子质量;
原子中,核电荷数=核内质子数=核外电子数=原子序数;
相对原子质量≈质子数+中子数,单位不是g;
化合物中元素化合价代数和为零;
一般情况下,最外层电子数小于4的,反应中容易失去电子,大于4的反应中容易得到电子,等于4的,既不容易得到电子,也不容易失去电子,因此最外层电子数相等的元素化学性质相似,最外层电子数是8的是一种稳定结构,第一层也是最外层时,达到2个电子也是一种稳定结构。
(1)若D为原子,则D中x的值为:17﹣2﹣8=7,
故填:7。
(2)写出A(氧元素)、B(硫元素)两粒子对应的元素形成化合物是二氧化硫,二氧化硫的化学式是SO2,
故填:SO2。
(3)根据E中提供的信息,可知铈原子的中子数为:140﹣58=82,
故填:82。
(4)C粒子中,若m>10,则阳离子的符号可能为带3个单位正电荷的铝离子,或带2个单位正电荷的镁离子,或带1个单位正电荷的钠离子。
故填:Al3+、Mg2+、Na+。
-
科目: 来源: 题型:
查看答案和解析>>【题目】氢气是理想的清洁、高能燃料。目前,液氢已应用于航天等领域。美囯普度大学研发出一种制备氢气的新工艺,基本流程如图所示。
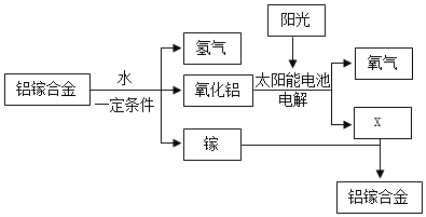
 资料:铝镓合金是金属铝和金属镓
资料:铝镓合金是金属铝和金属镓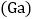 的混合物。
的混合物。
 推测X的化学式是______。
推测X的化学式是______。 铝镓合金能与水发生置换反应,该反应的化学方程式为______。
铝镓合金能与水发生置换反应,该反应的化学方程式为______。 已知镓的化学性质与铝相似,易生成
已知镓的化学性质与铝相似,易生成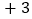 价的氧化物。常温下,铝镓合金在空气中反应的化学方程式为______。
价的氧化物。常温下,铝镓合金在空气中反应的化学方程式为______。 试分析该新工艺的优点
试分析该新工艺的优点 写两条
写两条 :______。
:______。 -
科目: 来源: 题型:
查看答案和解析>>【题目】某化学探究小组用盐酸与大理石的反应来研究影响反应速率的因素。实验温度为
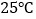 、
、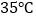 ;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙
;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙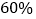 的大理石10g;所用盐酸的质量分数为
的大理石10g;所用盐酸的质量分数为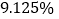 、
、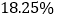 ,每次实验盐酸的用量为
,每次实验盐酸的用量为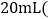 假设
假设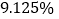 、
、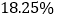 的盐酸的密度均为
的盐酸的密度均为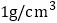 ;大理石中杂质不与盐酸反应
;大理石中杂质不与盐酸反应 。
。(提岀假设)盐酸与大理石反应的反应速率与所用盐酸的质量分数、大理石规格、反应温度有关。
 (实验设计与实施)完成以下实验设计方案并实验
(实验设计与实施)完成以下实验设计方案并实验实验
编号
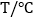
大理石
规格
盐酸的
质量分数
完全反应
的时间
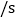
实验目的

25
粗颗粒
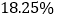
160
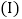 实验
实验 和
和 探究同体积下盐酸质量分数对该反应剧烈程度的影响。
探究同体积下盐酸质量分数对该反应剧烈程度的影响。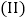 实验
实验 和
和 探究温度对该反应剧烈程度的影响。
探究温度对该反应剧烈程度的影响。 Ⅲ
Ⅲ 实验
实验 和
和 探究大理石规格对该反应剧烈程度的影响。
探究大理石规格对该反应剧烈程度的影响。
______
______
______
210

35
粗颗粒
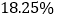
60
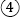
______
______
______
100
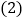 从实验
从实验 和
和 可以得出的实验结论是:______。
可以得出的实验结论是:______。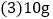 含碳酸钙
含碳酸钙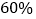 的大理石中,含有碳酸钙的质量为______g。
的大理石中,含有碳酸钙的质量为______g。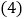 碳酸钙与盐酸反应的化学方程式为______;若
碳酸钙与盐酸反应的化学方程式为______;若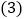 中的大理石与过量稀盐酸充分反应,能生成二氧化碳的质量为______
中的大理石与过量稀盐酸充分反应,能生成二氧化碳的质量为______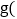 只列计算式,已知碳酸钙的相对分子质量为100,二氧化碳的相对分子质量为
只列计算式,已知碳酸钙的相对分子质量为100,二氧化碳的相对分子质量为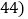 。
。 -
科目: 来源: 题型:
查看答案和解析>>【题目】在中学生“我与化学“活动中,小青以月饼食品中的“脱氧剂”
 如图
如图 为主题,组成小组开展探究。
为主题,组成小组开展探究。
(查阅资料)脱氧剂的工作原理是:在一定条件下,铁与空气中的氧气、水等物质发生氧化反应,把月饼包装中的氧气除去。
 (观察与思考)小青收集的脱氧剂是塑料袋包装,上面有许多小孔。这些小孔的作用是______。
(观察与思考)小青收集的脱氧剂是塑料袋包装,上面有许多小孔。这些小孔的作用是______。 (知识回顾)碳充分燃烧和不充分燃烧的产物是不同的,写出碳不充分燃烧的化学方程式:______。
(知识回顾)碳充分燃烧和不充分燃烧的产物是不同的,写出碳不充分燃烧的化学方程式:______。 (实验探究)剪开塑料袋,将脱氧剂中的物质倒在白纸上,观察,为黑色粉末。
(实验探究)剪开塑料袋,将脱氧剂中的物质倒在白纸上,观察,为黑色粉末。进一步查阅资料知:
脱氧剂的成分为:活性炭、铁粉、氯化钠。
检验氯化钠的反应的化学方程式为:
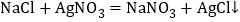 。
。取适量脱氧剂在烧杯中,加足量水,充分搅拌,过滤,得到黑色滤渣和无色滤液。进一步探究如下表
 请填写实验现象
请填写实验现象 :
:编号
实验操作
实验现象

取少量黑色滤渣在空气中烧灼,上方用蘸有澄清石灰水的玻璃棒实验,观察
______

取少量黑色滤渣于试管中,向其中加入足量稀盐酸,观察
______

取少量无色滤液于试管中,往其中加入硝酸银溶液,观察
______
(结论)脱氧剂中含有:活性炭、铁粉、氯化钠。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列实验装置图,按要求回答下列问题:
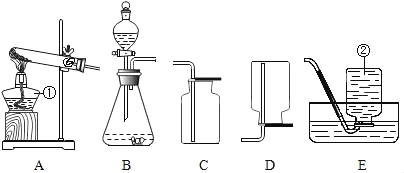
(1)写出标号仪器的名称:①______;②______。
(2)实验室可用氯酸钾和二氧化锰制取氧气,其反应的化学方程式为______,若要收集较纯净的氧气可选择的收集装置为______。
(3)实验室制取并收集二氧化碳应选择的装置为______; 装置B中用分液漏斗代替长颈漏斗的优点是
______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(5分)为测定某石灰石样品中碳酸钙的含量,取样品l0.0克于烧杯中再向其中加入稀盐酸50.0克,恰好完全反应(杂质不反应),反应后烧杯中物质总质量为56.7克。
(1)生成CO2的质量 。
(2)求石灰石样品中碳酸钙的质量分数(写出计算过程)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】碳和碳的化合物在人类生产生活中应用广泛,请根据相关知识回答以下问题:
(1)一氧化碳还原氧化铁的化学反应方程式______;
(2)金刚石、石墨、C60都是碳元素组成的单质,关于它们的说法正确的是______(填序号)
①碳原子的排列方式不同 ②都是黑色固体 ③都很软,可作润滑剂______ ④是同一种物质 ⑤完全燃烧都生成二氧化碳
(3)“低碳生活”中的“低碳”是指减少______(填化学式)的排放;
(4)X、Y、Z是初中化学常见的物质,它们之间有如图所示的转化关系。下列说法正确的是______;
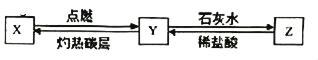
A.物质X和Y都是大气污染物
B.Y→Z的反应的基本类型是分解反应
C.在自然界中,Y转化为O2的主要途径是绿色植物的光合作用。
相关试题

