【题目】某实验小组取用生石灰时,发现装满生石灰的塑料试剂瓶已经膨胀破裂,于是小组中的几位同学对其中的成分进行了探究。

(提出猜想)小丹认为含有:CaO、Ca(OH)2;
小凯认为含有:CaO、Ca(OH)2、CaCO3;
小欣认为含有:Ca(OH)2、CaCO3。
(设计实验)
实验操作 | 实验现象 | 结论 | |
步骤一 | 取试样于试管中加水振荡 | 液体浑浊,用手摸试管外壁,感觉不发热 | ______________________ |
步骤二 | 向步骤一的试管中滴加无色酚酞溶液 | 溶液变红色 | ______________________ |
步骤三 | _______________________ | 试管内有气泡生成 | 一定含有CaCO3 |
(得出结论)通过以上探究可知_________同学的猜想正确,请写出使CaO变质的化学方程式:______。
(拓展)如果生石灰已全部变质为碳酸钙,请你设计实验加以证明(写出必要的步骤、现象和结论)___。
参考答案:
【答案】 一定不含CaO 一定含有Ca(OH)2 取试样于试管中,再向试管中加入足量稀盐酸 小欣 CaO+H2O![]() Ca(OH)2或Ca(OH)2+CO2
Ca(OH)2或Ca(OH)2+CO2![]() CaCO3 ↓+ H2O 取少量样品于试管中,加水溶解,取上层清液,滴加入无色酚酞溶液,再向试管中不溶物滴加足量稀盐酸;现象:上层清液不变色,有大量气泡冒出;结论:生石灰已全部变质为碳酸钙
CaCO3 ↓+ H2O 取少量样品于试管中,加水溶解,取上层清液,滴加入无色酚酞溶液,再向试管中不溶物滴加足量稀盐酸;现象:上层清液不变色,有大量气泡冒出;结论:生石灰已全部变质为碳酸钙
【解析】【设计实验】:(1)氧化钙和水反应生成氢氧化钙,放出大量热,所以用手摸试管外壁,感觉不发热,说明没有氧化钙;(2)向溶液中加入无色酚酞试液,如果酚酞变红,说明有氢氧化钙;碳酸钙和盐酸反应生成二氧化碳气体,产生气泡,氢氧化钙不能,所以验证碳酸钙,应向样品中加入足量的稀盐酸,试管内有气泡生成,说明一定含有CaCO3;【得出结论】(1)通过以上探究可知小欣同学的猜想正确, CaO变质的化学方程式:CaO + H2O === Ca(OH)2,氢氧化钙继续变质,方程式为: Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O; 【拓展】(2)如果生石灰已全部变质为碳酸钙,成分只有碳酸钙,没有氧化钙或氢氧化钙,验证方案是:取少量样品于试管中,加水溶解,取上层清液,滴加入无色酚酞溶液,再向试管中不溶物滴加足量稀盐酸;现象:上层清液不变色(说明没有氧化钙或氢氧化钙),有大量气泡冒出(说明有碳酸钙);结论:生石灰已全部变质。
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知NaHCO3在270 ℃时完全分解为碳酸钠、水和二氧化碳,而Na2CO3受热不分解。现有某工厂生产出的一批NaHCO3产品中混有少量的Na2CO3,某兴趣小组同学为了测定该产品中NaHCO3的质量分数,设计了下列两种实验方案。
方案一:样品
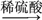 测定生成CO2的质量。
测定生成CO2的质量。(1)NaHCO3俗称_______,本实验采用如图所示的装置,C中盛放的物质是_______。
(2)若无装置E,在其他操作正确的情况下,_______(填“能”或“不能”)准确测定样品中NaHCO3的质量分数。
(3)在其他操作正确的情况下,不能将分液漏斗中的稀硫酸改为稀盐酸的原因是___________。
方案二:样品
 测定剩余固体质量
测定剩余固体质量具体操作步骤如下:
①取一只洁净的坩埚,称得质量为21.2克,再向其中加入样品,称得总质量为41.2克;
②加热盛有样品的坩埚;
③将坩埚充分冷却,称量坩埚和剩余固体的质量;
④多次重复步骤②和③至恒重,称得坩埚和剩余固体的总质量为35.0克。
(4)实验时需要重复“加热、冷却、称量”操作多次,其目的是__________________。
(5)根据题目中的信息,写出NaHCO3完全分解的化学方程式__________________。
(6)根据题意,计算样品中NaHCO3的质量分数为_____________。(请写出计算过程)
-
科目: 来源: 题型:
查看答案和解析>>【题目】某兴趣小组的同学对一包久置的生石灰(CaO)干燥剂产生了好奇,于是他们对这包干燥剂的成分展开了探究。
【提出问题】这包干燥剂是否变质,成分是什么?
【猜想假设】猜想一:全部是CaO; 猜想二:是CaO和Ca(OH)2的混合物;
猜想三:全部是Ca(OH)2; 猜想四:是Ca(OH)2和CaCO3的混合物。
【实验探究】(1)取部分该干燥剂于试管中,加水无放热现象,说明干燥剂中不含 。
(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂中含有 。
(3)为了进一步确定这包干燥剂中有无其他成分,小组同学设计了以下二种方案。
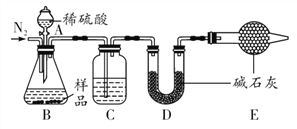
另取部分干燥剂于烧杯中,加水并搅拌,静置后取上层清液于3支试管中。请你参与实验,并填写表中的空白:
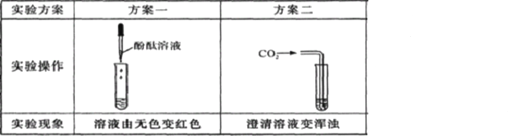
写出方案二发生的化学反应方程式 。
【实验结论】通过以上实验探究,得出猜想 成立。
【拓展迁移】小组同学反思生石灰干燥剂变质原因,认识到实验室保存氧化钙应注意 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图表示化学反应中溶液的颜色变化。下列叙述错误的是
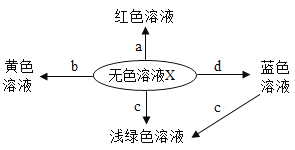
A. 若X是稀硫酸,a可能是紫色石蕊试液 B. 若X是稀硫酸,b可能是氧化物
C. 若X是稀盐酸,c不可能是单质 D. 若X是稀盐酸,d不可能是单质
-
科目: 来源: 题型:
查看答案和解析>>【题目】某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法正确的是

A.图中a点所示溶液中,含有的溶质是NaCl和Na0H
B.由a点到b点的pH变化过程证明酸和碱发生了中和反应
C.向图中c点所示溶液中滴加无色酚酞,溶液不变色
D.该实验是将盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列图象与所对应操作相符的是( )
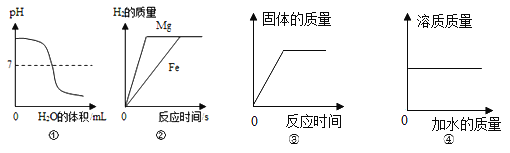
A. ①是对氢氧化钠溶液加水稀释
B. ②是将等质量镁片和铁片分别和等质量、等溶质质量分数的稀硫酸(足量)混合
C. ③向装有一定量铁粉的试管中滴加硫酸铜溶液
D. ④稀释氯化钠溶液
-
科目: 来源: 题型:
查看答案和解析>>【题目】右图是包含物质A、B、C、D和盐酸卡片的“化学拼图”,相邻两张卡片所标的物质(或其溶液)间能发生反应。
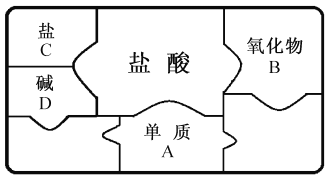
(1)A不可能是______(填标号)。
a.Mg b.Fe c.Ag d.Zn
(2)若B为铁锈的主要成分Fe2O3,B与盐酸反应的化学方程式为______。
(3)若C为碳酸钠
①C与D的反应属于______(填基本反应类型)。
②D与盐酸反应的化学方程式为______(写一个)。
③将二氧化碳通入C溶液,可化合生成碳酸氢钠( NaHCO3),该反应的反应物有______种。
相关试题

