【题目】兴趣小组同学取12.5g石灰石(杂质不与稀盐酸反应,也不溶于水)于烧杯中,向烧杯中加入稀盐酸,加入的稀盐酸和剩余固体的关系如下图。回答下列问题:
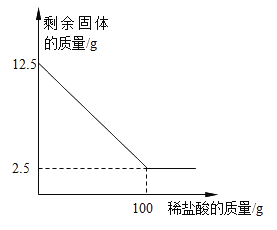
(1)石灰石中碳酸钙的质量分数是_____________。
(2)实验中产生的二氧化碳的质量是多少?(写出计算过程)
参考答案:
【答案】(1)80%
(2)解:设生成二氧化碳的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
10g X
![]() =
=![]()
X=4.4g
答(略)
【解析】(1)石灰石中杂质不与稀盐酸反应,也不溶于水,所以最后剩余的为杂质,所以石灰石中碳酸钙的质量为12.5g-2.5g=10.0g,则石灰石中碳酸钙的质量分数是![]() ×100%=80%。
×100%=80%。
(2)设生成二氧化碳的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
10g x
![]() =
=![]()
x=4.4g
答:实验中产生的二氧化碳的质量是4.4g。
-
科目: 来源: 题型:
查看答案和解析>>【题目】刘敏同学在化学课上提出,可用澄清石灰水来检验人呼出的气体是否含二氧化碳,就这一过程而言,属于科学探究环节中的
A.做出结论 B.收集证据 C.设计实验 D.建立假设
-
科目: 来源: 题型:
查看答案和解析>>【题目】兴趣组同学用木炭粉还原氧化铜一段时间后,发现剩余固体中有一些黑色粉末。甲同学取少量剩余固体加入5%的H2O2溶液中,发现有大量气泡迅速放出,于是兴趣小组同学进行了以下的探究

(1)乙同学取用少量剩余固体,在空气中灼烧,并在上方罩一个内壁涂有石灰水的烧杯(如图)进行实验,发现烧杯内壁的澄清石灰水不变浑浊,证明剩余固体中不含有__________。
(2)丙同学又进行了如下探究:
【提出问题】剩余固体的哪种物质加速了过氧化氢的分解,是过氧化氢溶液反反应的催化剂?

【猜 想】猜想Ⅰ.铜是H2O2溶液分解的催化剂。
猜想Ⅱ.氧化铜是H2O2溶液分解的催化剂。
【实验与判断】实验过程如下:
A.丙同学进行如右图所示实验,发现加入铜粉后几乎没有变化,证明猜想Ⅰ______(选填“成立”或“不成立”)。实验①的作用是______。
B.丙同学又用天平称量0.5g氧化铜,取5mL5%的过氧化氢溶液于试管中, 又进行如下实验:
实验
步骤
实验操作
实验现象
实验结论
步骤一

③的现象是
_________,木条复燃。
猜想Ⅱ成立
步骤二
步骤一中的③试管内的物质过滤,得到的固体烘干,称量。
质量为0.5g。
步骤三
步骤②得到的固体,加入到盛5%的过氧化氢溶液的试管中,把带火星的木条伸入试管中。
有气泡产生,
________。
步骤三的目的是__________________。过氧化氢能被氧化铜催化分解放出氧气的化学化学方程式为____________________。
【拓展】除了催化剂能改变化学反应的速率,你猜想还有那些因素也可能影响化学反应的速率_______________________(写一个即可)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关物质性质的叙述中,属于物质化学性质的是
A.标准状况下氧气的密度是1.429g/L
B.二氧化碳能使澄清的石灰水变浑浊
C.二氧化硫是无色具有刺激性气味的气体
D.在101kPa时,-218℃液态氧能变成雪花状的淡蓝色固体
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列关于“酒精温度计遇冷读数下降”的微观解释正确的是
A. 分子体积缩小 B. 分子间间隔减小
C. 分子停止运动 D. 分子种类发生了变化
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学概念在逻辑上存在如图所示的关系,对下列概念间的关系说法正确的是( )

A.纯净物与混合物属于包含关系
B.化合物与氧化物属于包含关系
C.单质与化合物属于交叉关系
D.氧化反应与化合反应属于并列关系
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质的用途中,主要利用其物理性质的是
A. 氧气用作火箭的助燃剂 B. 氮气用作食品保护气
C. 干冰用于人工降雨 D. 镁粉用于制烟花
相关试题

