【题目】通过一个学年的化学学习,我们已经了解了实验室制取气体的某些规律,以下是老师提供的一些实验装置。请结合下图回答:

(1)写出图中标号仪器的名称:a_____________;
(2)实验室常用石灰石和稀盐酸在常温下反应制取二氧化碳,若用F装置收集该气体,则气体从_____端进入(填c或d)。
(3)氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水;实验室通过加热氯化铵(NH4Cl)和氢氧化钙固体混合物制取氨气,则实验室制取氨气选择的发生和收集装置是_________。(填字母)
参考答案:
【答案】长颈漏斗 d A和E
【解析】
(1)据图可知仪器a的名称是长颈漏斗;
(2)二氧化碳的密度比空气的大,若用F装置收集该气体,则气体从d端进入,将空气从短导管排出;
(3)实验室通过加热氯化铵(NH4Cl)和氢氧化钙固体混合物制取氨气,属于固体加热型,应该选用的发生装置是A;氨气密度比空气小且极易溶于水,应用向下排空气法收集,所以应该选择E装置来收集。
-
科目: 来源: 题型:
查看答案和解析>>【题目】I.已知A、B、C、D、E五种物质中均含有某种相同的非金属元素,B为无色液体,C为黑色固体,D气体能使澄清石灰水变浑浊。图中“→”表示物质之间的转化关系。五种物质的转化关系如图所示(图中反应条件及部分反应物或生成物省略)。

(1)A、E的化学式分别是_____________、__________________。
(2)A→C反应的化学方程式是___________________________。
(3)A→B反应的化学方程式是___________________________。
II.工业制取硝酸的流程如下:
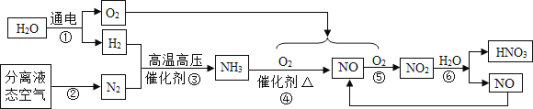
(1)步骤②是利用了氮气与氧气____________的不同,是____________变化(填“物理“或”化学“)。
(2)步骤③是化合反应,写出③的化学方程式为_______________________________。
(3)步骤④的化学方程式为 4NH3+5O2
 4NO+6X,X的化学式为_________________。
4NO+6X,X的化学式为_________________。(4)流程中一定要循环使用的物质是_____________________(写化学式)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙两物质的溶解度曲线如图所示。下列叙述中,正确的是( )
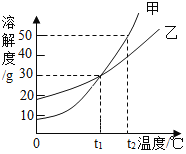
A. t1℃时,甲的溶解度大于乙的溶解度
B. t2℃时,甲和乙溶液中溶质质量分数相等
C. t2℃时,在100g水中放入60g甲,其溶质的质量分数为37.5%
D. 甲溶液中含有少量乙时,用降温结晶的方法提纯甲
-
科目: 来源: 题型:
查看答案和解析>>【题目】新版水污染防治法于2018年一月一日起正式施行。此次水污染防治法修改,将河长制首次纳入立法范畴,重点关注农村水环境治理,加大环境监测数据造假惩处力度,进一步转向水环境综合治理。我市某化学兴趣小组的同学用洁净的塑料瓶从捞刀河中取回一定量的水样,进行如下研究:
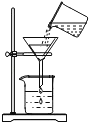
(1)将浑浊的河水样品倒入烧杯中,加入________(吸附杂质,使杂质沉降)搅拌,溶解后静置一会儿;
(2)将静置后的河水采用右图装置进行过滤,请问:图中还缺少的一种仪器是_________;
(3)过滤后得到的水澄清透明,取少量于小烧杯中,加入肥皂水并搅拌,发现烧杯中有大量浮渣,则说明河水是硬水。日常生活中使用硬水会带来许多麻烦,家庭生活中常用来降低水硬度的方法是___。
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙、丙、丁、戊分别是HCl、Na2SO4、Ba(NO3)2、NaOH、BaCl2五种溶液中的一种。现利用X溶液加以鉴别,其中白色沉淀Ⅱ不溶于稀硝酸。它们之间存在如下图所示的转化关系:
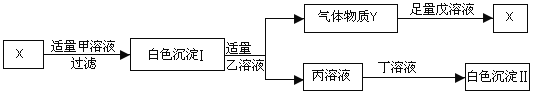
请填空:
(1)写出X的化学式:_____________;
(2)写出Y与足量戊溶液反应的化学方程式:________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某矿石由MgO、Fe2O3、CuO、SiO2组成,先将矿石粉碎,再用它制备氢氧化镁,流程示意图如图所示:
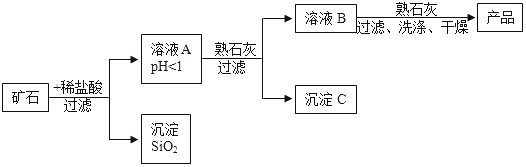
(1)矿石粉碎的目的是___________。
(2)溶液A中共含有________种阳离子。
(3)在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子转化为沉淀。该实验条件下,使金属阳离子沉淀的相关pH数据见下表。
氢氧化物
Fe(OH)3
Cu(OH)2
Mg(OH)2
开始沉淀的pH
1.5
4.2
8.6
完全沉淀的pH
3.2
6.7
11.1
为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可容许的范围为__________,溶液B中一定含有的溶质为_______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】同学们发现新鲜的苹果汁在空气中放置一段时间后会变色,仿佛铁生锈一样。于是,研究性小组同学设计并进行实验,探究苹果汁变色的原因。
(查阅资料)
a.苹果汁中含有0.001%的二价铁物质,同时也含有多酚类物质,多酚可与空气中的氧气反应变为褐色。
b.二价铁在空气中或与浓硝酸反应都能变为三价铁,且三价铁的溶液为黄色
c.硫氰化钾(KSCN)溶液变色规律
药品
二价铁溶液
三价铁溶液
KSCN溶液
不变色
变红色
(猜想与假设)
Ⅰ.苹果汁变色与苹果中的铁元素有关
Ⅱ.苹果汁变色是苹果汁中的多酚物质与空气中的氧气反应的结果
(进行实验)
编号
实验操作
实验现象
实验1
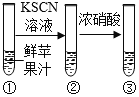
②中未出现明显变化
③:
实验2
分别放置于空气中一段时间(如下图所示)

试管编号
1min
10min
24小时
①
黄褐色
褐色
深褐色
②
无明显变化
无明显变化
无明显变化
③
略有些黄色
浅黄
黄色
实验3
(解释与结论) (1)实验1验证了苹果汁中含有二价铁物质。在该实验中③的现象是______________。
(2)实验2的②中FeSO4溶液溶质的质量分数为________%,该实验得出的结论是________。
(3)若试验3验证猜想Ⅱ成立的操作是:在除去氧气的空气中放置一段时间鲜苹果汁。则现象是:______________。
(反思与评价)
(4)写出一种防止苹果汁变色的方法:______。
相关试题

