【题目】课外活动小组为了测定石灰石的纯度,取25g石灰石放入85g稀盐酸的烧杯中,待石灰石完全反应后(杂质不与盐酸反应),烧杯中混合物的质量为101.2 g。求:
(1)生成二氧化碳的质量。
(2)该石灰石中碳酸钙的质量分数。
参考答案:
【答案】(1) 8.8g (2)80%
【解析】石灰石完全反应,即25g石灰石的主要成分碳酸钙全部发生反应,反应中只放出气体二氧化碳,所以反应前后物质总质量会减少,且减少的质量即为二氧化碳气体的质量。
解:(1)、反应中产生CO2的质量为:25+85-101.2=8.8g
(2)、设石灰石中碳酸钙的质量为x。
CaCO3+2HCl=CaCl2+H2O+CO2↑
10044
x8.8g![]()
解之得 x=20g
石灰石中碳酸钙质量分数=![]() ×100%=80%
×100%=80%
答:该石灰石中碳酸钙的质量分数为80%
-
科目: 来源: 题型:
查看答案和解析>>【题目】地沟油中含有一种强烈致癌物黄曲霉素B2(C17H14O6),长期食用会引起消化道癌变,请回答:
(1)黄曲霉素B2的相对分子质量为 ;
(2)黄曲霉素B2中碳、氢、氧三种元素的原子个数比为 ;
(3)15.7g黄曲霉素B2中含有 g氧元素.
-
科目: 来源: 题型:
查看答案和解析>>【题目】兴趣小组的同学学习了金属的性质后,在实验室找到的一种银白色金属R做如下探究:
(1)将金属R投入稀盐酸中,金属表面有气泡冒出。则该金属R在金属活动性顺序表中排在氢的___(选填“前面”或“后面”)。
(2)为了比较金属R与铁的活动性强弱,兴趣小组设计下列方案实验,请完成下表:
你的一种猜想
验证方法
现象
结论
金属R的活动性比铁______
将金属R投入_________
溶液中
金属R表面有黑色的物质析出
猜想_______(选填“正确”或“错误”)
(3)请根据上述的信息,标出金属Fe、R、Cu在下列金属活动性顺序表中的相应位置。
 ____
____ -
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列装置回答下列问题:
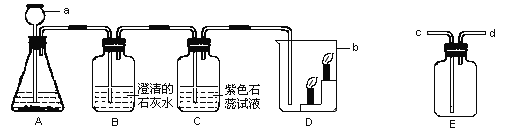
(1)仪器名称:a_______________b_______。
(2)若实验室制取二氧化碳时,长颈漏斗中加入的药品是_____ ,锥形瓶中加入的药品是__________。
(3)装置A中发生的化学方程式为____________,装置C中观察到的现象是___________。
(4)装置D中观察到的现象是___________,说明二氧化碳______________,______________。由此可知,二氧化碳在生活中可用于 ____________ 。
(5)实验室用装置E来收集二氧化碳时,二氧化碳应从 ____(填“c端”或“d端”)通入。
(6)用A装置还可制取________气体,反应的方程式为______________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】水是生命之源、万物之基,是人类宝贵的自然资源,我们每个人都要关心水、爱护水、节约用水。
(1)我国规定生活饮用水的水质必须达到下述四项指标:a.不得呈现异色 b.不得有异味 c.应澄清透明 d.不得含有细菌和病毒。其中“c指标”可以通过________ 操作达到。
(2)下列为净化水的操作,其中净化程度最高的是_______。
A. 吸附 B. 蒸馏 C. 过滤 D.静置沉淀
(3)世博园直饮水主要生产流程为:自来水→活性炭→超滤膜分离→紫外线消毒→直饮水,其中活性炭起_______作用。
(4)生活中可以采用____________区分硬水和软水,如果水的硬度大或者病原微生物过多,都可以采取________的方法来降低水的硬度和杀灭病原微生物。
(5)自来水中含有少量Ca(HCO3)2等可溶性化合物,烧水时Ca(HCO3)2发生分解反应,生成难溶性的碳酸钙、水和二氧化碳,这就是壶中出现水垢的原因之一。请写出Ca(HCO3)2受热分解的化学方程式:________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(1)久置的石灰水瓶壁上出现的白膜是________(化学式),形成原因的化学方程式____________,用_____(化学式)可以清洗。
(2) 天然气是常用的燃料,它的主要成分的名称是____,燃烧的化学方程式是__________。
(3)古籍记载:“曾青得铁则化为铜”(曾青指硫酸铜溶液),用化学方程式表示为________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列说法正确的是 ( )
A. 从外观上可区分硫酸钾和磷矿粉两种肥料
B. 等质量的Na2CO3和NaHCO3分别与足量盐酸反应产生等质量的CO2
C. 将硝酸铵肥料与生石灰长期堆放在一起
D. 反应3CO+Fe2O3
 2Fe+3CO2是置换反应
2Fe+3CO2是置换反应
相关试题

