【题目】已知元素周期表中第三周期各元素原子结构示意图如下图所示,请回答:

(1)从原子结构方面看:同一周期的元素的原子具有的相同点是_____________。
(2)氧元素的原子的结构示意图是:![]() ,氧原子在化学反应中易______(填“得到”或“失去”)电子,变成_______离子;氧元素与上图中的_______(填元素符号)元素化学性质相似。
,氧原子在化学反应中易______(填“得到”或“失去”)电子,变成_______离子;氧元素与上图中的_______(填元素符号)元素化学性质相似。
(3)钠元素与硫元素形成的化合物的化学式是__________。
(4)请写出该周期从左到右呈现的一个规律____________________。
参考答案:
【答案】 电子层数相同 得到 阴 S Na2S 质子数依次增大(或核电荷数、核外电子数、最外层电子数依次增大)
【解析】(1) 在原子结构示意图中,小圆圈表示原子核,圆圈内的数字表示质子数,质子数决定原子的类别,弧线表示电子层,弧线上的数字为该层上的电子数。从原子结构方面看:同一周期的元素的原子具有的相同点是电子层数相同;(2) 最外层电子数决定原子的化学性质,当最外层电子数小于4时,反应中易失去电子成为阳离子;当最外层电子数大于4时,反应中易得到电子成为阴离子;原子核外只有一个电子层且电子数为2,或者最外层电子数为8的结构为稳定结构,不易得失电子。氧元素的原子的结构示意图是:![]() ,氧原子在化学反应中易得到电子,变成阴离子;具有稳定结构的原子化学性质相似;非稳定结构的原子,最外层电子数一样的化学性质相似。氧元素与上图中的硫元素化学性质相似;(3)化合物中钠元素显+1价,硫元素显负价时显-2价,化合物的化学式书写:显正价的元素其符号写在左边,显负价的写在右边,化合价的绝对值交叉约减,得化学式右下角的数字,数字为1时不写,钠元素和硫元素形成的化合物的化学式是Na2S;(4)请写出该周期从左到右呈现的一个规律: 质子数依次增大(或核电荷数、核外电子数、最外层电子数依次增大)。
,氧原子在化学反应中易得到电子,变成阴离子;具有稳定结构的原子化学性质相似;非稳定结构的原子,最外层电子数一样的化学性质相似。氧元素与上图中的硫元素化学性质相似;(3)化合物中钠元素显+1价,硫元素显负价时显-2价,化合物的化学式书写:显正价的元素其符号写在左边,显负价的写在右边,化合价的绝对值交叉约减,得化学式右下角的数字,数字为1时不写,钠元素和硫元素形成的化合物的化学式是Na2S;(4)请写出该周期从左到右呈现的一个规律: 质子数依次增大(或核电荷数、核外电子数、最外层电子数依次增大)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某兴趣小组探究分子的特性时做了以下三组实验。
【实验一】已知:碱性溶液能使酚酞试液变红,而氨水呈碱性,打开盛浓氨水的试剂瓶时能够闻到强烈刺激性气味。请回答实验中的有关问题:
(1)甲同学用小烧杯取约40mL蒸馏水,向其中滴入5~6滴酚酞溶液,搅拌均匀,溶液的颜色无明显变化
(2)如图1所示,取上述溶液置于试管中,向其中慢慢滴加氨水,观察溶液颜色的变化是 ,通过上述实验,得出的结论是

(3)将烧杯中的酚酞溶液分别倒入A、B两个小烧杯中,另取一个烧杯C,向其中加入约5mL浓氨水.用一个大烧杯罩住A、C两个小烧杯,烧杯B置于大烧杯外(如图2所示).观察几分钟,烧杯A、B发生现象分别是
,这一现象说明 B烧杯的作用是 。
【实验二】乙同学将实验一进行改进(如图3所示)后进行有关分子性质的探究实验:在试管中的滤纸条上相间滴有无色酚酞溶液,试管口塞上一团蘸有浓氨水的棉花,试管中看到的现象是 此现象说明了: 。
如下图所示,某同学在玻璃管两端分别放入蘸有浓氨水和浓盐酸的棉花团,发现C处产生的白烟较多.

查阅相关资料可知:已知①浓氨水能挥发出氨气,浓盐酸能挥发出氯化氢气体,二者接触反应会产生白烟(即氯化铵固体);②由于分子质量小,所以化学上引入了分子的相对质量来表示分子的质量,即相对分子质量。③氨气分子的相对质量是17,氯化氢分子的相对质量是36.5。由此可知,分子的运动速率与相对分子质量的关系是 。
【实验三】丙同学设计实验如图4所示,在一个玻璃杯中放入约50ml水,向水中放入一大块糖块,在容器外壁沿液面画一条水平线,当糖块消失后,液面比水平线 (“高”“低”“相平”),这一现象说明了 ,同时还可以说明 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室制取气体所需装置如下图所示。
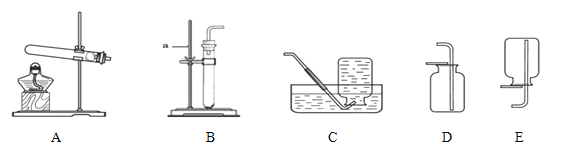
请回答以下问题:
(1)装置中标“a”的仪器名称是____________。
(2)用A装置制取气体时,要先预热,预热的操作方法是_______________。
(3)用高锰酸钾制取氧气反应的化学符号表达式为:_______________,用高锰酸钾制取氧气所选用的发生装置是______ (填序号,下同),用过氧化氢溶液和二氧化锰制取氧气应选用的发生装置是________。用过氧化氢溶液和二氧化锰制取氧气比用高锰酸钾制取氧气要好,其优点是___________________________(写一点)。
(4)收集较纯净的氧气应选择的收集装置是 ______(填序号),能用E装置收集的气体,其物理性质是__________________。检查B装置气密性的方法为_______________。
(5)若用D装置收集氧气时,检验是否收集满的方法是_______________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】用化学符号填空:①2个碳原子________;②2个水分子________;③2个铁离子________;④硫元素的化合价为﹣2价________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列有关实验回答问题:
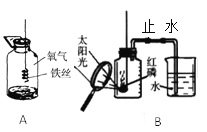
(1)如果A实验瓶中没有少量的水,导致的后果可能是_________________。A实验反应的化学符号表达式为 _________________,(例如:碳在氧气中燃烧的化学符号表达式为C+O2
 CO2,本试题的有关化学符号表达式都用这种形式表示)
CO2,本试题的有关化学符号表达式都用这种形式表示)(2)B是测定空气中氧气含量的的实验改进,改进后的优点是________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是某品牌补铁剂的标签。

(1)一个富马酸亚铁分子中含有______个原子,富马酸亚铁中C、H、Fe、O四种元素的质量比为_______________(填最简整数比)。
(2)富马酸亚铁的相对分子质量为__________。
(3)若每次服用一包该补铁剂,摄入铁元素的质量为__________mg(计算结果取整数)
-
科目: 来源: 题型:
查看答案和解析>>【题目】(8分)硫酸铵的化学式为(NH4)2SO4
(1)硫酸铵中氮元素的质量分数为___________(精确到0.1%)
(2)小明同学取100g含杂质的硫酸铵化肥进行检测,测得含氮元素质量为21g,计算这100g化肥中含有硫酸铵的质量是_______?
(3)小芳同学测得某含杂质的硫酸铵化肥的含氮量为26%,则含有的杂质可能是______(可能不止一个正确选项)
A.尿素CO(NH2)2 B.碳酸氢铵NH4HCO3 C. 硝酸铵NH4NO3
相关试题

