【题目】向100gBaCl2溶液中滴加Na2SO4溶液,至恰好完全反应,共用去Na2SO4溶液30g.反应后过滤得到溶液125.34g,请计算:(反应的化学方程式为BaCl2+Na2SO4═BaSO4↓+2NaCl)
(1)生成BaSO4的质量。
(2)BaCl2溶液中溶质的质量分数(写出计算过程)
参考答案:
【答案】(1)4.66g;(2)4.16%
【解析】
试题分析:(1)生成硫酸钡沉淀的质量为:100g+30g﹣125.34g=4.66g;
(2)设参加反应的氯化钡的质量为x
BaCl2+Na2SO4═BaSO4↓+2NaCl
208 233
x 4.66g
![]() x=4.16g
x=4.16g
所以BaCl2溶液中溶质的质量分数为:4.16/100×100%=4.16%
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图是甲乙两物质在高温条件下发生化学反应的微观示意图,根据图示回答:
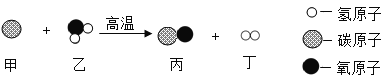
(1)该反应的基本类型是 。
(2)属于化合物的是 (写化学式)。
(3)一个丁分子是由 构成的。
(4)上述反应中,不发生改变的粒子是 (填“分子”或“原子”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在学习酸的化学性质后,同学们做了如图所示的A、B两个实验:
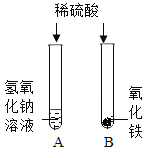
(1)A试管中发生反应的化学方程式 。向B试管中的加入足量的稀硫酸,观察到的现象是 。
(2)实验结束后,小红将A、B两试管中的废液倒入同一洁净的烧杯中,片刻后发现烧杯中出现了红褐色沉淀,经分析,红褐色沉淀是氢氧化铁。
小红将烧杯中物质进行过滤得到无色滤液,滤液中含有什么溶质?小红、小军对此进行探究。
【实验讨论】
①小红分析了反应物和生成物之后,认为滤液中不可能有H2SO4,因为 。
②小军认为滤液中不可能有Fe2(SO4)3,理由是 。
【提出猜想】
猜想Ⅰ:Na2SO4 NaOH
猜想Ⅱ:
【设计实验】
实验操作
实验现象
结论
取少量滤液于试管中,向其中滴加酚酞试液
猜想Ⅰ成立
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列情况不会造成空气污染的是
A.机动车辆排放尾气
B.增加城市绿地面积
C.工厂排放废气
D.建筑工地产生大量沙尘
-
科目: 来源: 题型:
查看答案和解析>>【题目】 化学变化的本质特征是
A.发光放热 B.生成新物质 C.颜色发生变化 D.有气体逸出
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关化学概念理解正确的是( )
A.氯化钠在20℃时的溶解度是36g,则100g的氯化钠溶液中含有氯化钠36g
B.含氧元素的化合物一定是氧化物
C.氧化反应一定是化合反应
D.化合物一定是由不同种元素组成的
-
科目: 来源: 题型:
查看答案和解析>>【题目】如表中,有关量的变化图象与其对应叙述相符的是( )
A
B
C
D
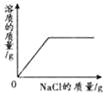
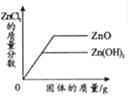

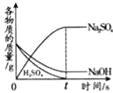
向接近饱和的NaCl溶液中加入固体NaCl
向等质量、等质量分数的两份稀盐酸中分别加入足量的ZnO和Zn(OH)2
向Na2CO3溶液中加入一定溶质质量分数的NaOH溶液
等质量、等质量分数的H2SO4溶液与NaOH溶液混合
A.A B.B C.C D.D
相关试题

