【题目】某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如图所示实验,并对反应后锥形瓶中残留废液进行探究.
【提出问题】
废液中所含溶质是什么物质?
【猜想与假设】
猜想(一):废液中的溶质可能是NaCl、Na2CO3和HCl.
猜想(二):废液中的溶质只有NaCl.
猜想(三):废液中的溶质是NaCl和HCl.
猜想(四):废液中的溶质是________.
【讨论与交流】
小明认为猜想(一)无需验证就知道是错误的.他的理由是________.
【实验与结论】
(1)为验证猜想(二),小强同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解.于是小强认为猜想(二)正确.小强的实验________(填“能”或“不能”)验证猜想(二)的正确性,原因是________________________________________________.
(2)小丽为验证猜想(三),选用大理石做试剂.若猜想(三)是正确的,验证时反应的化学方程式为________________________________________.
(3)若验证猜想(四)是否正确,下列试剂中可选用的有________(填序号).
①氢氧化钠溶液 ②氯化钙溶液 ③稀盐酸 ④氯化钾溶液
【拓展与应用】
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行________操作即可从废液中得到NaCl固体.此方法的缺点是________________________.

参考答案:
【答案】【猜想与假设】Na2CO3和NaCl
【讨论与交流】在溶液中Na2CO3和HCl不能共存
【实验与结论】(1)不能 溶液中若有HCl,遇AgNO3溶液也能产生不溶于稀HNO3的白色沉淀
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)②③
【拓展与应用】蒸发 挥发出的HCl气体会污染空气
【解析】Na2CO3与HCl反应生成NaCl、H2O和CO2,当Na2CO3过量时,废液中的溶质还可能是Na2CO3和NaCl.在溶液中Na2CO3和HCl不能共存,相互能反应,所以猜想废液中的溶质可能是NaCl、Na2CO3和HCl肯定是错误的.溶液中若有HCl,滴加AgNO3溶液也能产生不溶于稀HNO3的白色沉淀,所以滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解,不能证明只有NaCl.大理石的主要成分是CaCO3,能与盐酸反应生成二氧化碳气体.要证明Na2CO3存在,可以滴加氯化钙溶液看是否有沉淀生成,也可以滴加稀盐酸看是否有气体生成.
-
科目: 来源: 题型:
查看答案和解析>>【题目】有氮气、一氧化碳和二氧化碳的混合气体80 g,其中碳元素的质量分数为30%。使该混合气体通过足量的灼热氧化铜充分反应后。再将气体通入过量的石灰水中,能得到白色沉淀的质量为
A.30 g B.100 g C.150 g D.200 g
-
科目: 来源: 题型:
查看答案和解析>>【题目】以下是一些常见物质间互相转化的关系图(部分反应条件已省略).已知A、B、X、Y均为无色气体,E、F为常见单质.
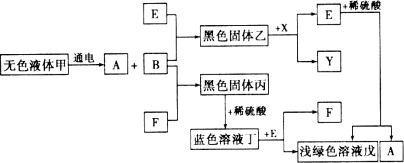
请回答:
(1)写出下列物质的化学式:F________、戊________.
(2)写出下列转化的化学方程式:
①甲→A+B________________________________;
②乙+X→E+Y________________________________.
(3)写出蓝色溶液丁中溶质的一种用途:________________________________________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】“侯氏制碱法”首先得到的是碳酸氢钠,然后将碳酸氢钠加热分解得到产品碳酸钠:2NaHCO3
 Na2CO3+CO2↑+H2O.碳酸钠露置在空气中能与空气中的二氧化碳和水反应生成碳酸氢钠:Na2CO3+CO2+H2O=2NaHCO3.
Na2CO3+CO2↑+H2O.碳酸钠露置在空气中能与空气中的二氧化碳和水反应生成碳酸氢钠:Na2CO3+CO2+H2O=2NaHCO3.某中学化学研究性学习小组对一瓶开启后久置的碳酸钠是否变质及变质程度进行研究.
【提出假设】 假设Ⅰ:完全变质;假设Ⅱ:没有变质;假设Ⅲ:________________.
【实验探究】 实验一:取少量样品于试管中,加水溶解后再加入少量CaCl2溶液,产生白色沉淀,说明假设________不成立.反应的化学方程式为________________________.
实验二:取少量样品于试管中,用导管连接后固定在铁架台上,导管的另一端插入澄清石灰水中.加热样品,有气体产生,澄清的石灰水变浑浊,说明假设________不成立.
【实验结论】 假设________成立,样品的成分是________.
【交流反思】 欲除去Na2CO3变质后产生的杂质,最合适的方法是________________________________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】生活中用到的下列物质,属于纯净物的是
A.调味用的食盐水
B.温度计中的水银
C.取暖用的煤炭
D.自来水
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室有三瓶化肥未贴标签,只知道它们分别是碳酸氢铵(NH4HCO3)、氯化铵(NH4Cl)和尿素[CO(NH2)2]中的一种.为鉴别三种化肥,某同学分别取少量样品编号为A、B、C,并进行如下实验(此处箭头表示得出实验结论):

根据上述实验回答:
(1)写出三种化肥的名称:A________;B________;C________.
(2)如果实验Ⅱ中B、C两种样品没有另取,对实验结果________(填“有”或“无”)影响.
(3)常温下如要鉴别B、C两种样品,________(填“能”或“不能”)采取闻气味的方法.
(4)由实验和查阅资料可知,人们在施用铵态氮肥时,若遇到碱性物质,会使铵态氮肥转化为氨气,氨气进入大气后与雨水作用,可能形成“碱雨”.“碱雨”中碱的化学式为________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】某同学实验时记录的现象,其中正确的是
A.红磷在空气中燃烧,产生大量白色烟雾
B.硫在氧气中燃烧,产生微弱的淡蓝色火焰
C.硫酸铜溶液中滴加氢氧化钠溶液,产生白色沉淀
D.向滴有酚酞的氢氧化钠溶液中不断滴加盐酸,溶液由红色逐渐变成无色
相关试题

