【题目】(二)铁的化合物应用
黄铁矿(主要成分是FeS2),是一种重要的化工原料,可用来制备硫酸和炼铁。
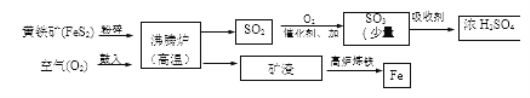
【1】工业上将黄铁矿粉碎的目的是____________________。
【2】生产硫酸后的尾气中含有SO2,如直接排放可能会造成环境问题是__________________。
【3】高炉炼铁的化学方程式为__________________________。
【4】150吨含FeS2 80%的黄铁矿理论上最多可以制得98%的浓硫酸________________吨。
参考答案:
【答案】
【1】 增大反应物接触面积,加快反应速率(或提高黄铁矿的利用率或使反应更加充分等)
【2】 酸雨
【3】 Fe2O3+3CO![]() 2Fe+3CO
2Fe+3CO
【4】 200
【解析】
增大反应物之间的接触面积可加快反应速率;化学反应遵守质量守恒定律;通过桥梁找出已知量与未知量之间的质量关系,然后进行计算即可。
【1】反应物之间的接触面积越大,反应速率越快。
【2】二氧化硫属于空气污染物,当空气中二氧化硫含量较高时,如果下雨,会形成酸雨,腐蚀建筑物、使树木枯萎等。
【3】化学反应前后原子种类不变、各种原子个数相等,Fe2O3+3CO ![]() 2Fe+3CO2 。
2Fe+3CO2 。
【4】根据化学反应前后硫元素质量不变可知,FeS2~2SO2~2SO3~2H2SO4,设150吨含FeS2 80%的黄铁矿理论上最多可以制得98%的浓硫酸的质量为x,则
FeS2 ~ 2H2SO4
120 196
150t×80% x×98%
![]() =
=![]() ,解得x=200t
,解得x=200t
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图表示某些物质间转化关系。已知D是一种最常见液体,C为紫红色金属,E为黑色固体。A、B、M、F为气体,F能参与绿色植物的光合作用。请回答:
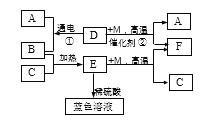
(1)E的化学式______;
(2)蓝色溶液中一定含有的溶质是______________(写化学式);
(3)写出下列反应的化学方程式:①__________;②__________;实验室进行反应①时,常加入少量稀硫酸,其目的是__________。
(4)工业上可用A和F合成乙醇(C2H6O),反应中A和F的质量比为__________。
-
科目: 来源: 题型:
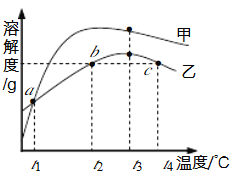
查看答案和解析>>【题目】MgSO4和Na2CO3的溶解度表及溶解度曲线如下。下列说法错误的是
温度/℃
20
30
40
50
60
70
80
溶解度
S/g
MgSO4
25.1
28.2
30..8
32.9
34.3
35.0
34.9
Na2CO3
21.5
39.7
49.0
48.5
46.0
45.2
43.9
A. 甲为Na2CO3
B. 乙的饱和溶液从t1升温到t4,溶质质量分数增大
C. 等质量甲、乙饱和溶液从t3降温到t1,析出晶体的质量(不带结晶水):乙>甲
D. b、c点乙的饱和溶液溶质质量分数相等,且大于a点甲的饱和溶液溶质质量分数
-
科目: 来源: 题型:
查看答案和解析>>【题目】(一)铁的应用和防护
【1】我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理______________。
【2】铁生锈的主要过程为
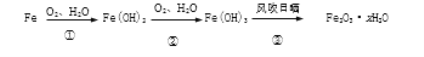
(1)写出转化①的化学方程式________________________
(2)转化③生成Fe2O3·xH2O,则x≤____________(x为整数)。
【3】请提出防止铁生锈的一条措施________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(三)铁的冶炼和探究
取24.0g Fe2O3粉末,小组同学用下图装置模拟炼铁,并测定反应后固体成分。
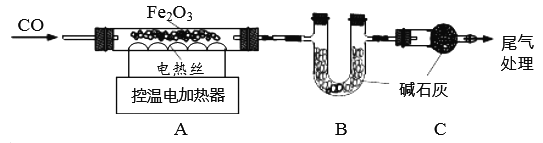
资料:碱石灰可吸收H2O和CO2。
【1】连接装置,先______________________,再装入药品。
【2】实验时先通入CO,目的是______________________________。
【3】控制A中温度在700℃至固体全部变黑,继续通CO至冷却。
(1)通过测定装置B中固体的质量变化,可准确求得装置A中剩余固体质量。装置C的作用是____。
(2)现直接测得装置A中剩余固体质量为19.2g。则装置B中固体应增重________________g。
【4】经分析A中剩余固体19.2g为Fe和FexOy的混合物,向其中加入足量的稀H2SO4充分反应,得H2 0.3g。
(1)固体中Fe质量为__________________g。
(2)FexOy的化学式为__________________
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙两种物质的溶解度曲线如图所示.下列说法中正确的是( )
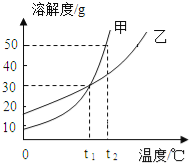
A. t1℃时,甲和乙的饱和溶液升温到t2℃时仍是饱和溶液
B. t1℃时,甲和乙各30g分别加入100g水中,充分溶解,均形成饱和溶液
C. t2℃时,甲和乙的饱和溶液各100g,其溶质的质量相等
D. t2℃时,在100g水中加入60g甲,充分溶解,形成不饱和溶液
-
科目: 来源: 题型:
查看答案和解析>>【题目】(4分)A、B、C、D为初中常见的物质,A与B之间发生的化学反应可表示为:“A+B→C+D”
(1)若C为氯化钠,D为氧化物,且在A溶液中加入铁粉能产生氢气.则A为 。若A、B两溶液恰好完全反应.则反应后溶液的pH 7(“>”或“<”或“=”)。
(2)若A和B均为黑色粉末,A与B反应时可观察到黑色粉末变为红色,同时生成能使澄清石灰水变浑浊的无色气体,则A与B反应的化学方程式为 。(2分)
相关试题

