【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示:
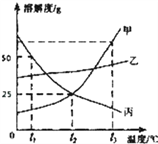
(1)甲在 t2℃时的溶解度为____;
(2)t1℃时 30g 丙与 50g 水充分溶解形成____(填“饱和”或“不饱和”)溶液;
(3)甲的饱和溶液中含有少量的乙可以采用____ 提纯甲.
(4)下列说法错误的是____(填序号).
A.从 t3℃甲、乙、丙的饱和溶液降温到 t2℃时,析出晶体最多的是甲
B.将 t2℃50g 丙的饱和溶液加水稀释成溶质质量分数为 10%的丙溶液,需要用到的仪器有:烧 杯、玻璃棒、量筒(50ml)、胶头滴管
C.t2℃乙的饱和溶液中加入固体甲,乙的溶质的质量分数不变
D.t3℃等质量甲、乙、丙的饱和溶液中,含溶剂最多的是丙
E.将接近饱和的甲溶液变成甲的饱和溶液,溶质质量分数可能不变.
参考答案:
【答案】 25g 饱和 降温结晶; AC
【解析】根据所学知识和题中信息知,(1)甲在 t2℃时的溶解度为25g。(2)t1℃时丙溶解度是50g,30g丙与50g水充分溶解形成饱和溶液。(3)甲的饱和溶液中含有少量的乙可以采用降温结晶提纯甲,甲物质溶解度随温度的升高而增大,乙物质溶解度随温度的升高而变化不大。(4)A、甲物质溶解度随温度的升高而增大,乙物质溶解度随温度的升高而变化不大,乙物质溶解度随温度的升高而减小,从 t3℃甲、乙、丙的饱和溶液降温到 t2℃时,由于溶液没有量的限制,析出晶体最多的不一定是甲,故A错误;B、将 t2℃50g 丙的饱和溶液加水稀释成溶质质量分数为10%的丙溶液,需要用到的仪器有:烧杯、玻璃棒、量筒(50ml)、胶头滴管,故B正确;C、t2℃乙的饱和溶液中加入固体甲,可以继续溶解固体甲,乙的溶质的质量分数减小,故C错误;D、t3℃时甲、乙、丙溶解度大小关系是甲>乙>丙,t3℃等质量甲、乙、丙的饱和溶液中,含溶剂最多的是丙,故D正确;E、将接近饱和的甲溶液变成甲的饱和溶液,溶质质量分数可能不变,可以采取降温的方法,故E正确。
点睛∶溶解度曲线的意义①表示同一种物质在不同温度时的溶解度或溶解度随温度变化的情况;②表示不同物质在同一温度时的溶解度,可以比较同一温度时,不同物质的溶解度的大小。若两种物质的溶解度曲线相交,则在该温度下两种物质的溶解度相等;③根据溶解度曲线可以确定从饱和溶液中析出晶体或进行混合物分离提纯的方法;④根据溶解度曲线能进行有关的计算。
-
科目: 来源: 题型:
查看答案和解析>>【题目】2017年5月,中国首次海城天然气水合物(可燃冰)试采成功,成为全球第一个稳定开采可燃冰的国家。可燃冰开采困难重重,原因之一是可然冰极不稳定易爆炸,大甲烷气体涌入大气层,会产生比二氧化碳更为严重的温室教应。置换法是开采方法之一,将CO2液化后进入1500米以下的洋面,就会生成二氧化碳水合物沉入海底,因CO2较甲烷易于形成水合物,因而就问能将甲烷水合物中的甲烷分子置换出来。
(1)甲烷属于______(填有机物”或无机物”),其氢元素的质量分数为_____。
(2)甲烷燃烧是将化学能主要转化为_____,甲烷燃料电池则是将化学能转化为_____能。
(3)下列有关说法正确的是______
A.开采可燃冰不会产生环境问题 B.二氧化碳水合物的密度比水小
C.可燃冰比二氧化碳水合物稳定 D.可燃冰是一种前景广阔的清洁燃料
(4)可燃冰的微观构成为46个H2O分子形成8个笼,有6个笼中每个笼容纳了1个CH4分子,余下2个笼每个容纳1个H2O分子,则可燃冰中H2O与CH4的分子数之比是_______。
(5)一定条件下,甲烷与二氧化碳反应是回收处理二氧化碳的一种方法,产物都是常见双(两)原子分子,请写出反应的化学方程式_________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】已知:SiO2不与稀盐酸反应。牙膏中的摩擦剂约占牙膏成分的50%,主要用于增强牙膏对牙齿的摩擦和去污,牙膏摩擦剂一般由CaHPO4、 CaCO3、 Al(OH)3、SiO2中的一种或几种组成。牙膏中只有摩擦剂不溶于水。请回答下列问题:
(1)上述几种物质中属于盐的是CaCO3和______(填化学式);Al(OH)3的名称是_________。
(2)已知某品牌牙膏中的摩擦剂是CaCO3、Al(OH)3和SiO2中的一种或两种,将适量的牙膏溶于水,静置后过滤,向滤渣中加入足量稀盐酸,没有观察到气泡,且有不溶物,则该牙膏中一定不含______,一定含______。
(3)用下图所示装置(夹持仪器略去)测定另一品牌牙膏中碳酸钙的含量。请回答下列问题:
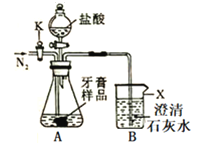
①装置B中仪器X的名称是______。
②装置A中滴加盐酸反应完全后,打开活塞K缓缓通入N2,其作用是_______。
③准确称取5.0g牙膏样品进行实验,测得B中沉淀质量为1.2g。则样品中碳酸钙的质量分数为_______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图所示Ⅰ~Ⅴ装置,可供实验室制取有关气体时选用.
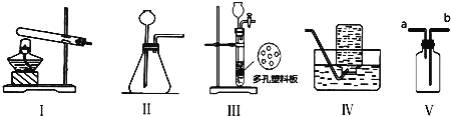
下列有关说法不正确的是( )
A. 实验室制取 CO2 或 O2 可选用Ⅱ、Ⅳ装置
B. 实验室用锌粒和稀硫酸制取 H2 可选用Ⅱ、Ⅳ装置
C. 用氯酸钾制取干燥的氧气可选用Ⅰ、Ⅴ装置,且氧气从 b 端进入
D. 装置Ⅲ与Ⅱ相比,其优点是能控制反应的速率
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组的同学在教师的指导开展如下探究活动.
(一)推断:某白色固体粉末甲可能含有硫酸铜、碳酸钠、氢氧化钠、氯化钠、硫酸钠中的一种或几种, 为探究它们的组成,开展了以下实验.
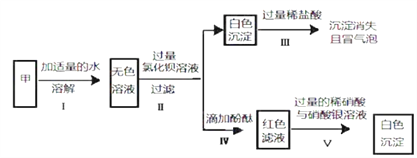
(1)甲加水后形成无色溶液的 pH____7(填“大于”、“小于”或“等于”);
(2)加水形成无色溶液说明固体甲一定不含____;
(3)将上述框图中某试剂稍作改动,可以证实可能有的物质不存在,改动操作及不存在该物质的现象 为____;
(二)除杂:乙溶液中主要含有氯化钠、还含有少量的氯化钙、氯化镁、硫酸钠杂质,现欲提纯氯化钠 开展以下实验.
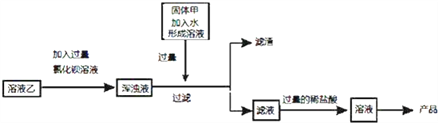
(4)过量稀盐酸的作用是____;
(5)若“过量氯化钡溶液”与“过量固体甲”颠倒位置添加,则最后溶液中含有的溶质一定 是____;
(6)最后得到的产品中所含氯化钠的质量____溶液乙中氯化钠的质量(填“>”“<”或“=”)
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室现有一种含有纯碱、小苏打的固体粉末样品.为了测定其中小苏打的含量,某化学兴趣小组的同学在老师的指导下,利用如下图所示装置(部分固定装置已略去)进行实验.加热条件下,纯碱稳定不分解,小苏打易分解,反应的化学方程式为:2NaHCO3
 Na2CO3+CO2↑+H2O。碱石 灰是 CaO 与 NaOH 的固体混合物;已知,该装置气密性良好,A、C、D 中所装药品足量且能完全吸收 相关物质.探究过程如下:
Na2CO3+CO2↑+H2O。碱石 灰是 CaO 与 NaOH 的固体混合物;已知,该装置气密性良好,A、C、D 中所装药品足量且能完全吸收 相关物质.探究过程如下: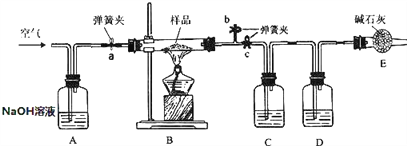
Ⅰ.称量样品和已装入相关药品的 C、D 质量,分别为:m、mC1、,mD1.
Ⅱ.将质量为 m 的样品装入 B 玻璃管中,按图连接好装置,进行操作 X.
Ⅲ.关闭弹簧夹 a、b,打开弹簧夹 c,给玻璃管加热.
Ⅳ.待玻璃管中样品完全反应,打开弹簧夹 a 通入空气,再熄灭酒精灯,直到玻璃管冷却. Ⅴ.再次称量 C、D 的质量,分别为 mC2、mD2.请回答下列问题:
(1)步骤Ⅱ中操作 X 具体为____;
(2)C 中所装药品为____;
(3)D 中发生反应的化学方程式为____;
(4)步骤Ⅳ打开弹簧夹 a 通入空气,再熄灭酒精灯,直到玻璃管冷却的多重作用是____;
(5)依据实验实际,选择实验所得数据,该样品中小苏打含量的表达式为____.
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图能正确反映其对应操作中各量的变化关系的是




A.向等质量的镁和锌中加 入相同的稀盐酸至过量
B.用等质量、等浓度的过氧化氢溶液制取氧气
C.高温煅烧一定质量的石灰石
D.氢氧化钠溶液中浓度加足量的水稀释
A. A B. B C. C D. D
相关试题

