
【题目】(2017石家庄质检二模)甲、乙两个化学学习小组在学习碱的性质时,进行了如图所示的两个实验。
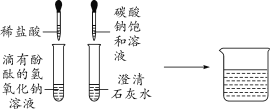
实验1:在滴有酚酞的氢氧化钠溶液中加入稀盐酸,溶液变为无色。
实验2:向氢氧化钙溶液中滴加碳酸钠溶液,反应的化学方程式为____。
实验后,将两支试管中的物质都倾倒到烧杯中,甲小组烧杯中废液为无色澄清溶液,乙小组烧杯中废液为红色。同学们都很好奇,决定对此展开探究。
(提出问题)甲小组烧杯中废液的溶质是什么?(不考虑指示剂)
(查阅资料)氯化钠和氯化钙溶液均呈中性,碳酸钠溶液呈碱性。
(作出猜想)
猜想一 | 猜想二 | 猜想三 |
_____ | NaCl和CaCl2 | NaCl、CaCl2和HCl |
(进行实验)步骤1:取少量甲组烧杯中的废液,向其中逐滴滴加___,当加入一定量该试剂时,废液突然变为红色,此时立刻停止滴加试剂。由此得出,甲组烧杯废液中含有HCl。
步骤2:取少量步骤1中的溶液,继续向其中滴加____,观察到的实验现象是___。由此得出,甲组烧杯废液中含有CaCl2。
根据上述实验,得出结论:猜想三成立。
(交流讨论)小刚认为直接向甲组烧杯中的废液滴加步骤2中所用的试剂,也能验证猜想三成立,应观察到的现象是______。
(拓展应用)同学们用上述探究思路,对乙组烧杯中废液的溶质也进行了分析。小红认为一种可能是NaCl和CaCl2,小燕不同意小红的观点,她的理由是____。
【答案】Ca(OH)2+Na2CO3= CaCO3↓+2NaOH NaCl(或NaCl和HCl) NaOH溶液 Na2CO3溶液(合理即可) 有白色沉淀生成 先有气泡产生,然后有白色沉淀生成 若乙组烧杯废液中只有NaCl和CaCl2两种溶质,烧杯中废液不呈碱性,溶液不会是红色的
【解析】
【作出猜想】稀盐酸和氢氧化钠溶液恰好完全反应,溶质只有反应生成的NaCl,若稀盐酸过量,则溶质为NaCl和HCl【进行实验】步骤1甲组烧杯中的废液不能使无色酚酞变色,所以烧杯中的废液呈中性或酸性,加入一定量试剂后废液突然变红,说明原废液呈酸性,加入的是碱,即NaOH溶液;步骤2是检验CaCl2的存在,应滴加碳酸盐溶液,如滴加Na2CO3溶液,产生白色沉淀,证明有CaCl2。【交流讨论】滴加过量Na2CO3溶液检验盐酸和氯化钙,先有气泡产生,证明有盐酸,后有沉淀产生,证明有氯化钙(注:加入过量的碳酸钠溶液,先和盐酸反应,产生气泡,当盐酸反应完后再和氯化钙反应,产生白色沉淀;化学方程式为Na2CO3+2HCl=== 2NaCl+H2O+CO2↑,Na2CO3+CaCl2=== 2NaCl+CaCO3↓)。【拓展应用】乙烧杯中的废液为红色,说明废液呈碱性,而CaCl2 和NaCl呈中性,因此溶质不可能只是NaCl和CaCl2。


科目:初中化学 来源: 题型:
【题目】利用溶解度曲线,可以获得许多有关物质溶解度的信息。下图是a、b两物质的溶解度曲线。有关叙述正确的是
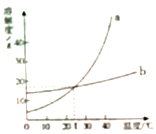
A. a的溶解度大于b的溶解度
B. 当a物质中混有少量b物质时,可以用蒸发结晶的方法除去b
C. 10℃时,取相同质量的a、b两物质分别配成饱和溶液所需水的质量是a大于b
D. 将t℃时a、b的饱和溶液升温至40℃,其溶液中溶质的质量分数为a大于b
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】材料、环境、能源跟生活密切相关.
(1)日常用品尼龙手套、铝壶、不锈钢刀、纯棉桌布中,主要用有机合成材料制成的是_______.
(2)为了减小燃烧化石燃料对环境的影响,人们一方面开发利用清洁高效的新能源,如_________(写一种);另一方面提倡“低碳生活”.下列符合“低碳生活”的做法是______(填数字序号).
①人走灯灭 ②少用一次性筷子 ③多使用空调调节温度
(3)目前氢氧燃料电池已经在宇宙飞船等航天器上实际使用,它能把氢气和氧气反应的化学能转化为___能,氢氧燃料电池内反应的化学方程式是___________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】正确使用和理解化学用语是重要的科学素养。下列说法或书写正确的是
A. KCI03、KCl中氯元素的化合价相同 B. H20、H2S04中均含有氢分子
C. 硫元素显-2价:S2- D. 两个二氧化氮分子:2NO2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分析下图,回答问题。
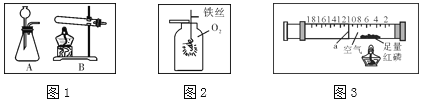
(1)实验室里用二氧化锰和氯酸钾制取氧气时,发生装置可以选用图1中装置____(填字母序号),二氧化锰作该反应的______。
(2)用图2的装置进行铁丝在O2中燃烧的实验,容易导致集气瓶炸裂,为了避免这种情况,应采取的措施是__________________。
(3)如图3所示,红磷用酒精灯加热后才能燃烧,由此可知可燃物燃烧的条件之一是_____________;红磷燃烧后冷却至室温,活塞a停在刻度____(填数字)处。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明在课外阅读中得知:氢氧化铜受热会分解生成氧化铜(Cu(OH)2![]() CuO+X),于是用CuSO4溶液与KOH溶液反应制取氢氧化铜,并对氢氧化铜进行加热。
CuO+X),于是用CuSO4溶液与KOH溶液反应制取氢氧化铜,并对氢氧化铜进行加热。
(1)生成物X的化学式为____。
(2)小明在加热氢氧化铜时,发现蓝色固体先变成黑色,继续高温灼烧黑色固体变成红色,同时有气体产生。为弄清这种红色固体的成分,进行了如下的探究:
(查阅资料)Cu和Cu2O均为红色固体,且Cu2O+H2SO4=Cu+CuSO4+H2O。
(提出猜想)红色固体是:Ⅰ.Cu;Ⅱ.Cu2O;Ⅲ. ____。
(进行实验)
操作 | 现象 | 结论 |
①取灼烧后的红色固体1.44 g于试管中,加入足量稀硫酸,加热并充分振荡,静置 | 溶液由无色变蓝色,固体减少 | 1.44 g红色固体一定有__ |
②过滤、洗涤、干燥 | 得红色固体 |
(结论分析)
①根据上述实验现象,小明认为猜想Ⅲ正确。但有同学认为小明的判断不严谨,因为猜想__也有相同现象。
②氧化铜高温灼烧由黑色变成红色的化学反应方程式为____。
③如要确定1.44 g红色固体成分,还需要补充的操作是__,再通过____得出结论。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(2017雅安)馒头、面包等发面食品的一个特点是面团中有许多小孔,他们使发面食品松软可口。小明学习相关化学知识后,将家里制作馒头用的白色粉末带到实验室与兴趣小组的同学一起进行探究。
(初步探究)取少量白色粉末于试管中,加适量水,测得溶液的pH>7,说明溶液呈________性。
(提出问题)白色粉末成分是什么?
(查阅资料)
(1)碳酸钠、碳酸氢钠都可用于制作发面食品。
(2)碳酸氢钠不稳定,受热易分解生成二氧化碳和水等; 碳酸钠很稳定。
(猜想与假设)
猜想Ⅰ:碳酸钠
猜想Ⅱ:碳酸氢钠
(实验探究)甲乙兴趣小组设计不同实验方案进行探究。
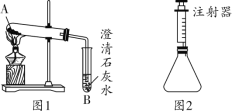
甲组方案:如图,取适量白色粉末于试管中,将导管伸入澄清石灰水,加热,澄清石灰水变浑浊,猜想Ⅱ正确。写出装置B中反应的化学方程式____________。
乙组方案:用如图所示装置作为反应容器,准确测量生成气体的体积以判断白色粉末的成分。
分别向盛有碳酸钠、碳酸氢钠和白色粉末的锥形瓶中,注入等体积、等浓度的足量的稀盐酸,记录如表:
实验编号 | 锥形瓶内物质 | 最终得到CO2体积 /mL | |
名称 | 质量/g | ||
① | 碳酸钠 | a | V1 |
② | 碳酸氢钠 | a | V2 |
③ | 白色粉末 | m | V3 |
实验①的化学反应方程式为______________;表中m=________g;根据上表中数据分析,猜想Ⅱ正确,判断的依据是______________。
(反思应用)
(1)甲组方案中,无法判断白色粉末是否为碳酸钠和碳酸氢钠的混合物;乙组方案可以判断,如果是两者的混合物,应该满足的条件是__________________。
(2)家中制作馒头、面包时,将面粉发酵(产生有机酸),再加入适量的碳酸氢钠,可以使馒头、面包松软。原因是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2017年5月,我国在南海首次试采可燃冰成功。
材料一:可燃冰的化学式为CH4·8H2O,相对分子质量为160,它是由甲烷气体与不在高压低温条件下形成的类冰状水合物。可燃冰热值高、储藏量大。燃烧不产生污染物。
材料二:将CO2注入海底的可燃冰储层,能将可燃冰中的CH4“挤走”,而形成二氧化碳水合物。
回答下列问题:
(1)写出甲烷(CH4) 燃烧的化学方程式__________________________________。
(2)CH4·8H2O碳元素的质量分数为_______________。
(3)下列关于可燃冰的说法正确的是________。
A.可燃冰是一种清洁能源
B.甲烷和水形成可燃冰的过程是化学变化
C.用CO2 “挤走”可燃冰中的CH4过程属于置换反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com