【题目】下列关系曲线不能正确反映其对应变化关系的是( )
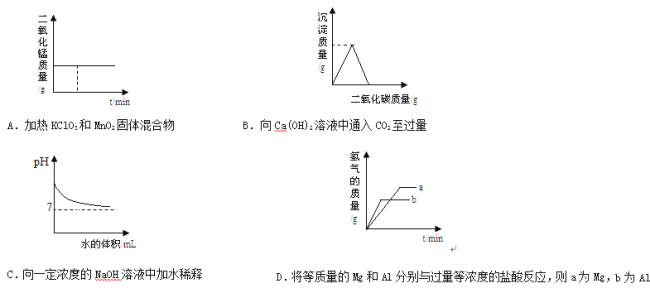
A. A B. B C. C D. D
参考答案:
【答案】D
【解析】
根据催化剂的特点,氢氧化钙、碳酸钙的性质,氢氧化钠碱性,金属与酸反应规律进行分析解答。
A、催化剂能改变化学反应的速率,而本身的质量和化学性质不变。二氧化锰是氯酸钾分解的催化剂,反应后前后质量不变,与图像相符;B、向Ca(OH)2溶液中通入CO2至过量先发生的是氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,氢氧化钙完全反应后,二氧化碳、水、碳酸钙三种物质反应生成易溶于水的碳酸氢钙,所以沉淀的质量减少,最后沉淀消失,与图像相符;C、氢氧化钠溶液呈碱性,溶液的pH大于7,随水的加入溶液碱性变弱,溶液的pH减小,但始终大于7,与图像相符;D、镁的金属活动性大于铝的金属活动性,镁和稀盐酸反应的方程式是Mg + 2HCl ===MgCl2 + H2↑,铝和稀盐酸反应的方程式是2Al + 6HCl === 2AlCl3 + 3H2↑,根据化学方程式可知,每24份质量的镁会生成2份质量的氢气,每18份质量的铝会生成2份质量的氢气,相同质量的镁和铝分别与过量的溶质质量分数相同的稀盐酸反应,生成的氢气质量铝大于镁;相同的条件下,铝的反应速率快,产生氢气速率快,与图像不符。故选D。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在宏观、微观和符号之间建立联系,是化学学科的特点,如图是某化学反应的微观过程示意图(“
 ”表示氧原子,“〇”表示氢原子).
”表示氧原子,“〇”表示氢原子).
(1)从宏观角度看,物质C属于 (选填“混合物”或“纯净物”);
(2)以上变化的基本反应类型是 ;
(3)从微观角度看,物质B是由 构成的(选填“分子”或“原子”或“离子”);
(4)参加反应的A与B的微粒个数比为 .
-
科目: 来源: 题型:
查看答案和解析>>【题目】探究原子结构的奥秘
1808年,英国科学家道尔顿提出了原子论,他认为物质都是由原子直接构成的:原子是一个实心球体,不可再分割.
1897年,英国科学家汤姆生发现原子中存在电子.他认为在原子结构中,电子就像“西瓜子”一样镶嵌在带正电的“西瓜瓤”中.
1911年英国科学家卢瑟福做了一个实验:用一束质量比电子大很多的带正电的高速运动的α粒子轰击金箔,结果是大多数α粒子能穿过金箔且不改变原来的前进方向,但也有一小部分改变了原来的方向,还有极少数的α粒子被反弹了回来.据此他提出了带核的原子结构模型:原子是由原子核和核外电子构成.
请根据以上信息回答下列问题:
(1)科学家对原子结构的探究经历了三个过程,下列(填字母序号,下同)________ 是汤姆森原子结构模型,________ 是卢瑟福原子结构模型;
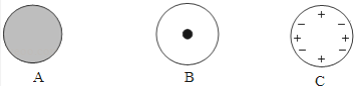
(2)在卢瑟福的实验中,大多数α粒子穿过金箔后方向不变,说明________ ;
A.原子的质量是均匀分布的 B.原子内部绝大部分空间是“空的”
(3)根据卢瑟福的实验所产生的现象,不能够获得的结论是________ ;
A.原子核体积很小 B.原子核质量较大 C.原子核带正电 D.核外电子带负电
(4)通过人类认识原子结构的历史,你对科学的发展有那些感想?(答一点即可)________ .
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列化学方程式与事实不相符的是( )
A. 铝在空气中与氧气反应生成一层致密薄膜4Al+3O2=2Al2O3
B. 铜在稀硝酸中逐渐溶解,放出气体,溶液变为蓝色Cu+2HNO3=Cu(NO3)2+H2↑
C. 胃酸过多病症可以服用含氢氧化铝药物进行缓解Al(OH)3+3HCl=AlCl3+3H2O
D. 人体摄入淀粉后能转换为葡萄糖,葡萄糖经缓慢氧化后变成二氧化碳和水C6H12O6+6O2
 6CO2+6H2O
6CO2+6H2O -
科目: 来源: 题型:
查看答案和解析>>【题目】铝合金是目前广泛使用的合金材料,已知某铝合金由Al、Fe、Cu三种金属构成,为了测定各种金属含量,取12.5g合金样品与盐酸反应,消耗浓盐酸(质量分数36.5%)100g。另取12.5g合金样品与氢氧化钠溶液反应,消耗含氢氧化钠12g的溶液40mL。
已知:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,Fe,Cu均不与氢氧化钠溶液反应。
请问:(1)12.5g样品中含铝多少克?
(2)铜在合金中所占的质量分数是多少?
-
科目: 来源: 题型:
查看答案和解析>>【题目】大庆市某中学化学兴趣小组利用以下装置制备氢气,并验证氢气的性质,按要求回答以下问题:
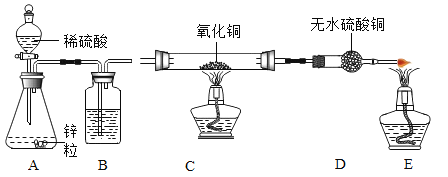
(1)化学实验室现有质量分数为98%的浓硫酸,需配制245g质量分数10%的稀硫酸,配制步骤如下:
①计算:所需质量分数98%的浓硫酸______g;②量取;③稀释量取和稀释浓硫酸所用的玻璃仪器有______________。简要描述浓硫酸的稀释方法___________。
(2)该兴趣小组制备氢气的原理为___________(化学方程式)。
(3)装置B的作用__________________。
(4)下列有关实验操作或现象描述不正确的是(____)
A.实验开始时,应先通入氢气,然后再点燃C处酒精灯
B.点燃C处酒精灯后,D处硫酸铜固体由白色逐渐变为蓝色
C.E处酒精灯的作用是点燃未反应的氢气
D.实验结束时,应先停止通入氢气,然后熄灭C处酒精灯
(5)实验结束后,发现部分氧化铜未被还原,已知反应前氧化铜质量为a克,反应结束后混合固体质量为b克,则被氢气还原的氧化铜的质量为___________g。
-
科目: 来源: 题型:
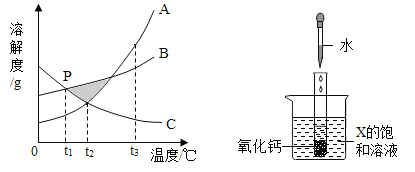
查看答案和解析>>【题目】已知A、B、C三种物质的溶解度曲线如图所示。
(1)在阴影区域部分,处于不饱和状态的是__________(选填“A、B盐酸反应生成、C”)。
(2)若饱和A溶液中含有少量的C,提纯A的方法为______结晶,过滤。
(3)P点表示的含义为_________。
(4)在t1℃下,B、C的饱和溶液升温至t2℃,所得溶液溶质的质量分数大小关系为_______。
(5)向试管中滴入2mL水后,若X中有固体析出,则X为______(选填“A、B、C”)。
相关试题

