【题目】下列化学方程式与事实不相符的是( )
A. 铝在空气中与氧气反应生成一层致密薄膜4Al+3O2=2Al2O3
B. 铜在稀硝酸中逐渐溶解,放出气体,溶液变为蓝色Cu+2HNO3=Cu(NO3)2+H2↑
C. 胃酸过多病症可以服用含氢氧化铝药物进行缓解Al(OH)3+3HCl=AlCl3+3H2O
D. 人体摄入淀粉后能转换为葡萄糖,葡萄糖经缓慢氧化后变成二氧化碳和水C6H12O6+6O2![]() 6CO2+6H2O
6CO2+6H2O
参考答案:
【答案】B
【解析】A、铝常温下和空气中的氧气反应,生成致密的氧化铝薄膜,反应的化学方程式为:4Al+3O2=2Al2O3,故相符;B、铜和硝酸反应生成气体是一氧化氮,反应的化学方程式为: 3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,故不相符;C、氢氧化铝是碱能与酸发生中和反应,用于治疗胃酸过多,反应的化学方程式为:Al(OH)3+3HCl=AlCl3+3H2O,故相符;D、淀粉在人体内消化成葡萄糖,葡萄糖经缓慢氧化后变成二氧化碳和水,反应的化学方程式为:C6H12O6+6O2![]() 6CO2+6H2O,故相符;故选:B。
6CO2+6H2O,故相符;故选:B。
-
科目: 来源: 题型:
查看答案和解析>>【题目】科学探究是重要的学习方式,假设和验证是探究过程的重要环节。为了探究“铁丝可以在纯净的氧气中燃烧”,同学们将一根火柴梗塞入一段螺旋状“铁丝”(可能是纯铁铁丝或含碳铁丝)末端,将它固定,用镊子夹住“铁丝”,然后将火柴在酒精灯上点燃,将“铁丝”由集气瓶口向下慢慢伸入,观察现象:
(1)甲同学只发现铁丝红热了一下,就没有观察到其他现象了,请你分析铁丝没有燃烧的可能原因是__________________________________________(只答一条)。
(2)乙同学发现“铁丝”在纯氧中燃烧起来,观察到火星四射,并有黑色固体生成,请写出该反应的化学反应式:_____________________。
(3)为了找出“铁丝”在纯氧中燃烧“火星四射”的原因,根据现有实验用品:纯铁细铁丝、含碳细铁丝、镁条、集气瓶装的几瓶纯氧气、酒精灯、火柴、镊子等,你提出的假设和验证方法有:
①假设1:_________________。验证方法是_________________。
②假设2:________________。验证方法是________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某同学为了研究竹子里面气体的成分,做了一个实验。
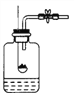
(1)他先将竹子浸在水里,钻个小孔,看到一串串气泡冒出,然后采用_______法(填实验室常用的一种集气方法)收集到了甲、乙两瓶气体。
(2)将放有足量红磷的燃烧匙伸入甲瓶中(如图所示),用放大镜聚焦,使红磷燃烧,瓶内充满了白烟一冷却至室温后,将甲瓶倒放在水中,松开夹子,结果流入的水约占甲瓶容积的1/10。这说明竹子里的气体中肯定含有_______。
(3)再往乙瓶中倒入一些澄清石灰水,发现石灰水马上变浑浊。这说明竹子里的气体中肯定含有_______。
(4)那么竹子里的气体含量与空气有什么区别呢?于是,他又用空气重复了上述实验。相比较后得出的结论是____________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列关系曲线不能正确反映其对应变化关系的是( )
A.
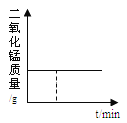 加热KClO3和MnO2固体混合物
加热KClO3和MnO2固体混合物B.
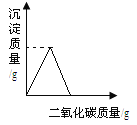 向Ca(OH)2溶液中通入CO2至过量
向Ca(OH)2溶液中通入CO2至过量C.
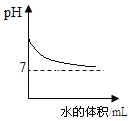 向一定浓度的NaOH溶液中加水稀释
向一定浓度的NaOH溶液中加水稀释D.
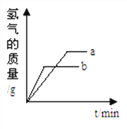 将等质量的Mg和Al分别与过量等浓度的盐酸反应,则a为Mg,b为Al
将等质量的Mg和Al分别与过量等浓度的盐酸反应,则a为Mg,b为Al -
科目: 来源: 题型:
查看答案和解析>>【题目】大庆市某中学化学兴趣小组利用以下装置制备氢气,并验证氢气的性质,按要求回答以下问题:
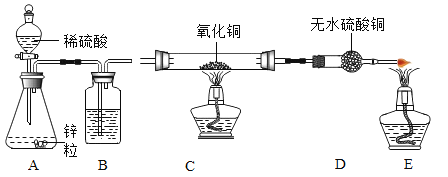
(1)化学实验室现有质量分数为98%的浓硫酸,需配制245g质量分数10%的稀硫酸,配制步骤如下:
①计算:所需质量分数98%的浓硫酸______g;②量取;③稀释量取和稀释浓硫酸所用的玻璃仪器有______________。简要描述浓硫酸的稀释方法___________。
(2)该兴趣小组制备氢气的原理为___________(化学方程式)。
(3)装置B的作用__________________。
(4)下列有关实验操作或现象描述不正确的是(____)
A.实验开始时,应先通入氢气,然后再点燃C处酒精灯
B.点燃C处酒精灯后,D处硫酸铜固体由白色逐渐变为蓝色
C.E处酒精灯的作用是点燃未反应的氢气
D.实验结束时,应先停止通入氢气,然后熄灭C处酒精灯
(5)实验结束后,发现部分氧化铜未被还原,已知反应前氧化铜质量为a克,反应结束后混合固体质量为b克,则被氢气还原的氧化铜的质量为___________g。
-
科目: 来源: 题型:
查看答案和解析>>【题目】A~J均为初中常见化学物质:它们之间的转化关系如图所示,部分产物已省略。已知A是人体胃酸的主要成分,B是由四种元素组成的盐类,C是一切生命生存所必须的物质,E是厨房重要的调味品。请回答下列问题:
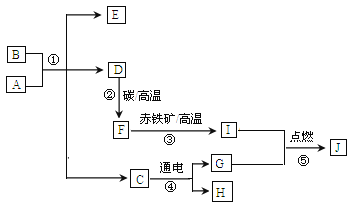
(1)物质F____________,H_________(用化学式表示)。
(2)A和B反应的化学方程式为_____________。
(3)①~⑤属于分解反应的是________________。
(4)A和J反应可生成两种不同盐类,两者所含元素种类相同,但其比例不同,则A何J反应的化学方程式为_______________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】铝合金是目前广泛使用的合金材料,已知某铝合金由Al、Fe、Cu三种金属构成,为了测定各种金属含量,取12.5g合金样品与盐酸反应,消耗浓盐酸(质量分数36.5%)100g。另取12.5g合金样品与氢氧化钠溶液反应,消耗含氢氧化钠12g的溶液40mL。
已知:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,Fe,Cu均不与氢氧化钠溶液反应。
请问:(1)12.5g样品中含铝多少克?
(2)铜在合金中所占的质量分数是多少?
相关试题

