【题目】如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是
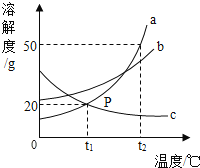
A. t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>c
B. t2℃时,将50ga物质(不含结晶水)放入100g水中充分溶解得到a的饱和溶液
C. 将t2℃时,a、b、c三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系是b>a=c
D. 将c的饱和溶液变为不饱和溶液,可采用降温的方法
参考答案:
【答案】C
【解析】
试题分析:A、t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>c,由图可知,正确;
B、t2℃时,a的溶解度为50g,即100g水溶解50ga得到a的饱和溶液,正确;
C、AB的溶解度随温度降低而减小,C的溶解度随温度的降低而增大,所以分别将三种物质的饱和溶液从50℃将至20℃时,AB析出晶体,依然是饱和溶液,此时B的溶解度大于A,C变为不饱和溶液,溶质的质量分数与降温前相等,20℃时A的溶解度与C的溶解度相等,根据饱和溶液中溶质的质量分数的计算式 溶解度/(溶解度+100g) ×100%可知:降温后所得溶液溶质质量分数大小关系是B>A>C,故错误;
D、降温c的溶解度降低,因此可以通过降温的方法将c的饱和溶液变为不饱和溶液,正确;
-
科目: 来源: 题型:
查看答案和解析>>【题目】卤水中含有MgCl2、KCl和MgSO4等物质,下图是它们的溶解度曲线。完成下列填空。
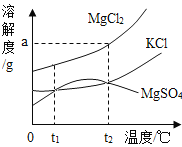
(1)在t1℃时,向100 g水中加入150 g MgCl2,形成 (填“饱和”或“不饱和”)溶液,将其温度升高到t2℃时,此时溶液中溶质的质量分数为 。
(2)t1℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液中,溶质质量分数最大的是 。将t2℃时MgCl2、KCl和MgSO4三种物质的饱和溶液降温至t1℃时,可能会析出的晶体有 (填字母序号)。
A.MgCl2和KCl
B.只有MgSO4
C.MgCl2、KCl和MgSO4
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质之间不能发生化学反应的是
A.石灰水与稀盐酸 B.铜与硝酸银溶液
C.银与稀硫酸 D.二氧化碳与水
-
科目: 来源: 题型:
查看答案和解析>>【题目】某班同学用氧化钠溶液和稀盐酸进行中和反应实验。

(1)甲同学实验操作如图:在烧杯中加入约5mL氢氧化钠溶液,滴入几滴无色酚酞溶液,此时溶液呈_____色.再用滴管滴入一定量的稀盐酸,再用玻璃棒搅拌,发现溶液为无色,于是甲同学得出两者恰好中和的结论,反应的化学方程式为_____________.
(2)乙同学对甲同学的结论提出了质凝,并对反应后溶液中的溶质成分进行探究.
【实验探究】
反应后溶液中的溶质是什么?
猜想一:只有NaCl
猜想二:NaCl和HCl
猜想三:NaCl和NaOH
以上猜想中,你觉得不合理的是 .
为了验证另外两种猜想,乙同学设计如下实验方案:
实验操作
实验现象
实验结论
取少量反应后的溶液于试管中滴入Na2CO3溶液
_______________
猜想二成立
【反思交流】
实验结束后,废液处理方法正确的是 (填序号).
A.倒入下水道 B.倒入废液缸 C.带出实验室.
-
科目: 来源: 题型:
查看答案和解析>>【题目】“微观﹣宏观﹣符号”三重表征是化学独特的表示物质及其变化的方法.请结合图示完成下列问题:

(1)图1中,“Cu”表示多种信息,如表示铜元素、金属铜单质,还能表示______________;
(2)从微粒的角度说明图2反应的实质是____________________;
(3)为减少温室气体排放,人们积极寻找不含碳元素的燃料.经研究发现NH3燃烧的产物没有污染.且释放大量能量,有一定应用前景.其反应的微观示意图如图3:

该反应的化学方程式为________________,其基本反应类型属于______________.
-
科目: 来源: 题型:
查看答案和解析>>【题目】锂电池是一种新型的高能电池,质量轻、容量大,颇受手机、电脑等用户的青睐。某种锂电池的总反应式可表示为:Li十MnO2═LiMnO2下列说法错误的是
A.该反应前后锂元素的化合价发生了变化
B.MnO2中Mn的化合价为+4价
C.LiMnO2属于氧化物
D.该反应属于化合反应
-
科目: 来源: 题型:
查看答案和解析>>【题目】图中A~E是操作化学常见的物质,已知A和E都可以作燃料,其中A是天然气的主要成分,请分析回答:

(1)反应①的化学方程式为_____________________;
(2)反应②中的产物B通常用_____________检验;
(3)E物质作燃料的优点是________________(答一条即可).
相关试题

