【题目】化学用语是学习化学的主要工具,是国际通用的化学语言。请你用适当化学用语填空。
(1)保持水化学性质的最小粒子____________;
(2)2个硫酸根离子 _______;
(3)标出氧化镁中镁元素的化合价__________;
(4)2个亚铁离子____________
(5)氖气___; 两个氢氧根离子_______;氯化钠中的阴离子______;4个二氧化硫分子 ____
参考答案:
【答案】H2O; ![]() ;
; ![]() ;
; ![]() ; Ne; 2OH-; Cl-; 4SO2
; Ne; 2OH-; Cl-; 4SO2
【解析】
(1)保持水的化学性质的最小粒子是水分子,1个水分子含有2个氢原子和1个氧原子,化学式中元素符号右下角的数字表示分子中原子的个数。因此水的化学式表示为:H2O;
(2)每个硫酸根离子含有1个硫原子和4个氧原子且带有2个单位的负电荷,化学式中元素符号右下角的数字表示分子中原子的个数,元素符号右上角的数字表示离子所带的电荷数,且数字在前(是“1”时省略)、正负号在后。若表示多个该离子,就在其符号前加上相应的数字。因此2个硫酸根离子表示为:![]() ;
;
(3)氧化镁中氧元素显-2价,则镁元素显+2价;由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故氧化镁中镁元素的化合价可表示为:![]() ;
;
(4)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其离子符号前加上相应的数字,故2个亚铁离子可表示为:![]() ;
;
(5)氖气属于稀有气体单质,是直接用元素符号表示其化学式的,故其化学式为:Ne;标在离子符号前面的数字表示离子的个数,故2个氢氧根离子表示为:2OH-;氯化钠中的阴离子是氯离子,其离子符号为:Cl-;标在化学式前面的数字表示分子的个数,故4个二氧化硫分子表示为:4SO2。
-
科目: 来源: 题型:
查看答案和解析>>【题目】人类文明进步与金属材料的发展关系十分密切,金属在生活生产中有着非常广泛的应用。请回答下列问题:
(一)金属的广泛应用
(1)“共享单车”是指在公共场所提供共享服务的自行车,符合“低碳出行”理念,颇受年轻人的喜爱。车上的钢丝网篓属于_____混合(填“纯净物”或“混合物”);
(2)2017年5月5日我国首架试飞成功的大型客机C919使用了多种新材料,其中有锂铝合金,在飞机制造中使用该材料说明其具有的特点有____(填序号)。
①硬度大 ②密度小 ③易导电 ④耐腐蚀
(3)如图为生活中常见“暖贴”的部分标签。暖贴可以贴于身体的某个部位,自行发热,用于取
暖或热敷。使用时空气进入暖贴,空气中的氧气、水蒸气与暖贴中的____铁发生反应而使暖贴放热。使用后,发现暖贴内有物质变为红色,该红色固体主要成分的化学式为_____。

(二)设计对比实验探究铁的化学性质
如图实验是大小形状相同的Mg、Zn、Fe、Cu四种金属同时投入到盐酸中发生的现象,金属周围的黑点表示生成的气体。下列结论不正确的是____。(填字母 )

A.铜不能发生置换反应
B.四种金属中金属活动性位于第三的是Fe
C.等质量的锌和铁分别与足量的盐酸反应生成气体质量:Fe比Zn少
(三)炼铁过程的探究
在化学实验室里,可以利用如图装置制得铁:

(1)A处玻璃管内所发生反应的化学方程式是______,该反应中的还原剂是_____。
(2)装置B中的实验现象是通CO2____________。
(3)C处酒精灯的作用是____________。
(四)定量计算
某化工厂产生的废液中含有硫酸亚铁和硫酸铜(不考虑其它物质 ),为回收铜和硫酸亚铁,研究人员设计出“用铁处理”的方案。取100g上述废液,向其中加入2.8 g铁粉,恰好完全反应,测得反应后溶液中溶质的质量分数为15%。求:
(1)回收得到铜的质量为________g。
(2)回收得到硫酸亚铁的质量是________。(写出计算过程,结果保留小数点后一位)
-
科目: 来源: 题型:
查看答案和解析>>【题目】今年暑假,巴厘岛蓝色可乐汽水风靡全国。下图是该可乐汽水配料表的部分内容,请完成下列问题。
蓝色百事可乐汽水
(配料)碳酸水、白砂糖、磷酸、柠檬酸、柠檬酸钠、食用香精、咖啡因、苯甲酸钠、阿拉伯胶、亮蓝、诱惑红
(净含量)450mL
(营养成分表)
项目
每100毫升
能量
190千焦
蛋白质
0克
脂肪
0克
碳水化合物
11.5克
钠
8毫克
蓝色百事可乐汽水
(配料)碳酸水、白砂糖、磷酸、柠檬酸、柠檬酸钠、食用香精、咖啡因、苯甲酸钠、阿拉伯胶、亮蓝、诱惑红
(净含量)450mL
(营养成分表)
项目
每100毫升
能量
190千焦
蛋白质
0克
脂肪
0克
碳水化合物
11.5克
钠
8毫克
(1)据分析,碳酸水是由二氧化碳溶于水形成的,请写出此反应的化学式表达式_________。
(2)该瓶可乐中含有钠元素________g(精确到0.001g)。
(3)配料表中的苯甲酸钠起防腐作用,其化学式为C7H5O2Na,试计算:
①Mr(C7H5O2Na)=________。
②苯甲酸钠中碳元素、氧元素的质量比为________。
③14.4g苯甲酸钠中含有多少克钠元素________?
-
科目: 来源: 题型:
查看答案和解析>>【题目】采用适当的试剂,可从石灰石 (主要成分是CaCO3 )中获得高纯度CaCO3,其流程如下:(流程中的杂质不溶于水也不与酸反应 )
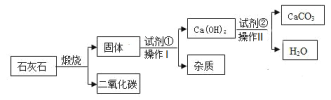
(1)流程图中进行的操作I的名称是____,该操作的温度要求控制在相对____(填“较高”或“较低” )的环境下进行,才能更好地提高提纯效率。
(2)石灰石煅烧反应的基本反应类型是_______。
(3)该流程图所示物质中,溶于水放出大量热的氧化物是_____(填“化学式” )。
(4)使原料中各原子的利用率尽可能达到 100%是“绿色化学”的核心理念之一。上述流程中有的物质可以再利用,该流程中可再利用的物质是 ___和____(填“化学式”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在用白磷(白磷与红磷组成相同,着火点为40℃)探究质量守恒定律的实验中,晓涵同学将橡皮塞上的细玻璃管下端放到酒精灯火焰上灼烧至红热后,迅速用橡皮塞将锥形瓶塞紧,并引燃白磷,实验过程如下图所示。请回答下列问题:

(1)此实验能否不用气球,改为直接用橡皮塞使锥形瓶密封?且说明理由____________
(2)实验中观察到气球先变大后变小,用理化知识解释产生此现象的原因是____________
(3)该同学联想到以前测定氧气体积分数时也用到红磷,且当时红磷必须过量,请解释原因。________。经过分析该同学认为上述探究质量守恒定律的实验中红磷也应过量,你认为她的观点正确吗?并加以解释____________________
(4)上述探究质量守恒定律的实验后,该同学为了验证锥形瓶内是否还有氧气剩余,用如下方法:打开瓶塞,用燃着的木条伸入锥形瓶,发现木条继续燃烧,说明瓶内还有少量氧气剩余。请你评价其实验方法正确与否,并解释:____________________
-
科目: 来源: 题型:
查看答案和解析>>【题目】某研究性学习小组想探究“能使带火星木条复燃的氧气的最低体积分数是多少?”每个同学分别收集多瓶不同体积分数的氧气进行实验。
(1)甲同学想收集体积分数为50%的氧气,他向容量为250毫升集气瓶内装入125毫升水,然后用如图所示的向上排空气法收集,他能否收集体积分数为50%的氧气________,(填“能”、“否”)因为____________________
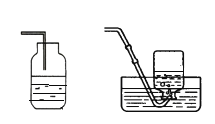
(2)乙同学也想收集体积分数为50%的氧气,他向容量为250毫升集气瓶内装入125毫升水用如图排水法收集。能否收集体积分数为50%的氧气________(填“能”“否”)因为____________
(3)丙同学想收集一瓶体积分数为20%的氧气实验,你觉得有无必要,____________(填“有”“无”),因为________________
(4)丁同学收集了一瓶体积分数为40%的氧气发现并没使带火星木条复燃,又收集了一瓶体积分数为 60%的氧气发现使带火星木条复燃了,你觉得他下一步实验应该做什么____________
(5)戊同学用250毫升集气瓶用排水法收集体积分数为50%的氧气应如何操作____________________________
-
科目: 来源: 题型:
查看答案和解析>>【题目】亚硒酸钠(Na2SeO3)可用于提升人体免疫力,硒元素在元素周期表中的部分信息及原子结构示意图如图所示,下列说法正确的是( )

A.Na2SeO3中Se的化合价为+3 B.Se是一种金属元素
C.n的值为6 D.Se相对原子质量为78.96g
相关试题

