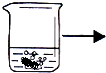
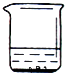
【题目】黄铜是铜和锌组成的合金.现取某黄铜样品40g,请根据如图所示实验过程和数据进行有关计算.
实验步骤 | ①将黄铜样品和过量稀盐酸加入烧杯中并称重 | ②待反应完全后,称重 |
实验图示 |
|
|
实验数据 | 烧杯、样品和稀盐酸的质量共为200.0g | 烧杯和其中混合物的质量为199.6g |
(1)反应产生氢气的质量是g.
(2)黄铜样品中铜的质量分数(计算结果精确到0.1%).
参考答案:
【答案】
(1)0.4g
(2)解:设黄铜样品中含锌的质量为x
Zn+2HCl═ZnCl2+ | H2↑ |
65 | 2 |
x | 0.4g |
![]() =
= ![]()
x=13g
样品中铜的质量是40﹣13=27g,
样品中铜的质量分数为: ![]() ×100%=67.5%
×100%=67.5%
答:黄铜样品中铜的质量分数为67.5%
【解析】(1)反应产生氢气的质量是:200g﹣199.6g=0.4g;
根据质量守恒定律,反应前后总质量不变,故反应后剩余固体的质量+生成气体的质量=200,则生成气体的质量=200-199.6=0.4。依据金属活动性顺序,铜不能和酸反应,锌能和酸反应生成氢气,故0.4g氢气完全是由锌和稀盐酸反应生成的。所以可利用化学方程式计算求出锌的质量,从而再求出铜的质量。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列食物中属于碱性食物的是( )
食物
苹果
葡萄
牛奶
豆浆
pH
2.9~3.3
3.5~4.5
6.3~6.6
7.4~7.9
A.苹果B.葡萄C.牛奶D.豆浆
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列化学用语书写正确的是( )
A.五氧化二磷:P2O2B.亚铁离子:Fe2-
C.2个钾原子:2KD.3个氮分子:N3
-
科目: 来源: 题型:
查看答案和解析>>【题目】马英同学取某地石灰石样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如下表所示:
加入稀盐酸的质量/g
生成气体的总质量/g
第1次
20
1.1
第2次
20
2.2
第3次
20
m
第4次
20
4.4
第5次
20
4.4
(1)m的值为_________g
(2)12g石灰石样品中碳酸钙的质量等于_________g
(3)反应完全后最终溶液中氯化钙的质量分数为_______?(写出计算过程,计算结果精确至0.1)
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列制作过程中的变化属于化学变化的是( )
A.粮食酿酒B.酒精挥发C.铁水铸锅D.麦磨成面
-
科目: 来源: 题型:
查看答案和解析>>【题目】豆浆已成为众多家庭的饮品。下表是豆浆中部分营养成分的平均质量分数。请根据下表回答:
成分
蛋白质
油脂
糖类
钙
铁
维生素
质量分数/%
1.8
0.7
1.1
0.01
0.0005
0.015
(1)豆浆中含有人体所需的微量元素是___,青少年因缺___而导致佝偻。
(2)豆浆所含的营养素中不能供给人体能量,但可以起到调节新陈代谢作用的是____(填序号)
A 蛋白质 B 油脂 C 糖类 D 维生素
-
科目: 来源: 题型:
查看答案和解析>>【题目】请结合下列实验常用装置,回答有关问题.
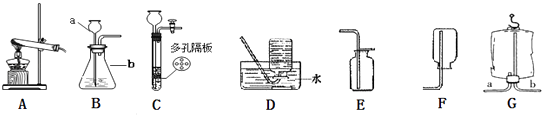
(1)写出图中标有字母的仪器名称:a、b .
(2)若用高锰酸钾制取氧气,应选择的发生装置是(填字母,下同) , 反应的化学方程式是 . 用排水法收集完氧气,应先将导管移出水面,然后再停止加热,主要是防止 .
(3)若用石灰石和稀盐酸来制取二氧化碳,可选用B或C作为发生装置,这两种装置相比,C装置优点是 . 该反应的化学方程式为 .
(4)甲烷是密度小于空气,极难溶于水的气体.实验室用加热醋酸钠固体和碱石灰固体混合物的方法来制取.制取甲烷应选用的发生装置是 , 若要收集较纯的甲烷,可选择D、E、F中的 . 若用图G所示医用塑料袋排空气法收集甲烷,则甲烷进入端为(填“a”或“b”) .
相关试题