【题目】硝酸钾是实验室常见的一种试剂。
(1)硝酸钾是由___和___构成的(填写微粒符号)。
(2)硝酸钾中钾元素的质量分数是__________(结果用百分数表示,保留到0.1%)。
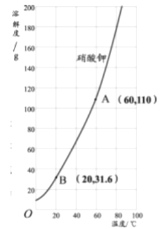
(3)右图是硝酸钾的溶解度曲线,由图可以总结出硝酸钾的溶解度随温度变化的趋势是_________。60℃时110g硝酸钾溶于100g水中形成的溶液是____(选填“饱和“或“不饱和”)溶液,将此时配得的溶液降温至20℃,析出硝酸钾晶体的质量是___g。
(4)列式计算:用100g10%的硝酸钾溶液配制5%的硝酸钾溶液。需要加水多少亳升____?(水的密度为1.0g·mL-1)
参考答案:
【答案】K+;NO3-38.6%随着温度的升高硝酸钾的溶解度逐渐增大饱和78.4100mL
【解析】
(1)硝酸钾由钾离子和硝酸根离子构成;(2)根据元素的质量分数公式计算;(3)结合硝酸钾的溶解度曲线图分析;(4)根据稀释前后溶质的质量不变分析。
(1)硝酸钾是由K+和NO3构成的;
(2)硝酸钾中钾元素的质量分数是![]() ×100%≈38.6%;
×100%≈38.6%;
(3)通过分析硝酸钾的溶解度曲线,可以总结出硝酸钾的溶解度随温度变化的趋势是:硝酸钾的溶解度受温度变化影响较大,60℃时,硝酸钾的溶解度是110g,所以110g硝酸钾溶于100g水中形成的溶液是饱和溶液,将此时配得的溶液降温至20℃,硝酸钾的溶解度是31.6g,所以析出硝酸钾晶体的质量是110g-31.6g=78.4g;
(4)用100g 10%的硝酸钾溶液配制5%的硝酸钾溶液,需要加水![]() -100g=100g,体积为100g÷1g/mL=100mL。
-100g=100g,体积为100g÷1g/mL=100mL。
-
科目: 来源: 题型:
查看答案和解析>>【题目】请根据图中实验装置回答下列问题。
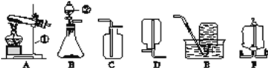
(1)写出标号仪器的名称:①________,②____________。
(2)用A、E组合制取氧气,有关反应的文字表达式为______________;
A装置中试管口通常放一团棉花,在该实验中的作用是____________________,能用装置E收集氧气的原因是____________,在气体收集完毕后,接下来的操作是______________。
(3)实验室也可以用装置B制取氧气,锥形瓶内放入的固体物质通常是________,该物质在该实验中的作用是________,有关反应的文字表达式为____________。写出利用该装置制取氧气的一个优点:__________。
(4)某同学利用空塑料输液袋(如图F)收集氧气,验满氧气时,把带火星的火柴放在玻璃管________(填“a”或“b”)端,如果木条复燃,则说明收集满了。
(5)请再写一个实验室制取氧气的文字表达式:____________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】一定质量的某有机化合物完全燃烧,生成2.2gCO2和1.8gH2O,另取3.2g该有机化合物在O2中完全燃烧,消耗4.8gO2,该有机化合物的化学式可能是
A. C2H4 B. CH4O C. CH4 D. C2H4O
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下列反应事实写出相应的化学方程式。
(1)稀硫酸与锌粒反应制氢气:___________,
(2)金属铝与氧气反应生成氧化膜:________________;
(3)碳酸钙在高温下分解:________________;
(4)石灰水与硫酸铜溶液反应:________________;
(5)甲烷在足量氧气中充分燃烧:________________;
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学是一门以实验为基础的科学,化学实验和科学探究离不开实验装置。
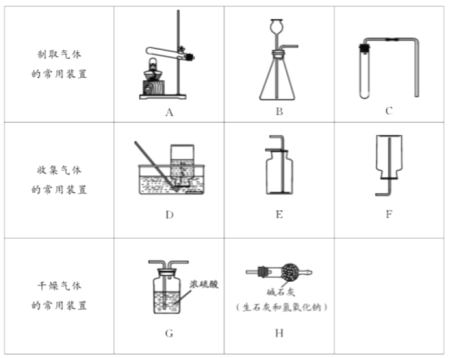
(1)制取气体实验时,首先要对发生的装置进行气密性检查,确保装置不漏气,装置C气密性检查的方法是______。
(2)收集某种气体的方法,主要取决于这种气体的性质,装置E所示的收集方法是____,被收集的气体密度_______空气密度(选填“>”,“<”,“=”)。
(3)实验室用大理石与稀盐酸制取并收集一瓶干燥的二氧化碳,所选装置正确的连接顺序是______→______→______(填装置编号)。
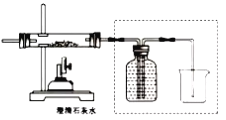
(4)下图所示一氧化碳与氧化铁的反应装置中,虚线方框内装置的作用有________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】从大理石(主要杂质是氧化铁)中提纯碳酸钙的一种实验流程如下:
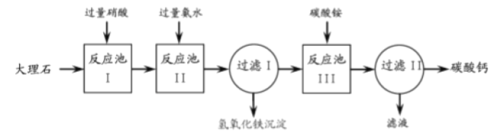
(1)反应池I中用硝酸不用稀硫酸的主要原因是______________。
(2)反应池II中加入氨水的目的是______________。
(3)反应池III用生成碳酸钙的化学方程式是______________。
(4)过滤II中所得滤液在农业生产中的一种用途是______________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(1)控制变量,设计对比实验是实验探究的重要方法。
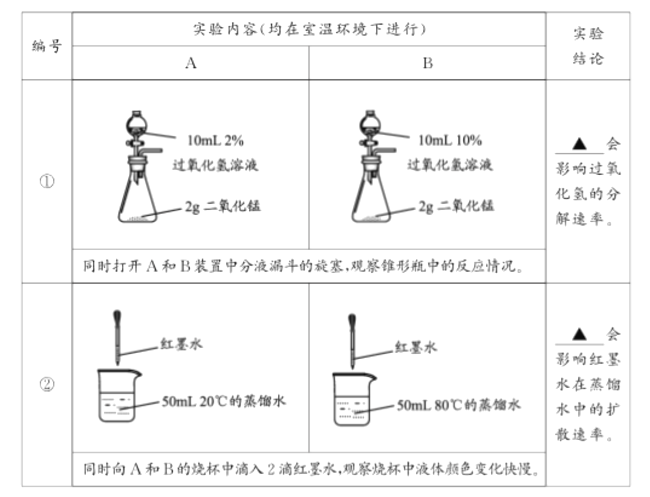
_______、_______
(2)观察是学习化学的重要方法。
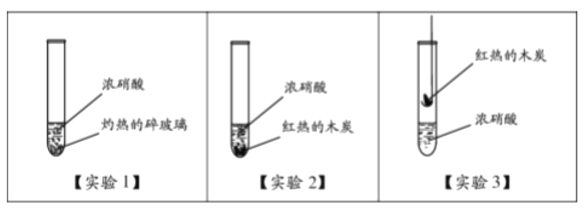
研究小组进行如下实验,发现均有红棕色二氧化氮气体产生。
查阅资料:4HNO3
 O2↑+4NO2↑+2H2O
O2↑+4NO2↑+2H2OC+4HNO3(浓)
 CO2↑+4NO2↑+2H2O
CO2↑+4NO2↑+2H2O①(实验1)中所用碎玻璃与浓硝酸不发生化学反应,灼热的碎玻璃在实验中起到的作用是_______。
②(实验2)中有红棕色气体产生,能否证明(实验2)中木炭与浓硝酸发生了反应?请做出判断,并说明理由:________。
③(实验3)中发现红热的木炭表面有红棕色气体产生,且生成的气体产物中检测出二氧化碳(体积分数大于0.03%),能否证明(实验3)中木炭与浓硝酸发生了反应?请做出判断,并说明理由:______。
相关试题

