【题目】氯化钙在生活中常用作干燥剂、融雪剂,在工业上可用于制造防冻液等。某工厂以石灰石为原料生产氯化钙晶体的流程如下。原料石灰石中含有杂质主要是MgCO3、MgSO4 和Al2O3。
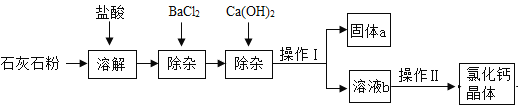
⑴石灰石粉溶解时,Al2O3发生反应的化学方程式为________________。
⑵加入BaCl2除去的杂质离子是____________(填离子符号);
⑶操作Ⅰ的名称为____________,需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、____________。操作Ⅱ的具体步骤为:____________、冷却结晶。
⑷固体a的成分一定含有________________________(只写一种)。检验溶液b的酸碱性,如果显碱性,还需加入适量的____________ (填化学式)提高产品纯度。
参考答案:
【答案】 ![]() SO42- 过滤 玻璃棒 蒸发浓缩 硫酸钡(或氢氧化镁;或氢氧化铝) HCl
SO42- 过滤 玻璃棒 蒸发浓缩 硫酸钡(或氢氧化镁;或氢氧化铝) HCl
【解析】本题考查了酸、碱、盐的性质和混合物的分离。
(1)氧化铝与盐酸反应生成氯化铝和水,化学方程式为Al2O3+6HCl=2AlCl3+3H2O;
(2)氯化钡能与溶液中的硫酸镁反应生成硫酸钡沉淀和氯化镁,因此,除去的杂质离子为SO42-;
(3)操作Ⅰ将固体与液体分离,方法为过滤,过滤用到的玻璃仪器有铁架台(带铁圈)、漏斗、烧杯、玻璃棒;为了提高结晶的效率,在结晶前对溶液应作蒸发浓缩处理。操作Ⅱ的具体步骤为蒸发浓缩、冷却结晶;
(4)氯化钡能与硫酸镁反应生成硫酸钡和氯化镁,氢氧化钙能与溶液中氯化镁、氯化铝反应生成氢氧化镁沉淀、氢氧化铝沉淀和氯化钙,固体a的成分一定含有硫酸钡(或氢氧化镁;或氢氧化铝);如果滤液显碱性,是操作中加入的氢氧化钙过量,可加入适量的HCl与氢氧化钙反应生成氯化钙和水,除去氢氧化钙而得到较为纯净的氯化钙,提高产品纯度。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下表是氯化钠和硝酸钾在不同温度时的溶解度,根据此表回答
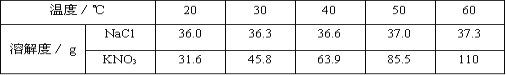
(1)60℃时,氯化钠的溶解度为 g。
(2)在30℃时,100g水中加入50g硝酸钾,充分搅拌后得到的溶液质量为 g。
(3)欲从海水中获得氯化钠晶体,应采取 方法。
(4)由表中数据分析可知,硝酸钾和氯化钠在某一温度时具有相同的溶解度x,则x的取值范围是 g。
-
科目: 来源: 题型:
查看答案和解析>>【题目】“探险队员”——硫酸,走进了有许多“食人兽”(即能与硫酸发生反应的物质)的小山,请你帮助它安全地走出小山。
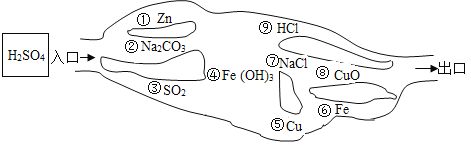
⑴请用图中物质前的序号连接起来表示所走的路线:
入口→____________→____________→____________→____________→出口。
⑵小山中潜伏着一种红褐色的“食人兽”,若硫酸遇上,发生的反应方程式为: __________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】物质王国举行一场趣味篮球赛。某队由五名“队员”组成:铁、二氧化碳、稀硫酸、氢氧化钙、氯化铜。比赛中,由氯化铜“队员”发球,“队员”间传接球,最后由D位置“队员”投篮进球完成有效进攻,传接球“队员”间物质必须能相互反应,场上“队员”位置及传球路线如图。已知D位置上投篮的“队员”是个灭火“能手”。请回答:
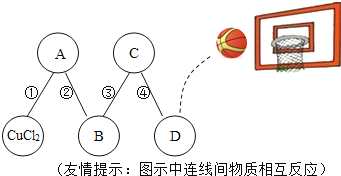
⑴D所代表物质的化学式是____________。
⑵图中反应②的化学方程式____________。图中反应④的化学方程式________________。
⑶图中反应③所属的基本反应类型是____________反应。
⑷为实现“快速进攻”,氯化铜除传球给A位置“队员”外,还能直接传球的另一名“队员”是________(填物质名称)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(本题的所有夹持仪器均已省略)请根据下图回答问题:
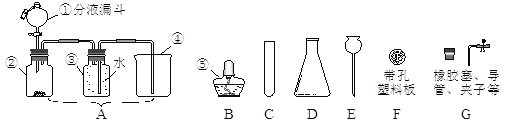
⑴ 图中仪器⑤的名称:⑤____________。
⑵ 实验室制取氧气,周颖同学设计了图A的装置,并用仪器③收集氧气。其中,仪器①中盛放的试剂名称应为_________,此法生成氧气的化学方程式为________________,收集氧气的方法为___________。
⑶ 实验室制取二氧化碳,从B~G中选择仪器,组装发生装置,要求能方便控制反应的发生或停止,你的选择为__________(填字母),反应的化学方程式为__________________。若用下图装置进行“排空气法”收集制取的CO2,请把图中的“导气管”补画完整。
 ________________
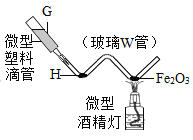
________________⑷ 下图是氢气还原氧化铁的微型实验装置图。其中“微型塑料滴管”的作用相当于上图A实验装置中的____________(填仪器编号);用微型仪器进行实验,具有的优点是___________________(写1点)。
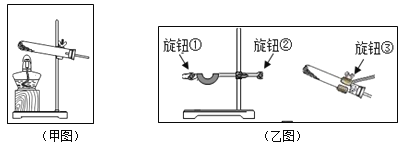
⑸ 如下甲图是周颖同学组装的另一套制O2装置,但她发现试管固定得太高,此时她应调节乙图中的旋钮____________(填①或②或③)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】兴趣小组同学为了弄清即将维修的沼气池中气体的成分,进行了有关实验。请你与他们一起完成以下探究活动:
【收集气体】将不加盖的矿泉水瓶装满水,用细绳吊入池中,再用木棍拨动使瓶中的水全部倒出(见图),然后迅速拉起矿泉水瓶,盖上瓶盖。

这种方法属于____________集气法。
【对气体猜想】猜想Ⅰ:全部是CH4; 猜想Ⅱ:全部是CO;
猜想Ⅲ:全部是CO2; 猜想Ⅳ:是CH4和CO2的混合气体。
【实验和推断】

⑴若“现象a”为石灰水变浑浊,则说明气体中含有_____气体。
⑵步骤②的目的是____________________________________;步骤③“注水装置”应选下图中的____________(填序号)。

⑶若“现象b”为杯壁有水雾出现,有同学认为“猜想Ⅰ或Ⅳ”成立,其反应方程式为:____________; 另有同学认为此现象不能证明收集到的气体中一定含有氢元素,理由是_______________;要排除这种干扰可采取的措施是______________________________。
⑷ 采取⑶中的排除干扰措施后:若“现象a、b”为无明显现象,“现象c”为石灰水变浑浊,则证明“猜想_________”成立;若“现象a、c”均为石灰水变浑浊,“现象b”为杯壁有水雾,则证明“猜想__________”成立。
-
科目: 来源: 题型:
查看答案和解析>>【题目】我国女科学家屠呦呦获2015年诺贝尔生理学或医学奖。她最初的发现,让青蒿素(化学式:C15H22O5)成为世界卫生组织推荐的一线抗疟药,挽救了全球数百万人的生命。而下图是某厂生产的青蒿素的说明书部分内容。
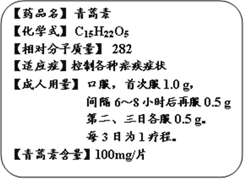
⑴青蒿素属于____________化合物(填“有机”或“无机”)
⑵青蒿素含有____________种元素;碳、氧的原子个数比为____________(填最简比)。
⑶青蒿素中氢元素的质量分数是_________(精确到0.1%)。
⑷用青蒿素控制疟疾症状一般以三天为1个疗程。根据图中说明,一个成人疟疾患者在一个疗程中共需服该药物____片。
相关试题

