【题目】质量守恒定律的发现对化学的发展作出了巨大贡献。
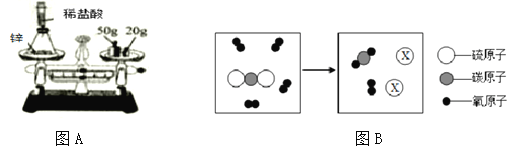
(1)为验证质量守恒定律,小华设计如上图所示装置进行实验。
实验时,先将装有药品的装置放在天平上,添加砝码,移动游码至2.6g,天平平衡(如上图A所示)。然后取下装置,用针筒向锥形瓶中注入少量稀盐酸,反应后再将装置放置于天平上,观察到总质量为__________g,从而验证了质量守恒定律,反应的化学方程式为___________________,若将锥形瓶改为烧杯,则不能验证质量守恒定律,原因是__________________。
(2)某反应的微观示意图,如图B所示。
①X的化学式是_______。
②从微观角度分析, 在化学反应前后一定不变的是____________(选填序号)。
a原子种类 b分子种类 c元素质量 d分子质量 e分子数目
参考答案:
【答案】 72.6 Zn+2HCl=ZnCl2+H2↑ 装置没有密闭或气体逸出了 SO2 a
【解析】(1)化学反应遵守质量守恒定律,故反应后再将装置放置于天平上,观察到的总质量为:50g+20g+2.6g=72.6g,验证质量守恒定律的实验,有气体参加或生成时,要在密闭装置中进行。(2)①根据反应的微观示意图,该反应是:CS2+3O2== CO2+2X,化学反应前后各种原子个数相等,2X中含有2S、4O,故X的化学式为SO2 ②化学反应的实质是原子的重新结合,故在化学变化中,分子种类发生了改变,分子质量和分子数目不能确定原子种类不变,而元素是一个宏观概念,故从微观角度分析,在化学反应前后一定不变的是原子种类。
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验是进行科学探究的重要方式,请根据下图回答问题:
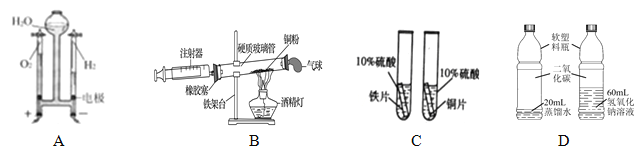
(1)A实验证明水是由_______________组成的。
(2)B实验过程中要反复推拉注射器的活塞,原因是____________________。
(3)C实验从金属活动性的角度获得的结论是__________________________。
(4)D实验是小鹏同学设计的对比实验,用于证明二氧化碳和氢氧化钠能否反应。小燕同学认为该实验设计不符合对比实验的基本原则,她的理由是______________________ 。
-
科目: 来源: 题型:
查看答案和解析>>【题目】“共享单车”是指在公共场所提供共享服务的自行车,由于符合“低碳出行”的理念,颇受年轻人的喜爱。
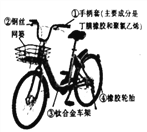
(1)“低碳出行”中“低碳”指的是较低的______气体排放;
(2)如图所示自行车中的材料属于金属材料的是______(选填一个序号);
(3)铁车架的表面刷油漆能防止锈蚀,其原因是__________;
(4)扫描二维码可以租用“共享单车”,二维码的制作材料一般是用PVC不干胶贴纸。PVC[化学式(C2H3 Cl)n]中碳元素和氢元素的质量比为_________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】元素家族新成员——鉨(
 )
)2016年6月8日,国际纯粹与应用化学联合会正式发布113号等四种新元素的英文名称和元素符号。2017年5月9日,我国发布了这四种元素的中文名称。其中113号元素的元素符号为Nh,中文名称为“鉨”。图1中,甲为鉨原子结构示意图,乙为铝原子结构示意图。请回答下列问题;
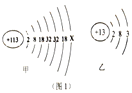
(1)甲中x=________。
(2)鉨元素的原子与铝元素的原子具有相同的_____________数。
(3)在化学反应中,鉨原子形成离子的符号为___________。
(4)根据鉨和铝的结构,理论上鉨的金属活动性比铝强,试预测鉨可能与哪些物质反应? ________,________。(写出两种不同类别的物质的化学式即可)
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是实验室制取气体的部分装置,请根据实验装置(部分固定装置已省略)回答问题:
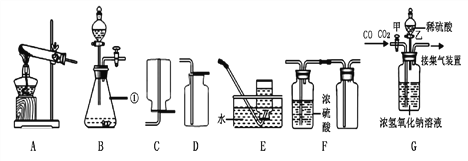
(1)图中标识①仪器的名称是________
(2)实验室既可以制取CO2,又可以制取O2的发生和收集装置组合为:________(在A—E中选),用该装置制取CO2的化学方程式为:__________________________________
(3)若用F装置收集一瓶干燥的某气体,则该气体可能是________(填字母代号)。
A. NH3 B. H2 C. O2 D.CH4
(4)工业上常需分离CO和CO2的混合气体。某同学采用装置G也能达到分离该混合气体的目的,操作步骤如下:
①关闭活塞乙,打开活塞甲,通入混合气体,可收集到________气体(填化学式);②然后,_____________(填操作),又可收集到另一种气体。
-
科目: 来源: 题型:
查看答案和解析>>【题目】我国每年报废的手机超过1亿部。废旧手机的电路板中含有铝、铁、铜、银、金等多种金属,随意丢弃既会造成资源浪费,也会污染土壤和水体。化学兴趣小组为回收其中的铜,设计并进行了如下实验。

已知:Cu+H2O2+H2SO4=CuSO4+2H2O;不考虑金、银发生类似反应。
(1)将电路板粉碎成粉末的目的是_____________。
(2)步骤①所得滤液中的溶质除硫酸外,还有_________________。(用化学式填空)
(3)步骤②中的实验现象是:固体部分溶解,________________。
(4)步骤④中反应的化学方程式是_______________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】归纳总结是学习化学的重要方法,某化学兴趣小组学习碱的性质后,通过实验对氢氧化钙的化学性质进行了验证和总结,如图所示-——表示物质两两之间能发生化学反应。请根据如图,回答问题。(已知:CaCl2溶液呈中性,CaCl2+Na2CO3═CaCO3↓+2NaCl)


(1)甲同学将酚酞试液滴入氢氧化钙溶液中,观察到溶液变红,得出结论:氢氧化钙溶液呈_________________(填“酸性、碱性或中性”)。
(2)乙同学将过量的稀盐酸加入到甲同学所得溶液中,观察到的现象是________________,此时含有的溶质有________(酸碱指示剂除外)(用化学式填空,下同)。
(3)为验证乙同学所得溶液中含有的溶质,可取少量反应后的溶液滴加过量的____________溶液(填一种物质的化学式),产生_______________________________现象,则证明存在。
相关试题

