【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示。请回答:
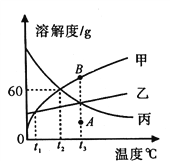
(1)0℃时,三种物质中溶解度最大的是________。
(2)t2℃时,在盛有50g水的烧杯中加入35g甲物质,充分搅拌后所得溶液的质量是_______g。
(3)将t3℃的甲、乙、丙三种物质的饱和溶液降温到t1℃时,所得溶液中溶质的质量分数关系为____________________(用“=”“<”或“>”符号连接)。
(4)将甲溶液由A点转变为B点,可采用的方法是_______(填一种即可)。
(5)如图,将放有固体X的试管放入烧杯中,然后向试管内加入液体Y,一段时间后丙溶液中有固体析出,则对应的X和Y物质是__________(填序号)。
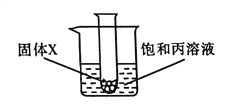
A.氯化钠和水
B.镁条和稀盐酸
C.硝酸铵和水
D.氢氧化钠和水
参考答案:
【答案】 丙 80 丙> 乙= 甲 增加溶质或蒸发溶剂 BD
【解析】(1)根据溶解度曲线解答;
(2)根据t2℃时甲物质的溶解度解答;
(3)根据三种物质的溶解度随温度变化情况及饱和溶液中溶质质量分数的计算式分析解答;
(4)根据不饱和溶液转化为饱和溶液的方法解答;
(5)根据丙物质的溶解度随温度的升高而减小解答。
解:(1)由溶解度曲线可知,0℃时,三种物质中溶解度最大的是丙;
(2)t2℃时甲物质的溶解度是60g。即在100g水中最多溶解60g甲物质。那么在50g水中最多溶解30g甲物质。故t2℃时,在盛有50g水的烧杯中加入35g甲物质,充分搅拌后所得溶液的质量是80g;
(3)据图可知:甲、乙的溶解度随温度的升高而增大,且甲物质受温度的影响变化较大,丙的溶解度随温度的升高而减小;所以将t3℃时甲、乙、丙三种物质的饱和溶液降温到t1℃时,甲、乙有晶体析出,而t1℃时甲、乙溶解度相等。此时甲、乙溶质质量分数相等。丙无晶体析出,溶质质量分数不变。据饱和时质量分数的计算式![]() ×100%,可知溶解度越大质量分数也就越大,t3℃时丙物质溶质质量分数大于t1℃时甲、乙溶质质量分数。故所得溶液中溶质的质量分数关系为丙> 乙= 甲;
×100%,可知溶解度越大质量分数也就越大,t3℃时丙物质溶质质量分数大于t1℃时甲、乙溶质质量分数。故所得溶液中溶质的质量分数关系为丙> 乙= 甲;
(4)将甲溶液由A点转变为B点,是将不饱和溶液转化为饱和溶液,可采用的方法是增加溶质或蒸发溶剂;
(5)由于丙物质的溶解度随温度的升高而减小。由题意可知,一段时间后丙溶液中有固体析出,说明此时溶液温度升高,丙物质溶解度减小。进而说明固体X与Y混合后放出热量。A中氯化钠和水温度不变;B中镁条和稀盐酸反应温度升高,符号要求;C中硝酸铵遇水温度降低;D中氢氧化钠溶于水温度升高,符号要求。故填:BD。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列有关物质用途的叙述错误的是
A.明矾可用于净水 B.一氧化碳可用于灭火
C.液氧可用于火箭助燃剂 D.稀硫酸可用于除铁锈
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列描述属于化学变化的是
A. 立竿见影 B. 木已成舟 C. 风起云涌 D. 钢铁生锈
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列做法不正确的是
A. 塑料回收,节能环保 B. 杀菌消毒,高温煮沸
C. 油锅着火,锅盖盖灭 D. 燃气泄漏,明火查看
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列物质的归类正确的是
选项
甲
乙
A
无机材料
陶瓷、玻璃、青铜
B
同一物质
烧碱、纯碱、苛性钠
C
提供能量营养物
淀粉、蛋白质、无机盐
D
常见干燥剂
浓硫酸、生石灰、石灰石
A. A B. B C. C D. D
-
科目: 来源: 题型:
查看答案和解析>>【题目】A—J都是初中化学常用的物质。其中B、E、H、J是单质,其余均为化合物,气体C可用于灭火。它们相互间的转化关系如下图所示(部分反应物、生成物及反应条件已略去)。
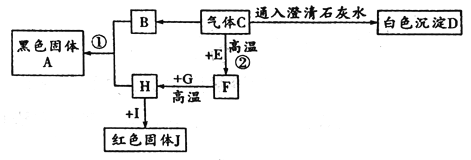
请回答下列问题:
⑴写出物质D、J的化学式:D____________,J____________。
⑵“气体C→B”的转化过程,在自然界中称为________________作用。
⑶反应①的反应条件______________,其基本反应类型________________。
⑷写出反应②的化学方程式:______________________________________。
⑸若要实现“H+I→红色固体J”的转化,物质I必须满足的条件是_________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化学兴趣小组的同学对实验室制取CO2及相关性质进行一系列的探究活动。
(1)气体制取。
按如图1所示的制取装置进行实验。
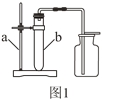
①写出有标号仪器的名称:a __________,b ___________。
②实验室制取CO2的反应化学方程式是______________________________。
③实验室收集CO2的方法是________________________________________,
原因是_____________________________________________。
(2)实验探究。
[提出问题] 实验室制取CO2时能否采用排水法收集?
[设计实验]
实验一:向一个充满CO2气体的质地较软的塑料瓶中加入约1/3体积的水,立即旋紧瓶盖,用力摇晃塑料瓶。可观察到塑料瓶 ________________________,说明CO2能溶于水。
实验二:先用集气瓶装满一瓶蒸馏水(pH=7.0),然后按如图2所示组装装置并进行实验,再用pH计测定从装置C排到烧杯中的液体的pH。
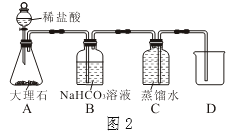
测得烧杯中液体的pH<7.0,说明溶液呈酸性,原因是 _____________________。
[实验结论] 实验室制取CO2不宜采用排水法收集。
[拓展延伸] 某同学先对图2装置做了以下改进:将装置C中的部分蒸馏水换成植物油,将烧杯换成量筒(如图3所示)。然后利用改进后的装置测定收集到CO2的体积,测得气体的实际体积小于理论值,原因可能是:①__________,② ___________。

相关试题

