【题目】(1)化学用语是国际通用语言。请用化学用语填空:
①氮元素__________;②3 个乙醇分子____________;
③氢氧根离子_______________;④SO2 中硫 元素的化合价为+4____________________;
(2)经过近一年的学习,我们已能定量研究一些化学反应。如表达式为 a+b→c+d 的 化 学反应就接触过很多,请你写出符合下列要求的化学方程式:
①参加反应的 a 和 b 的 质 量 比 为 1:1 的化学方程式为_________________。
②参加反应的 a 和 b 的 质 量 比 为 1:2 的化学方程式为______________________。
③参加反应的 a 和 b 的 质 量 比 为 1:4 的化学方程式为___________________________。
④参加反应的 a 和 b 的 质 量 比 为 1:10 的化学方程式为____________________________________。
参考答案:
【答案】 N 3C2H5OH OH- ![]() H2SO4+Cu(OH)2=CuSO4+2H2O CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
H2SO4+Cu(OH)2=CuSO4+2H2O CuSO4+2NaOH=Na2SO4+Cu(OH)2↓ ![]() 2Al+3Fe(NO3)2=2Al(NO3)3+3Fe
2Al+3Fe(NO3)2=2Al(NO3)3+3Fe
【解析】(1)①氮元素的元素符号为:N;
②分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,所以3个乙醇分子可表示为:3C2H5OH;
③离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.故氢氧根离子可表示为:OH-;
④元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以SO2中硫元素的化合价为+4,故可表示为![]() ;
;
(2)①硫酸与氢氧化铜反应生成硫酸铜和水,符合题意,反应的化学方程式为:H2SO4+Cu(OH)2=CuSO4+2H2O;
②硫酸铜与氢氧化钠反应生成硫酸钠和氢氧化铜,符合题意,反应的化学方程式为:CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;
③甲烷与氧气反应生成二氧化碳和水,符合题意,反应的化学方程式为:CH4+2O2 ![]() CO2+2H2O;
CO2+2H2O;
④铝与硝酸铁反应生成硝酸铝和铁,符合题意,反应的化学方程式为:2Al+3Fe(NO3)2=2Al(NO3)3+3Fe。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在碱性溶液中能大量共存,并且为无色透明溶液的是( )
A. Na+、K+、MnO4-、SO42- B. NH4+、Na+、NO3-、Cl-
C. K+、Ba2+、NO3-、Cl- D. Mg2+、Fe3+、Cl-、NO3-
-
科目: 来源: 题型:
查看答案和解析>>【题目】诗句是民族灿烂文化的瑰宝,下列著名诗句描述的全为物理变化的是( )
A. 野火烧不尽,春风吹又生 B. 白玉为床,金作马
C. 粉身碎骨浑不怕,要留清白在人间 D. 春蚕到死丝方尽,蜡炬成灰泪始干
-
科目: 来源: 题型:
查看答案和解析>>【题目】在等质量的稀硫酸中分别投入 Mg、Al、Fe 的粉末,完全溶解后,溶液质量仍相等。则 投入的金属质量关系是 ( )
A. Mg>Al>Fe B. Al>Mg>Fe C. Fe>Mg>Al D. Mg=Al=Fe
-
科目: 来源: 题型:
查看答案和解析>>【题目】(1)生命的孕育和维系需要水,人类的日常生活和工农业生产离不开水。
①下列“水”中,属于纯净物的是____________(填序号);
a.海水 b.河水 c.蒸馏水 d.井水
②水在通电条件下分解的化学方程式为_________________________。
③生活中可用活性炭净水器来净水,是利用了活性炭的____________性。活 性炭不能将硬水软化, 生活中可用____________的方法降低水的硬度。
(2)化学就在我们身边,它与我们的生产、生活息息相关。现有干冰、熟石灰、钛合金三 种物质。请选择适当的物质填空。
①可用于人工降雨是的_________;
②可用于制造人造骨的是______________;
③可用于改良酸 性土壤的是_______________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(1)实验室制得的二氧化碳中常含有水蒸气和少量酸 雾,为了获得纯净的二氧化碳可选用下图中的 套装置来净化。
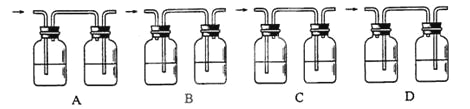
其中左瓶中应盛 ;右瓶中应盛 。
(2)向氢氧化钠溶液中通入适量二氧化碳后,仅使溶液中 5O%的氢氧化钠反应,反应后溶液中 CO32—和 OH—的个数比为 。
(3)现将石灰石样品 15g 与 105.4g 稀盐酸放入烧杯中充分反应(杂质不溶于水也不与稀 盐酸反应),反应时间与反应前后烧杯内物质的质量变化如下表所示:
反应时间/s
20
40
60
80
100
120
质量/g
119.52
118.64
117.76
116.88
116
116
请计算回答:①样品中碳酸钙的质量分数。(计算结果保留 1 位小数)
② 反应后所得溶液中溶质的质量分数。
-
科目: 来源: 题型:
查看答案和解析>>【题目】工业上用纯碱和石灰石为原料制备烧碱的简要工艺流程如下图所示,请回答。
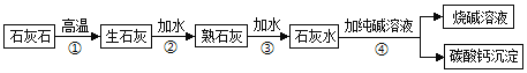
(1)石灰石、生石灰、熟石灰均能与下列___________(填字母)发生化学反应。
A.水 B.盐酸 C.二氧化碳
(2)上述工艺流程中没有涉及的化学反应的基本类型是___________。
(3)某研究性学习小组的同学想检验上述工艺中的烧碱溶液里是否含有纯碱,甲同学选择了 一种酸溶液,乙同学选择了一种碱溶液,丙同学选择了一种盐溶液,他们都能达到检验目的。 你认为丙同学所选溶液中的溶质可能是_____________________(填一种物质的化学式)。
(4)步骤④中检验碳酸钙沉淀已洗涤干净的方法是________________________。
相关试题

