【题目】分类、类比是同学们学习化学获取知识的重要科学方法。
(1)氧化反应在生活中随处可见,下面是常见的氧化反应:
|
|
|
|
A动植物呼吸 | B生活火灾 | C金属锈蚀 | D火药爆炸 |
请你将上述氧化反应平均分成两组,其中一组是__________;比较B和D,图D发生的现象除了具备B中条件外,还必须具备的另一个条件是________________。
(2)在元素周期表中,C与Si所处的位置及结构如图
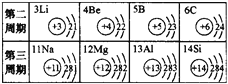
已知二氧化碳与氢氧化钠溶液反应如下
CO2+2NaOH=Na2CO3+H2O
装有氢氧化钠溶液的细口瓶,瓶口磨砂后暴露出SiO2,请你写出二氧化硅与氢氧化钠溶液的反应方程式为_________________,生成物是玻璃胶的成分,因此装有氢氧化钠溶液的细口瓶应用__________塞。
参考答案:
【答案】 AC(BD) 有限的空间 SiO2 + 2NaOH = Na2SiO3 + H2O 胶(塞)
【解析】(1).物质与氧气的反应属于氧化反应;AB都是反应速率非常慢的氧化反应,叫缓慢氧化;BD都是燃烧,是剧烈的氧化反应,是可燃物与氧气充分接触发生的发光放热的剧烈的氧化反应。爆炸的条件是,可燃物与氧气充分混合并且含量达到可燃物的爆炸极限、燃烧发生在有限的空间;(2)二氧化硅与二氧化碳物质类别相同,其中碳和硅的化合价都是+4价,所以二氧化硅与氢氧化钠发生的反应类似于二氧化碳与氢氧化钠的反应。反应方程式为SiO2 + 2NaOH = Na2SiO3 + H2O ;由于硅酸钠是玻璃胶的主要成分,如果试剂瓶的塞子用玻璃塞则会将瓶塞和试剂瓶粘贴在一起,所以应用橡胶塞塞瓶子。
-
科目: 来源: 题型:
查看答案和解析>>【题目】韩国三星在Note7上第一次用到了铝合金做外壳,并使机壳超薄。不过,这样的外观设计却最终断送了Note7的前程,使手机充电时过热,发生燃烧而爆炸现象。
试回答:
(1)锂电池的使用是利用______能和______能的转化过程。
(2)三星Note 7使用铝合金,所利用了铝合金的优点是____(多选题)
A.光泽好、密度小 B.强度大、耐腐蚀性好 C.导电性好
(3)在高温的条件下,铝合金中的铝也会燃烧,反应的化学方程式为_________________;
(4)锂电池使用的阳极材料是钴酸锂,其化学式为LiCoO2已知锂的原子结构示意图为
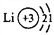 则钴元素的化合价是________价
则钴元素的化合价是________价 -
科目: 来源: 题型:
查看答案和解析>>【题目】在古代江西上饶,人们发现一苦泉,其溶质为X,用赤铁矿A冶炼出的金属B放入其中,发现金属B变红,且上述物质与HCl、H2SO4有如下反应和转化关系(其中“—”连接的两种物质能反应,“→”某物质在一定条件下能转化为另一物质)。试回答:
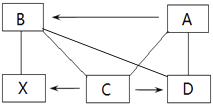
(1)用化学式表示:苦泉中溶质X是________;C为________;
(2)B和C反应的现象是____________________;
(3)写出工业上用A和气体反应冶炼出B的化学方程式为_________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】同学们想知道X、Y两种金属的活动性强弱,他把两种金属放入硫酸铜溶液中,发现在Y的表面有红色物质生成, X没有任何变化,你认为下列推断合理的是: ( )
A. X>Cu>Y B. Y>Cu>X C. Cu>X>Y D. Y>X>Cu
-
科目: 来源: 题型:
查看答案和解析>>【题目】三毛在实验室中做实验时,通过测定某物质中只含有一种元素,因此对该物质作了以下推断,你帮他选择一下哪种说法是正确的
A.该物质可能是单质 B.该物质一定是混合物
C.该物质一定不是化合物 D.该物质一定是纯净物
-
科目: 来源: 题型:
查看答案和解析>>【题目】学习化学过程中有许多“不同”.下列对“不同”的分析错误的是( )
A.CO与CO2性质不同﹣﹣分子构成不同
B.铁丝与铜丝化学性质不同﹣﹣构成的原子不同
C.金刚石与石墨性质不同﹣﹣由不同碳原子构成
D.O2急救病人而O3则不能﹣﹣性质不同
-
科目: 来源: 题型:
查看答案和解析>>【题目】为了测定石灰石中碳酸钙的质量分数,将石灰石粉碎,取粉末10 g,放入烧杯中,做如下实验(假设石灰石样品中杂质不与稀盐酸反应,也不溶于水),请回答下列问题:

(1)配制100 g质量分数为7.3%的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是_______;
(2)写出碳酸钙发生反应的化学方程式为__________________;
(3)设碳酸钙质量为x,写出求解10g石灰石粉末中碳酸钙质量的比例式为____________;则石灰石中碳酸钙质量分数为_________。
(4)将所得的固液混合物过滤,并将滤液蒸发2.8g水(不考虑HCl蒸发),发现无晶体析出,则此时滤液中氯化钙的质量分数是______。
相关试题





