【题目】某校化学兴趣小组的同学根据实验室提供的仪器和药品,在老师的指导下从下图中选择 装置进行了氧气的制备实验。
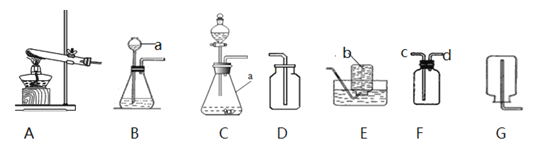
(1)仪器a的名称_______
(2)甲同学选择过氧化氢溶液和二氧化锰制取氧气,为获得平稳的氧气流并收集一瓶较纯净的氧气,完成该实验应选用的装置 _________(填字母)。写出发生反应的化学方程式______。
(3)乙同学称取一定质量高锰酸钾放在大试管中,将温度控制在 250℃加热制取氧气, 实验结束时,乙同学发现收集到的氧气大于理论产量,针对这一现象,同学们进行了如下探究:
(提出猜想)猜想 1:反应生成的二氧化锰分解放出氧气;
猜想 2:反应生成的锰酸钾分解放出氧气。
(实验验证)同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的二氧化锰于试管中,在 250℃条件下加热一段时间,冷却 后测得二氧化锰的质量不变。则猜想 1_____(选填“正确”或“错误”)。
②第二组同学取锰酸钾于试管中在 250℃条件下加热,没有用测定质量的方法得出了猜想 2 正确的结论。该组同学选择的实验方法是________。
(4)丙同学在实验中发现氯酸钾固体加热制取氧气的反应速率很慢,但如果将高锰酸钾固体与氯酸钾固体混合加热,则氯酸钾的分解速率大大加快,该学生认为高锰酸钾在氯酸钾的分解反应中可以作催化剂。你同意他的看法吗?______(选填“同意”或“不同意”),理由是_______
参考答案:
【答案】长颈漏斗 CE 2H2O2 ![]() 2H2O+O2↑ 错误 把带火星的木条放在试管口,木条复燃 不同意 高锰酸钾在反应前后质量和化学性质改变或高锰酸钾分解生成的二氧化锰对氯酸钾的分解起催化作用
2H2O+O2↑ 错误 把带火星的木条放在试管口,木条复燃 不同意 高锰酸钾在反应前后质量和化学性质改变或高锰酸钾分解生成的二氧化锰对氯酸钾的分解起催化作用
【解析】
(1)仪器a的名称长颈漏斗;
(2)分液漏斗可以控制液体的滴加速率,从而控制反应速率,甲同学选择过氧化氢溶液和二氧化锰制取氧气,要获得平稳的氧气流应控制生成氧气的速率,所以应选择装置C,氧气的密度比空气的大,可以用向上排空气法收集,氧气不易溶于水,可用排水法收集,收集一瓶较纯净的氧气应选择排水法,完成该实验应选用的装置为CE,发生反应的化学方程式2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(3)【实验验证】
①第一组同学取一定质量的二氧化锰于试管中,在 250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变,说明二氧化锰没有进一步发生反应,则猜想1错误;
②取锰酸钾于试管中,在250℃条件下加热,把带火星的木条放在试管口,木条复燃,说明有氧气生成;
(4)丙同学在实验中发现氯酸钾固体加热制取氧气的反应速率很慢,但如果将高锰酸钾固体与氯酸钾固体混合加热,则氯酸钾的分解速率大大加快,该学生认为高锰酸钾在氯酸钾的分解反应中可以作催化剂。不同意他的看法,理由是高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰、氧气,生成的二氧化锰是氯酸钾分解的催化剂。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在宏观、微观和符号之间建立联系是化学学科的特点。
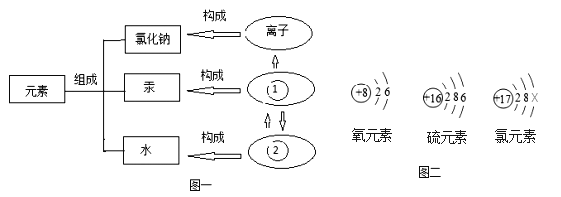
(1)物质的组成及构成关系如图一所示,图中①表示的是_______,②表示的是_______。
(2)下列说法正确的是_______(填字母)。
A.氯化氢是由氢、氯两种元素组成
B.氯化氢是由氢气和氯气混合而成
C.氯化氢是由一个氢原子和一个氯原子构成
(3)如图二所示是氧、硫、氯三种元素的原子结构示意图。
①氯原子结构示意图中X的数值是_______,
②氧和硫两种元素的化学性质具有相似性的原因是它们的原子的_________相同。
-
科目: 来源: 题型:
查看答案和解析>>【题目】水是人类生活中不可缺少的物质。
(1)下列净水方法中,净水程度最高的是_____
A.过滤B.煮沸C.蒸馏 D.吸附
(2)自来水厂常用二氧化氯(ClO2)消毒,其中氯元素的化合价为________。
(3)小花同学设计了电解水简易装置,其中A、B电极由金属曲别针制成。通电后的现象如图所示,则与A电极直接相连的是电源的_____极。该实验常常在水中加入少量稀硫酸或氢氧化钠,目的是_____。
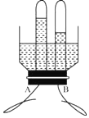
(4)电解水的化学方程式为________。
(5)使用硬水会给生活和生产带来许多麻烦,区分硬水与软水的方法是分别加入________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙、丙三种物质是初中常见的化学物质,甲、乙都是化合物,丙是单质。甲、乙都含有相同的两种元素。它们之间有如图所示转化关系。(“→”表示转化,部分反应物和生成物已略去)
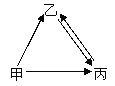
(1)甲的物质名称为:________,请写出丙的一种用途________;
(2)请写出丙转化为乙化学方程式:________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】某同学加热33g氯酸钾和二氧化锰混合物制氧气,至混合物质量不再减少时得到23.4g固体,则
(1)生成氧气的质量为_________
(2)反应前混合物中二氧化锰质量分数计算的表达式为___________
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图为钛(Ti)元素在周期表中的信息,从中获得的信息正确的是

A. 属于非金属元素 B. 原子核内中子数为22
C. 原子核外有22个电子 D. 相对原子质量为47.87g
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是氧化汞受热分解的微观变化过程示意图(“○”表示汞原子,“●”表示氧原子),由图分析得到的结论中错误的是
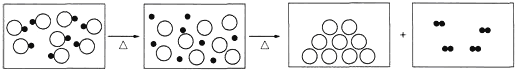
A. 所有分解反应的产物一定是单质 B. 原子是化学变化中最小的粒子
C. 分子在化学变化中发生了变化 D. 分子、原子都是构成物质的粒子
相关试题

