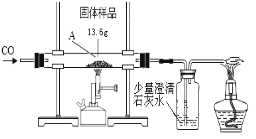
【题目】某化学兴趣小组的同学对一份固体样品进行了探究。通过实验已确定该样品由氧化铁和铁粉混合而成。他们称取了13.6g固体样品,用下图所示的装置继续实验,完全反应后,测定的有关数据如下表所示。
A中固体 的质量 | 澄清石灰水 的质量 | |
反应前 | 13.6g | 102.5g |
反应后 | 11.2g | 108.0g |
请计算:
⑴实验中先通CO的目的是____________________________________。
⑵从上表中选择合适的数据,计算固体样品中氧化铁的质量是_____________克。
⑶在上述反应后的固体中加入100g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数___。(请写出完整计算过程,结果精确到0.1%)
参考答案:
【答案】 除去装置内的空气,防止加热时引起爆炸 8 22.9%
【解析】(1)由于一氧化碳具有可燃性,不纯点燃可能引起爆炸,所以实验中先通CO,除去装置内的空气;
(2)因为少量澄清石灰水不能将生成的二氧化碳完全吸收,所以应该选择A中固体的质量变化进行计算,固体减少的质量为13.6g-11.2g=2.4g,即为氧化铁中氧元素的质量,
设氧化铁的质量为x,
Fe2O3+3CO ![]() 2Fe+3CO2 固体减重
2Fe+3CO2 固体减重
160 112 160-112=48
y (13.6g-11.2 g)=2.4g
![]()
解得x=8g
⑶设生成的FeCl2和H2质量分别为y、z,
Fe + 2HCl =FeCl2 + H2↑
56 127 2
11.2g y z
![]()
解得y=25.4g ,z=0.4g
则反应后的溶液中溶质的质量分数为![]() ×100%≈22.9%。
×100%≈22.9%。
答:反应后的溶液中溶质的质量分数为22.9%。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据题意回答下列问题

(1)实验室常用双氧水和二氧化锰反应制取氧气,写出该反应的化学方程式________________,该反应的基本反应类型为___________________,MnO2在此反应中起______________作用。
(2)从上图中选取BCD组合作为气体发生装置,与ABD相比的优点是_______________________;选取F作为气体收集装置,验满的方法是________________________________ ;选择_____作为气体的收集装置时收集的氧气比较纯净。
(3) I是一种可用于集气、洗气等的多功能装置。若用I装置收集氧气,则气体应从_____(填“a”或“b”)进入,若将I装置内装满水,再连接量筒,就可以用于测定不溶于水且不与水反应的气体体积,则气体应从___________(填“a”或“b”)进入。
-
科目: 来源: 题型:
查看答案和解析>>【题目】Ⅰ.请结合下图回答问题。
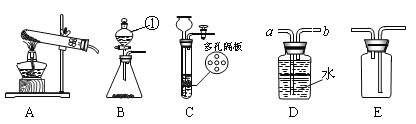
(1)写出图中有标号仪器的名称: ①__________________。
(2)用高锰酸钾制取一瓶干燥的氧气,可选用装置组合为___________(选填序号);实验室制取二氧化碳和氧气可选用发生装置C或B,C装置的优点是__________________,用此装置制取O2的化学方程式是____________________;
(3)实验室常用甲酸(HCOOH)溶液滴加到浓硫酸中制CO气体,可选用的制取装置是______(选填序号)。该反应中浓硫酸既是催化剂又是脱水剂,试写出该反应的化学方程式________________。
Ⅱ.某同学将氢氧化钠溶液滴入到一定量的稀氯化铜溶液中,出现蓝绿色不溶于水的固体。该同学对生成蓝绿色而不是蓝色固体的现象产生疑惑。
(查阅资料)
(1).CuCl2溶液与NaOH溶液反应可生成蓝色固体(Cu(OH)2),在氢氧化钠较少的情况下会生成蓝绿色碱式氯化铜(Cux(OH)yClz),其不溶于水,能与酸反应。
(2).Cu(OH) 2在60℃开始分解生成两种氧化物,100℃分解完全。碱式氯化铜在300℃开始分解生成氧化铜、水和氯化氢,在400℃分解完全。
(猜想)蓝绿色固体可能是:①Cu(OH)2;②Cux(OH)yClz晶体;③_______。猜想①的理由是:________(用化学方程式表示)。
(验证)该同学取31.25g蓝绿色固体,加热至100℃出现黑色固体。则猜想 ________不正确。继续加热到400℃至质量不再改变,并使产生的气体全部缓缓通过如图_____(选填“甲”或“乙”)装置(装置中药品足量)。

(实验数据) ①最终得到剩余固体24.00g;
②与硝酸银溶液反应得到的沉淀经过滤、洗涤和低温烘干,得到固体14.35g;
③浓硫酸装置中数据如表。
加热前
100℃
400℃
250.00g
251.80g
253.60g
(得出结论)猜想③成立,且碱式氯化铜中X∶Y:Z = _________。
(拓展延伸)
为使实验中生成蓝色固体,少出现蓝绿色固体,应作_______________改进(选填序号)。
a.实验中将氯化铜溶液滴加到氢氧化钠溶液中
b.实验中应提供足量、较浓的氢氧化钠溶液
c.实验应该在80℃的水浴中进行
-
科目: 来源: 题型:
查看答案和解析>>【题目】用化学符号填空:
(1)水中氢元素显正一价________________ (2)氯化钠________________
(3)地壳中含量最高的金属元素__________ (4)一个氦原子________________
(5)五个磷原子________________________ (6)三个铁离子________________
-
科目: 来源: 题型:
查看答案和解析>>【题目】亚硒酸钠(Na2SeO3)可用于提高人体免疫力,硒元素的部分信息如图。下列说法正确的 是
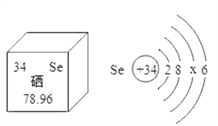
A. 硒元素的原子核外有 78 个电子
B. 硒原子结构示意图中 x=18
C. 1 个硒原子中有 34 个中子
D. 在化学反应中,硒原子容易失去电子
-
科目: 来源: 题型:
查看答案和解析>>【题目】能反映相关实验过程中量的变化的图象是( )

A. 用一氧化碳还原氧化铁
B. 等质量镁、锌分别和足量等质量分数的盐酸反应
C. 镁在氧气中燃烧
D. 等质量、等质量分数的双氧水完全分解
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法错误的是( )
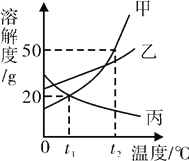
A. t1℃时,甲和丙的溶解度都为 20g
B. 通过冷却热饱和溶液,可以分离甲中混有的少量乙
C. t2℃时,60g 甲加到 100g 水中,能得到 150g 饱和溶液
D. 将 t2℃甲、乙、丙的饱和溶液分别降温到 t1℃,所得溶液的溶质质量分数大小顺序为:乙>甲=丙
相关试题

