【题目】过氧化氢俗称双氧水,常温下是一种无色液体,性质比较稳定。在加热的条件下,它能分解生成氧气和水。查阅资料:
①将新制的浓度5%的双氧水加热到65℃时就有氧气产生,加热到80℃时就有较多氧气产生。
②若在相同质量5%的双氧水加入少量二氧化锰固体,常温下就会立即产生氧气,反应速度快,所需时间短。
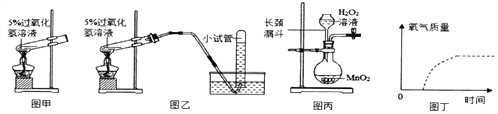
请根据上图回答问题:
(1)请你写出双氧水和二氧化锰反应的化学方程式:_______。其中二氧化锰的作用是_____。
(2)小晨按图甲装置进行实验,当试管中有大量气泡出现时,伸入带火星的木条,木条并未复燃,为此,他利用图乙装置收集气体,再用带火星的木条检验,木条复燃,那么图甲实验中带火星木条未复燃的原因是___________。
(3)小柯利用催化剂使双氧水分解制取氧气,若要控制双氧水制取氧气的速率,可以将装置丙作如下改进_______________________。
(4)采用相同质量5%的双氧水,图丁虚线表示加热分解制取氧气的曲线,请你在该图中用实线画出利用催化剂制取氧气的大致曲线。___________ (假定两种方法过氧化氢均完全分解)
(5)二氧化锰(不溶于水的固体粉末),在该反应中可以重复使用,理由是___________;实验结束后可采取___________的方法,予以回收利用。
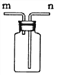
(6)如果用下图的装置收集一瓶氧气,则气体应从________口导入(填“m”或“n”)。
参考答案:
【答案】 2H2O2![]() 2H2O+O2↑ 加快过氧化氢分解的速率 加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,氧气的量较少 长颈漏斗的下端未伸入液面以下,生成的气体会从长颈漏斗中逸出
2H2O+O2↑ 加快过氧化氢分解的速率 加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,氧气的量较少 长颈漏斗的下端未伸入液面以下,生成的气体会从长颈漏斗中逸出 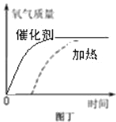 反应前后物质种类、化学性质、质量不变 过滤 n
反应前后物质种类、化学性质、质量不变 过滤 n
【解析】(1)双氧水和二氧化锰反应的化学方程式: 2H2O2 ![]() 2H2O+O2↑。其中二氧化锰的作用是加快过氧化氢分解的速率;(2) 图甲实验中带火星木条未复燃的原因是:加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,氧气的量较少;(3) 在图丙的气体发生装置中,错误是:长颈漏斗的下端未伸入液面以下,生成的气体会从长颈漏斗中逸出; (4) 由于过氧化氢在二氧化锰催化作用下能迅速分解放出氧气,所以,利用催化剂制取氧气的大致曲线为:
2H2O+O2↑。其中二氧化锰的作用是加快过氧化氢分解的速率;(2) 图甲实验中带火星木条未复燃的原因是:加热过氧化氢溶液的同时,溶液中的水蒸气随氧气一起逸出,环境湿度较大,氧气的量较少;(3) 在图丙的气体发生装置中,错误是:长颈漏斗的下端未伸入液面以下,生成的气体会从长颈漏斗中逸出; (4) 由于过氧化氢在二氧化锰催化作用下能迅速分解放出氧气,所以,利用催化剂制取氧气的大致曲线为: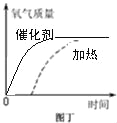 ;(5)二氧化锰(不溶于水的固体粉末),在该反应中可以重复使用,理由是二氧化锰是过氧化氢分解的催化剂,反应前后物质种类、化学性质、质量不变;由于二氧化锰不溶于水,实验结束后可采取过滤的方法,予以回收利用。(6)如果用下图的装置收集一瓶氧气,由于氧气的密度比空气大,则气体应从n。
;(5)二氧化锰(不溶于水的固体粉末),在该反应中可以重复使用,理由是二氧化锰是过氧化氢分解的催化剂,反应前后物质种类、化学性质、质量不变;由于二氧化锰不溶于水,实验结束后可采取过滤的方法,予以回收利用。(6)如果用下图的装置收集一瓶氧气,由于氧气的密度比空气大,则气体应从n。
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学概念间有如右下图所示的部分关系,下列说法正确的是

A. 纯净物与混合物属于包含关系
B. 氧化物与化合物属于交叉关系
C. 物理变化与化学变化属于包含关系
D. 氧化反应与化合反应属于交叉关系
-
科目: 来源: 题型:
查看答案和解析>>【题目】暖宝宝贴(主要成分为铁粉、木炭、食盐)的热量来源与铁粉的氧化.小涛同学设计使用暖宝宝贴来测定空气中氧气的含量,实验开始前的装置如图所示,实验后从量筒中流入玻璃瓶(容积为250mL)中的水的体积为45mL(铁粉生锈消耗的水忽略不计).下列说法错误的是

A.实验前必须检查装置的气密性
B.通过本次实验数据测得空气中氧气的体积分数为18%
C.若实验测得空气中氧气体积分数偏低,可能是暖宝宝贴的使用数量不足
D.必须等温度计的读数恢复至实验前的温度后才能记录量筒内剩余水的体积
-
科目: 来源: 题型:
查看答案和解析>>【题目】完成下列变化的化学方程式,并按要求填空。
(1) 镁粉在空气中燃烧;____;常用镁粉制_____。
(2)加热铜绿:________;其基本反应类型是:_____。
(3)加热碳酸氢铵固体:________;保存方法是______。
(4)实验室制取二氧化碳气体:__________________;如右图:将干燥CO2缓慢通入竖直放置的玻璃管中,能观察到第_______(填序号)号棉球先变色。
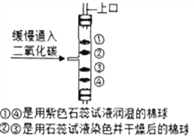
-
科目: 来源: 题型:
查看答案和解析>>【题目】在宏观、微观和符号之间建立联系是化学学科的特点。
(1)下图是水发生甲、乙两种变化的微观结构模型。
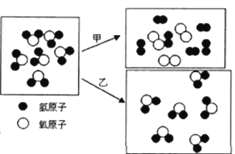
①甲、乙两种变化中属于物理变化的是 ________________________________。
②变化甲的化学方程式为:_________。
(2)低钠盐适合患有高血压、肾病、心脏病的患者服用,苹果酸钠盐(C4H5O5Na)是低钠盐的一种。请回答:
①苹果酸钠盐的相对分子质量是________。
②苹果酸钠盐中各元素的质量比为m(C): m(H): m(O): m(Na)=_________________。
③若某病人每天食用4.68g苹果酸钠盐,则摄入钠元素的质量是________g,比食用相同质量的食盐(NaCI)摄入钠元素少________g。(计算结果保留2位小数)
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室有下列装置,请根据要求回答问题:
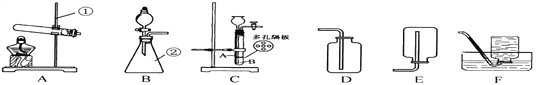
(1)写出有标号仪器②的名称:______________________。实验室用A装置制取氧气的化学方程式:______________________。
(2)检查B装置的气密性的方法是:堵住右侧导气管,____________________,向分液漏斗中加适量的水,若观察到分液漏斗末端出现稳定的水柱,则装置不漏气。
(3)若用装置C制取二氧化碳气体,为了防止二氧化碳从长颈漏斗下端逸出,正确的操作是:_________________,其中块状固体大理石应放置在__________________处(填“A”或“B”),一段时间后,需停止反应,其操作是______________________。
(4)实验室用高锰酸钾制取氧气并用于验证蜡烛燃烧产物的实验,最好选用收集装置为________________填序号);如何判断该装置已收集满氧气___________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】请在下面的横线上写出相应的符号或名称,注意格式规范。
(1)2个氧分子_________; (2)NH4+的名称是_________;(3)3个铜原子_________;
(4)2个碳酸根离子________;(5)硫酸铝___________; (6)2H2O______________;
(7)人体内含量最多的元素______; (8)标出KNO3中N元素的化合价_______。
相关试题

