【题目】铜及铜的化合物在生产、生活中有着广泛的应用。
(一)铜的广泛应用
(1)我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理______。
(2)铜在工业上可用于生产电缆(外面包裹了电缆皮),这是利用了铜的_____性。
(二)硫酸铜晶体的制备
工业上用含铜废料(如:碎铜、电缆皮等)。某化学小组的同学提出可以用含铜废料制备硫酸铜晶体(CuSO4·xH2O).主要流程如下:
![]()
(1)含铜废料粉碎的目的是__________。
(2)该流程中,加入H2O2后要求温度控制在50℃到60℃加热的原因为_____。
(3)兴趣小组同学一致指出,将滤液经蒸发浓缩、_____(填结晶方法)、过滤等操作后,用少量95%的酒精淋洗后晾干,得硫酸铜晶体(CuSO4·xH2O),晶体采用酒精淋洗而不用水的原因是____________。
(三)铜生锈会生成碱式碳酸铜,而工业上所制得的碱式碳酸铜种类较多,其组成表示为:xCuCO3·yCu(OH)2·zH2O。
资料:xCuCO3·yCu(OH)2·zH2O加热至200时会分解得到氧化铜,二氧化碳和水。
测定某种产品的组成,该兴趣小组准确称量了25.8g的样品,设计了如下装置并进行实验:
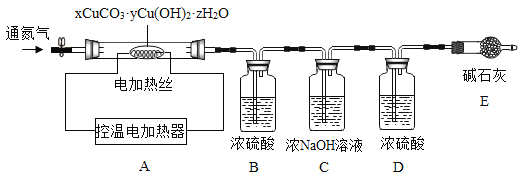
实验数据记录如下表:
B中溶液质量/g | C中溶液质量/g | D中溶液质量/g | E中固体质量/g | |
反应前 | 100.0 | 100.0 | 100.0 | 120.5 |
反应后 | 105.4 | 104.4 | 100.2 | 120.5 |
实验分析和数据处理
(1)实验前应该先_________,再鼓入一段时间氮气后称量B、C、D、E的质量。
(2)停止鼓入氮气,调控温电加热220℃持续加热,观察到装置B中______时表明碱式碳酸铜已经完全分解。
(3)反应结束后,再缓缓鼓入一段时间氮气的目的是___________。
(4)该碱式碳酸铜的化学式是__________。
参考答案:
【答案】Fe+CuSO4=FeSO4+Cu 导电 增大反应物之间的接触面积,加快反应速率 防止温度过高过氧化氢分解 冷却结晶 防止晶体溶于水带来损耗或酒精有挥发性便于晾干(答一点就对) 检查气密性 不再有气泡生成 排装置内气体,使生成的二氧化碳和水蒸气被后面的装置充分吸收 CuCO3·Cu(OH)2·2H2O
【解析】
(一)(1)“曾青得铁则化为铜”是铁与硫酸铜反应生成铜和硫酸亚铁;故填:Fe+CuSO4=FeSO4+Cu;
(2)铜具有导电性,可以制成导线;故填:导电性;
(二)(1)含铜废料粉碎的目的是增大反应物之间的接触面积,加快反应速率;故填:增大反应物之间的接触面积,加快反应速率;
(2)H2O2受热易分解,温度应该控制在50℃到60℃之间,防止温度过高过氧化氢分解;故填:防止温度过高过氧化氢分解;
(3)兴趣小组同学一致指出,将滤液经蒸发浓缩、冷却结晶、过滤等操作得到硫酸铜晶体;用水洗涤可以溶解硫酸铜晶体,使硫酸铜晶体有损失,所以所得硫酸铜晶体需要洗涤后晾干,最合适的洗涤试剂是95%的酒精,因为硫酸铜晶体不溶于酒精,且酒精有挥发性便于晾干;故填:冷却结晶;防止晶体溶于水带来损耗或酒精有挥发性便于晾干;
(三)(1)实验前应该先检查气密性,再鼓入一段时间氮气后称量B、C、D、E的质量。故填:检查气密性;
(2)xCuCO3·yCu(OH)2·zH2O加热至200时会分解得到氧化铜,二氧化碳和水。停止鼓入氮气,调控温电加热220℃持续加热,观察到装置B中不再有气泡生成时表明碱式碳酸铜已经完全分解。故填:不再有气泡生成;
(3)反应结束后,再缓缓鼓入一段时间氮气的目的是排装置内气体,使生成的二氧化碳和水蒸气被后面的装置充分吸收。故填:排装置内气体,使生成的二氧化碳和水蒸气被后面的装置充分吸收;
(4)B中溶液质量增加5.4g,C中溶液质量增加4.4g,所以生成水的质量为5.4g,二氧化碳的质量为4.2g,A中生成氧化铜固体的质量为25.8g-4.4g-5.4g=16g,
设碳酸铜的质量为x,生成氧化铜的质量为y
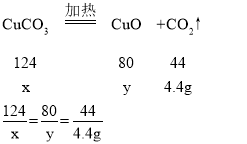
x=12.4g y=8g
所以氢氧化铜加热分解生成氧化铜的质量为16g-8g=8g
设氢氧化铜的质量为z,生成水的质量为a
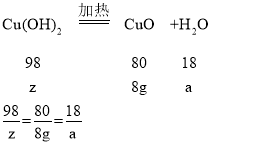
z=9.8g a=1.8g
所以xCuCO3·yCu(OH)2·zH2O中结晶水的质量为5.4g-1.8g=3.6g
根据题意有:![]() x:y:z
x:y:z
通过计算可得:x:y:z=1:1:2
所以该碱式碳酸铜的化学式是CuCO3·Cu(OH)2·2H2O。
故填:CuCO3·Cu(OH)2·2H2O。
-
科目: 来源: 题型:
查看答案和解析>>【题目】日前,东南大学教师首创“南京地铁车厢速查表”走红网络。地铁是指在地下运行为主的城市轨道交通系统,地铁建设中各种材料被广泛应用。
(1)地铁站的排水管采用聚乙烯塑料管道,聚乙烯塑料属于__________(填“金属材料”或“合成材料”)。
(2)施工中挖掘岩石的机械刀片用钨钢制成,据此推测钨钢具有的一条物理性质______________________________。
(3)科研人员研制出的钢轨防锈涂料主要是为了防锈,其原理是_________________________。
(4)地铁隧道中常用氢氧化镁作为阻燃材料,其阻燃原理是受热分解生成水蒸气和耐高温的氧化镁,该反应的化学方程式是_________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据所学知识并结合下图回答有关问题。
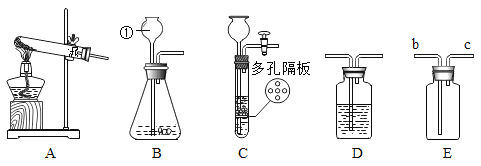
(1)写出标号①仪器名称______。
(2)实验室可用高锰酸钾制取氧气,应选用上述装置_____作为发生装置,反应的化学方程式为______________。如果用E装置收集O2,则验满的方法是_________。
(3)实验室常用锌与稀硫酸为原料制取H2,其反应的化学方程式为_____。若要获得干燥的H2,除发生装置外,还应选用D装置,并在该装置中盛放_____(填写试剂名称),若制取0.4gH2,理论上需要________g10%的稀硫酸与足量锌反应。
(4)小睿和小琦两位同学用下图所示装置进行实验,验证二氧化碳与氢氧化钠、氢氧化钙都能发生反应。
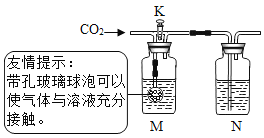
①小琦先关闭K,通入二氧化碳,M、N中均无明显变化,M中盛放______溶液。
②小琦再打开K,继续通入二氧化碳,N中反应的化学方程式为______。此步实验目的__________。小睿认为:通常状况下,1体积的水约能溶解1体积二氧化碳,因此上述实验不足以证明二氧化碳和氢氧化钠发生了反应。
③小睿用洗涤干净的上述装置重新实验,分别量取50 mL上述溶液放入M、N中,关闭K,通入约500 mL二氧化碳,M、N中均无明显变化。此实验可以说明二氧化碳和氢氧化钠发生了反应,其理由是____________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】二氧化氯(ClO2)可用于自来水消毒。以粗盐为原料生产ClO2的工艺主要包括:
①反应Ⅰ是粗盐除杂;
②反应Ⅱ是特殊条件下电解NaCl溶液制NaClO3;
③反应Ⅲ是ClO2的制取。其中反应Ⅲ制取ClO2的化学方程式为:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O。
工艺流程如图,
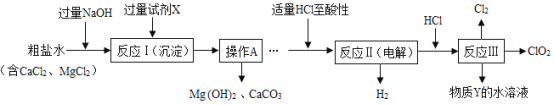
(1)加入过量氢氧化钠的目的是________。
(2)过量的试剂X是____(填化学式),操作A的名称是_______。
(3)求出沉淀ClO2中Cl的化合价为_______。
(4)加入适量HCl除为了满足电解时的微酸性外,还能除去溶液中的杂质离子,请写出其中所发生的中和反应的化学方程式:___________。
(5)该流程中可循环利用的物质是水和________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】推理是化学学习的重要方法之一,下列说法正确的是( )
A.酸雨的pH小于7,因此pH小于7的雨水一定是酸雨
B.溶液具有均一性和稳定性,因此具有均一性和稳定性的液体一定是溶液
C.置换反应生成单质和化合物,因此生成单质和化合物的反应一定是置换反应
D.点燃可燃性气体前要检验气体纯度,因此点燃甲烷前一定要检验气体的纯度
-
科目: 来源: 题型:
查看答案和解析>>【题目】甲、乙两种固定物质的溶解度曲线如图所示,下列说法正确的是( )
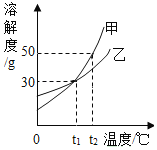
A.在0~t1℃时,甲的溶解度大于乙的溶解度
B.t1℃时,两种物质的溶液中溶质质量分数一定相等
C.t2℃时,150g甲的饱和溶液和100g水混合,所得溶液的溶质质量分数为20%
D.将t2℃时等质量的甲、乙饱和溶液分别降温至t1℃,甲析出固体的质量比乙小
-
科目: 来源: 题型:
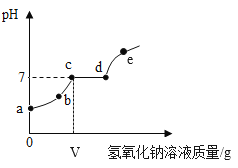
查看答案和解析>>【题目】向一定量的稀盐酸和氯化镁的混合溶液中,逐滴加入一定溶质质量分数的氢氧化钠溶液至过量,溶液pH的变化曲线如图所示:
(1)e点时溶液中含有哪些溶质?_____。
(2)写出cd段发生反应的化学方程式_____。
(3)若将Vg氢氧化钠溶液换用等质量、等溶质质量分数的氢氧化钾溶液,反应后溶液的pH_____7(选填“>”“<”或“=”)。
相关试题

