【题目】过氧化钠(Na2O2)是一种供氧剂,与水反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑。将10g含过氧化钠78%的过氧化钠样品(只含有NaOH杂质)加入到85.2g质量分数为10%的氢氧化钠溶液中充分反应(水的挥发忽略不计)。请计算:
(1)生成氧气的质量。
(2)反应后所得溶液中溶质的质量分数。
(3)若将反应后的溶液的溶质质量分数恢复到10%,需加入水的质量。
参考答案:
【答案】(1)1.6g;(2)20%;(3)93.6g
【解析】10g含过氧化钠78%的过氧化钠样品中含过氧化钠质量∶10g×78%=7.8g.
解∶设生成氧气的质量质量为xg,生成氢氧化钠质量为yg
2Na2O2+2H2O═4NaOH+O2↑
156 160 32
7.8g y x
![]() =
=![]() ,x=1.6g;
,x=1.6g; ![]() =
=![]() ,y=8g.
,y=8g.
反应后所得溶液中溶质的质量分数∶![]() ×100%=20%;
×100%=20%;
解∶设若将反应后的溶液的溶质质量分数恢复到10%,需加入水的质量为xg
﹙10g+85.2g-1.6g﹚×20%=﹙10g+85.2g-1.6g+x﹚×10%
x=93.6g
答∶(1)生成氧气的质量是1.6g;(2)反应后所得溶液中溶质的质量分数是20%;﹙3)若将反应后的溶液的溶质质量分数恢复到10%,需加入水的质量是93.6g。
点睛∶本题主要考查质量守恒定律的应用以及根据化学方程式进行计算。
-
科目: 来源: 题型:
查看答案和解析>>【题目】在一定条件下发生反应:2R+2H2O+7O2═2FeSO4+2H2SO4,则R的化学式是
A.FeS B.Fe2S3 C.FeO D.FeS2
-
科目: 来源: 题型:
查看答案和解析>>【题目】在当下热播的电视剧《人民的名义》中,达康书记在省委召开的环境综合治理扩大会议上指出:工厂废液应变废为宝并处理达标后才能排放。某工厂废液中含有氯化钠、氯化铜和氯化亚铁,某课外小组要从废液中回收铜,并得到铁红(主要成分是Fe2O3),要求全过程不引入其它金属元素,设计实验方案如图所示,回答下列问题:

(1)在步骤①中,操作a的名称是____________。
(2)步骤①、②、③中所发生的化学反应,其中属于复分解反应的是_________(填序号)。
(3)步骤④中,如果发生的是一个分解反应,且生成物为两种氧化物,则另外一种生成物应该是____________。
(4)铁红是炼铁的主要原料,工业上用CO和铁红炼铁的化学方程式是________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】化学兴趣小组在吴老师的指导下,借助紫甘蓝汁液进行中和反应实验。
【演示实验】取少许久置的NaOH溶液,并滴入几滴紫甘蓝汁液(溶液由紫变黄);然后向黄色NaOH溶液中逐滴加入稀盐酸,发现溶液中冒气泡,且溶液从下至上依次呈现黄色、绿色、蓝色、紫色、粉红、深红色等,宛若彩虹、非常美丽。
探究Ⅰ:为什么反应过程中溶液里呈现多彩的颜色
【进行猜想】
小彤猜想:可能是反应过程中,溶液中各部位紫甘蓝汁液的浓度不同。
小哲猜想:可能是反应过程中,溶液中各部位的酸碱度(pH)不同。
【实验验证】
(1)在小烧杯中加入少许紫甘蓝汁液,然后逐渐加入适量的水,溶液始终是紫色。
(2)在另一个小烧杯中加入适量新配制的NaOH溶液,然后逐滴加入稀盐酸,及时观察溶液颜色的变化,同时用传感器测出反应过程中溶液pH的变化,绘制溶液pH及颜色的变化图(如图所示)。读图可知,______________________的猜想是正确的。

【拓展延伸】结合图像思考:
(1)当酸碱恰好完全中和时,溶液呈____________________色;
(2)当溶液呈红色时,对应溶液中的溶质是________________。
探究Ⅱ:久置的NaOH溶液的溶质成分
【查阅资料】CaCl2溶液显中性。
【实验验证】
(1)小宇认为,因为向久置的NaOH溶液中滴加稀盐酸时产生了气泡,所以该溶液已变质。请用化学方程式表示NaOH溶液变质的原因:___________________________________。
(2)小文取少量久置的NaOH溶液,滴入足量CaCl2溶液,产生白色沉淀;再向上层清液中滴入几滴紫甘蓝汁液,溶液显黄色。因此,这瓶久置的NaOH溶液的溶质成分是_____________。
【评价反思】作为酸碱指示剂,紫甘蓝汁液与紫色石蕊溶液相比,优点明显,它既能测出溶液的酸碱性,还能显示溶液的___________________________________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】烧杯中有CaCl2与稀HCl的混合溶液50g,向烧杯中逐渐加入10.0% Na2CO3溶液,所得溶液的质量与所滴加Na2CO3溶液质量关系如图(不考虑生成气体在溶液中的溶解和其他物质的挥发)。下列说法正确的是( )
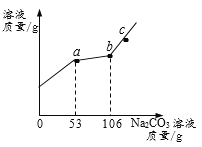
A. a-b段产生气体
B. c点溶液的pH>7
C. b点时烧杯中物质的总质量为148.8g
D. a到b过程中,溶液中NaCl的质量分数在不断增大
-
科目: 来源: 题型:
查看答案和解析>>【题目】KNO3和NaCl的溶解度表及溶解度曲线如下,下列说法错误的是( )
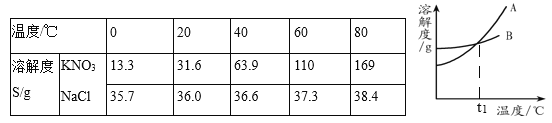
A. t1介于20℃-40℃之间
B. 50℃时,溶液的溶质质量分数:KNO3>NaCl
C. 当KNO3中混有少量NaCl时,可用降温结晶的方法提纯
D. 60℃时,30g KNO3加入50g水,充分溶解,再降温到20℃,会析出晶体14.2g
-
科目: 来源: 题型:
查看答案和解析>>【题目】除去下列物质中的杂质(括号中的为杂质),所用试剂错误的是
选项
A
B
C
D
物质
CO2(CO)
CO2(HCl)
Cu(CuO)
KCl(MnO2)
除杂试剂
CuO
NaOH溶液
稀盐酸
H2O
相关试题

