【题目】请结合下图回答问题:
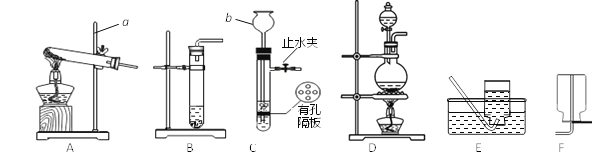
(1)仪器名称:a_______,b_______。
(2)用氯酸钾和二氧化锰制取O2,可选用装置A和______(选填装置序号)组合,反应的化学方程式为________。
(3)实验室制取氢气的化学方程式为_______,可选用发生装置C或______(选填装置序号);相对于另一装置,C具有的优点是________。
(4)用下图装置制取CO2并验证相关性质。
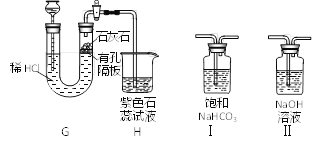
①生成CO2反应的化学方程式________。
②装置H中石蕊变红,甲同学得出CO2与H2O反应生成H2CO3的结论,乙同学提出质疑,理由是________。
③要消除以上质疑,可在装置G、H之间连接装置_________(选填“Ⅰ”或“Ⅱ”)。
参考答案:
【答案】 铁架台 长颈漏斗 E 2KClO3 ![]() 2KCl+3O2↑ Zn+2HCl=ZnCl2+H2↑或Zn+ H2SO4=ZnSO4+H2↑ B 控制反应的发生和停止 CaCO3+2HCl=CaCl2+CO2↑+ H2O CO2中含有HCl Ⅰ
2KCl+3O2↑ Zn+2HCl=ZnCl2+H2↑或Zn+ H2SO4=ZnSO4+H2↑ B 控制反应的发生和停止 CaCO3+2HCl=CaCl2+CO2↑+ H2O CO2中含有HCl Ⅰ
【解析】(1)仪器名称:a_铁架台,b长颈漏斗。(2)氧气难溶于水,可用排水法收集,用氯酸钾和二氧化锰制取O2,可选用装置A和E组合,反应的化学方程式为_2KClO3 ![]() 2KCl+3O2↑;(3)实验室常用锌和盐酸或硫酸反应制取氢气,化学方程式为Zn+2HCl=ZnCl2+H2↑或Zn+ H2SO4=ZnSO4+H2↑,可选用发生装置C或F,因为氢气的密度比空气小,可以用向下排空气法收集;相对于另一装置,C具有的优点是控制反应的发生和停止。关闭弹簧夹,大试管内气体增多,压强变大,在压力的作用下,试管内液面下降,当液面下降到隔板下边时,固体反应物与液体分离,反应停止;反之,打开弹簧夹,反应开始;(4) ①石灰石的主要成分碳酸钙和盐酸反应生成氯化钙、二氧化碳、水,反应的化学方程式CaCO3+2HCl=CaCl2+CO2↑+ H2O;②装置H中石蕊变红,不能得出CO2与H2O反应生成H2CO3的结论,理由是盐酸有挥发性,制取的CO2中含有HCl,也能使紫色石蕊试液变红;③要消除以上质疑,可在装置G、H之间连接装置Ⅰ,因为碳酸氢钠和盐酸反应生成氯化钠、二氧化碳、水,将氯化氢吸收。
2KCl+3O2↑;(3)实验室常用锌和盐酸或硫酸反应制取氢气,化学方程式为Zn+2HCl=ZnCl2+H2↑或Zn+ H2SO4=ZnSO4+H2↑,可选用发生装置C或F,因为氢气的密度比空气小,可以用向下排空气法收集;相对于另一装置,C具有的优点是控制反应的发生和停止。关闭弹簧夹,大试管内气体增多,压强变大,在压力的作用下,试管内液面下降,当液面下降到隔板下边时,固体反应物与液体分离,反应停止;反之,打开弹簧夹,反应开始;(4) ①石灰石的主要成分碳酸钙和盐酸反应生成氯化钙、二氧化碳、水,反应的化学方程式CaCO3+2HCl=CaCl2+CO2↑+ H2O;②装置H中石蕊变红,不能得出CO2与H2O反应生成H2CO3的结论,理由是盐酸有挥发性,制取的CO2中含有HCl,也能使紫色石蕊试液变红;③要消除以上质疑,可在装置G、H之间连接装置Ⅰ,因为碳酸氢钠和盐酸反应生成氯化钠、二氧化碳、水,将氯化氢吸收。
-
科目: 来源: 题型:
查看答案和解析>>【题目】向10.0g某石灰石(杂质不溶于水且不参加反应)中先后滴加100.0g稀HCl和一定质量Na2CO3溶液,反应过程中加入溶液的质量与不溶固体或产生气体的质量关系如右图所示。下列说法错误的是
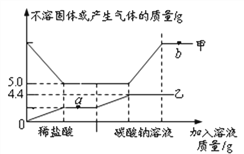
A. 甲表示不溶固体的质量
B. a点对应溶液中的溶质只有1种
C. 该稀盐酸的溶质质量分数为7.3%
D. 检验b点对应溶液中的溶质,可先滴加足量的AgNO3溶液,静置后再滴加少量Ca(NO3)2溶液
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图是目前研究热点——人工光合作用的构想。
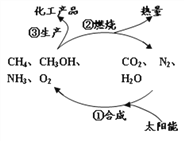
下列说法错误的是
A. 光合作用中太阳能转化为化学能
B. 此构想体现无机物与有机物可相互转化
C. ①中吸收的CO2与②中释放的CO2的量一定相等
D. 合成CH3OH的化学方程式:2CO2 + 4H2O
 2CH3OH + 3O2
2CH3OH + 3O2 -
科目: 来源: 题型:
查看答案和解析>>【题目】在KMnO4溶液中加入双氧水,振荡、静置,再滴入酚酞,出现如图所示现象。
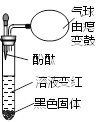
(1)将混合物进行过滤,向滤渣中加入双氧水,迅速产生大量气泡,滤渣的作用是_____。
(2)写出KMnO4溶液与双氧水反应的化学方程式(其中KMnO4与H2O2的化学计量数为2和3)______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下图为某些物质间的转化关系。A为常见化肥,E常作食品干燥剂,M只含3种元素。部分反应条件和生成物已略去。
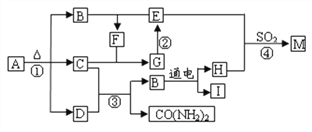
(1)化学式:A___________,F____________。
(2)反应①提醒在施用A时要注意__________。
(3)反应②的化学方程式:_______________。
(4)反应③中C和D的质量比为_________________。
(5)反应④符合“化学反应绿色化”(即原料中所有的原子全部转入期望的产品中),写出反应④的化学方程式________________。
-
科目: 来源: 题型:
查看答案和解析>>【题目】实验室用碳酸钡矿石(杂质不溶于水且不参加反应)制备BaCl2晶体的主要流程如下:
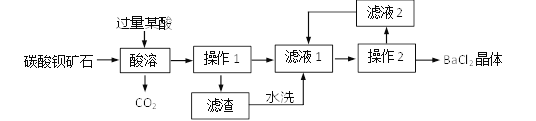
(1)某酸应选用______(选填序号)。
a.H2SO4 b.HCl c.HNO3
(2)证明某酸过量的方法:静置,向上层清液中滴加______溶液,产生气泡。
(3)操作1中,所用玻璃仪器有______、玻璃棒、烧杯。
(4)将滤渣水洗液和滤液2加入滤液1中的目的是_____(选填序号)。
a.提高原料的利用率 b.减少钡盐对环境的污染
-
科目: 来源: 题型:
查看答案和解析>>【题目】铁及其化合物应用广泛。
(一)铁及其化合物的应用
①下图3为某小儿硫酸亚铁糖浆。
(1)适当服用该糖浆可治疗______________(选填序号)。
A.佝偻病 B.侏儒症 C.贫血症
(2)图中不涉及到的材料是_________________(选填序号)。
A.无机材料 B.合成材料 C.复合材料

②食品保鲜“双吸剂”含铁粉、食盐等,上图4为其原理探究实验:
(1)滴入食盐水后,关闭分液漏斗活塞。一段时间后,铁粉上出现红色固体,气球______(选填“变大”、“不变”或“变小”)。
(2)食盐水的作用是______。
(二)铁及其化合物的实验
(1)将废铁屑加入滴有洗涤剂的热水中,充分搅拌以除去油污,这利用了洗涤剂的______作用。
(2)取干燥后的过量铁屑溶于一定量的稀H2SO4(水浴加热控制在50~80℃),搅拌、静置、过滤、洗涤,检验铁粉已洗净的方法是________。
(3)向上述所得滤液中加入饱和(NH4)2SO4溶液,经蒸发浓缩、________、过滤等操作得到浅蓝绿色晶体。
(查阅资料)常见含铁元素的浅蓝绿色晶体有:①硫酸亚铁晶体[FeSO47H2O];
②硫酸亚铁铵晶体[FeSO4(NH4)2SO46H2O]。
(4)取一定量晶体样品,溶于适量水,加入足量的______溶液,微热,并把产生的气体通入酚酞试液,酚酞试液变成______色,说明该晶体是硫酸亚铁铵晶体。
(三)硫酸亚铁铵晶体的热分解实验
兴趣小组称取此晶体样品39.2g,在科研人员的指导下用下图装置进行热分解实验。
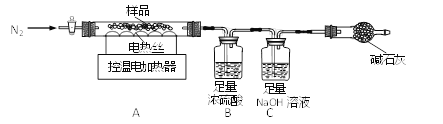
(查阅资料)①硫酸亚铁铵晶体(相对分子质量为392)在100℃完全失去结晶水,剩余物在500℃完全分解为铁的某氧化物、SO2、SO3、NH3和H2O。
②B装置中浓硫酸只能吸收NH3、SO3和H2O。
(1)装配好实验装置后,先要________。
(2)加热前后及过程中均通入N2,停止加热后继续通N2的目的是防止倒吸和________。
(3)控制不同的温度对A中固体加热,测得装置B和C中的质量变化如下表。
温度/℃
室温
100
500
B装置/g
200.00
x
228.00
C装置/g
100.00
100.00
103.20
①表格中x =________。
②最终生成SO3的质量为________g,铁的某氧化物的化学式为________。
相关试题

