【题目】某无毒气体的密度比空气密度大,且不与空气反应并极难溶于水,那么收集该气体的方法是 ①向上排空气法 ②向下排空气法 ③排水法 ( )
A. ①② B. ①③ C. ②③ D. ①②③
参考答案:
【答案】B
【解析】该气体的密度比空气大,极难溶于水,并且是无毒气体,可用向上排空气法或排水法收集.故选B。
-
科目: 来源: 题型:
查看答案和解析>>【题目】中和反应是放热反应吗?三位同学为探究此问题进行了下列实验:
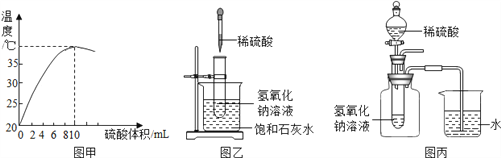
(1)甲同学取10mL10%的NaOH溶液于试管中,逐滴加入10%的稀硫酸,随着硫酸的加入,烧杯中溶液温度与加入硫酸体积之间的变化关系如甲图所示.本实验选用10%的NaOH溶液而不选用NaOH固体的原因是_________________________________________________。
(2)乙同学按乙图装置进行实验,其中的澄清饱和石灰水的作用是__________________。
(3)丙同学按丙图实验,可以根据_____________的现象也能证明中和反应是放热的。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列事实分别说明微粒具有什么性质?
①打气筒能将空气压入足球内: ;
②食醋在空气中放置一段时间后,醋的酸味会变淡: ;
③一滴水里的水分子个数由十亿人来数,每人每分钟数一百个,日夜不停,需三万年才能数完: .
-
科目: 来源: 题型:
查看答案和解析>>【题目】将0.4%的氢氧化钠溶液滴加到2mL0.4%的盐酸中,测得混合液的pH变化曲线如图。某学习小组对加入0—— VmL氢氧化钠过程中,所得混合液pH增大原因进行了如下探究:

【猜想假设】
猜想Ⅰ:pH增大是因为 ;
猜想Ⅱ:pH增大是因为发生了反应,写出反应方程式 。
【实验探究】
为验证猜想Ⅱ,请你帮助该小组完成下列实验。(可供选择的实验用品有:pH计、0.4%的氢氧化钠溶液、0.4%的盐酸、水。)
(1)向2mL0.4%的盐酸中加入VmL0.4%的氢氧化钠溶液,用pH计测得混合液的pH=7。
(2)向2mL0.4%的盐酸中加入VmL ,用pH计测得混合液的pH 7(填“>”、“=”或“<”)。综合(1)和(2)证明猜想Ⅱ成立。
-
科目: 来源: 题型:
查看答案和解析>>【题目】为测定某盐酸的质量分数:往20 g 40%的氢氧化钠溶液的烧杯中逐滴加入该盐酸,加入盐酸的质量与烧杯中溶液pH的变化关系如图所示。

(1)所用氢氧化钠溶液中溶质的质量为________g。
(2)当滴加盐酸到图象中B点时,烧杯中溶液的溶质是________(填化学式)。
(3)计算该盐酸的质量分数是________?
-
科目: 来源: 题型:
查看答案和解析>>【题目】一定温度下,向图Ⅰ烧杯中加入一定量的水,如图Ⅱ所示,所得溶液与原溶液相比,下列判断一定正确的是( )

A. 所得溶液是饱和溶液 B. 溶质的浓度变大
C. 溶质的质量增加 D. 溶质的溶解度变大
-
科目: 来源: 题型:
查看答案和解析>>【题目】请你各举一个实例,说明下列有关溶液的叙述是错误的.
(1)溶液一定是无色的.实例: .
(2)溶液中的溶质一定是固体.实例: .
(3)均一稳定的液体一定是溶液.实例: .
相关试题

