【题目】在一烧杯中盛有100g BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入的Na2CO3溶液的质量关系图象如图所示。
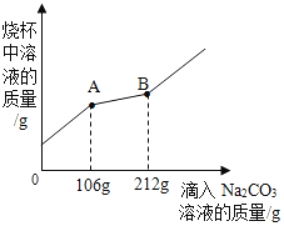
(1)在实验过程中,可以先后看到的明显实验现象是_____。
(2)求原溶液中BaCl2的质量分数为多少?_________
(3)当滴入Na2CO3溶液至图中B点时,通过计算求所得不饱和溶液中溶质质量分数为多少?(计算结果精确到0.1%)_________
参考答案:
【答案】先有气体放出,后有白色沉淀生成 7.3% 8.1%
【解析】
(1)向盛有BaCl2和HCl的混合溶液中滴加Na2CO3溶液时,碳酸钠先与盐酸反应产生二氧化碳,当盐酸反应完后,再与氯化钡反应产生碳酸钡沉淀;
(2)开始时是生成气体的,由于加入的是碳酸钠溶液,而生成的是二氧化碳气体,两者的质量明显是增加多,减少的少,所以曲线明显上扬。当不再生成二氧化碳时,就生成碳酸钡,由于碳酸钡的质量要多于碳酸钠的,所以导致溶液的质量增加减缓。从图中曲线可看出,当滴入碳酸钠106g时,盐酸完全反应,据此可根据滴入碳酸钠质量计算消耗HCl的质量;
(3)从图中曲线可看出,开始滴入106克的碳酸钠与盐酸反应,106克~212克之间滴入碳酸钠与氯化钡反应;即与氯化钡反应的碳酸钠质量为212克-106克;由化学方程式知,碳酸钠和盐酸、氯化钡反应后溶液中溶质均为氯化钠,可根据化学方程式中参加反应的碳酸钠质量计算生成的氯化钠质量和碳酸钡沉淀质量,再根据质量守恒定律,参加反应的物质总质量等于生成的物质总质量,最后所得不饱和溶液的质量等于l00gBaCl2和HCl的混合溶液,加上滴入的212gNa2CO3溶液,减去生成的气体和沉淀的质量,即可计算所得不饱和溶液中溶质质量分数。
解:(1)碳酸钠和盐酸反应产生二氧化碳,有气体放出,与氯化钡反应产生碳酸钡,即有白色沉淀产生;
(2)设原溶液中BaCl2的质量为x,则:
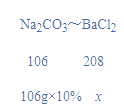
![]()
x=20.8g,
原溶液中BaCl2的质量分数为:![]() ×100%=20.8%;
×100%=20.8%;
(3)设实验过程中产生氯化钠质量为y,产生碳酸钡质量为z,则:本关系是指整个过程的,不考虑是碳酸钠与盐酸还是和氯化钡反应,最终对应的钠都在氯化钠中;

![]()
y=23.4g,
后期的碳酸钠中碳酸根转化为碳酸钡沉淀,所以对应的碳酸钠是106g溶液之后的部分:

![]()
z=19.7g,
所得NaCl溶液的质量分数为:![]() ×100%=8.1%;
×100%=8.1%;
答:(1)在实验过程中,可以先后看到的明显实验现象是:先有气体放出,后有白色沉淀生成;
(2)原溶液中BaCl2的质量分数为20.8%;
(3)所得不饱和溶液中溶质质量分数是8.1%。
-
科目: 来源: 题型:
查看答案和解析>>【题目】向Na2CO3溶液中滴入Ca(OH)2溶液至恰好完全反应。
(1)可以观察的实验现象是_____。
(2)如图表示该反应前后溶液中存在的主要离子,写出每种图形代表的离子(填离子符号)。
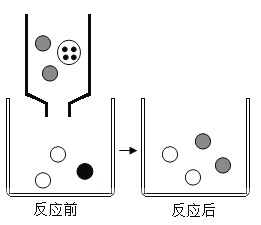
 _____
_____  _____
_____  _____
_____(3)下列物质只有一种能与BaCl2溶液反应产生类似上述实验现象,应是_____(填字母序号)。
A.H2SO4 B.NaOH C.NaCl
-
科目: 来源: 题型:
查看答案和解析>>【题目】2010年4月28日某媒体题为“排污工程施工,毒气放倒三人”的报道,引起某兴趣小组同学的思考.
提出问题:排污管道中的毒气有什么成分?
查阅资料:
I.排污管道中的大部分有机物在一定条件下发酵会产生CO、CO2、H2S,CH4等.
Ⅱ.H2S气体能与CuSO4溶液反应生成黑色沉淀,且能与碱溶液发生中和反应.
提出猜想:小组同学对排污管道气含有上述气体中最少3种成分的猜想如下:
猜想1:有CO、CO2、H2S; 猜想2:有CO、CO2、CH4;
猜想3:有CO、H2S、CH4; 猜想4:有CO2、H2S、_____;
猜想5:有CO、CO2、H2S、CH4.
实验方案:小组同学共同设计了下图所示的装置并进行探究(夹持仪器已省略).
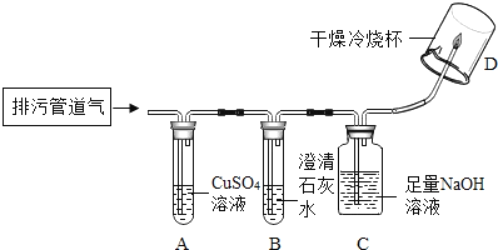
问题讨论:
(1)如果A装置没有明显变化,则猜想_____成立;
(2)在验证猜想1的实验中,装置C中NaOH溶液的作用是_____;若要进一步验证气体燃烧后的产物,操作是:迅速把烧杯倒过来,向烧杯内注入_____,振荡.
(3)要确证猜想5中是否有CH4,某同学认为图示装置有不足之处,需要在装置C与D之间加一个_____装置.改进后,若气体燃烧,且D装置内壁出现_____,证明气体中一定含有CH4.
-
科目: 来源: 题型:
查看答案和解析>>【题目】某化肥由(NH4)2SO4,K2SO4、KCI混合而成,对提高农作物产量有重要作用。
(1)该化肥施用后,能使植物_____(填序号)
A.茎叶生长茂盛 B.增强抗寒抗旱能力 C.增强抗倒伏,抗虫害能力
(2)(NH4)2SO4中N、O两元素的质量比为_____(化成最简比)
(3)为测定该化肥样品中氮元素的质量分数,小民和小青分别按自己设计的方案进行了实验。
方案1:小民取10.0g样品溶于水,加入足量的BaCl2溶液,充分反应后,过滤、洗涤、干燥、称量得固体质量为16.5g
方案2:小青另取等质量的样品,加入足量的Ca(OH)2加热,将气体通过氢氧化钠固体和浓硫酸,氢氧化钠固体增重1.8g,浓硫酸增重1.7g(假设气体全部吸收)。
用方案1计算出的氮元素的质量分数偏大,简述理由_____。
用方案2计算该化肥样品中氮元素的质量分数数(请在答题纸上写出计算过程)。___________
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列反应属于置换反应的是( )
A. NH3+CO2+H2O=NH4HCO3
B. H2+CuO
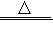 Cu+H2O
Cu+H2OC. 2KMnO4
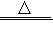 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑D. HCl+AgNO3=AgCl↓+HNO3
-
科目: 来源: 题型:
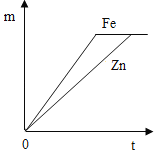
查看答案和解析>>【题目】足量且形状相同的锌、铁分别于等质量、相同溶质质量分数的稀盐酸充分反应,生成氢气的质量m与反应时间t的关系正确的是( )
A.
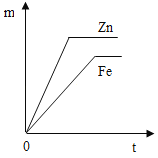 B.
B. 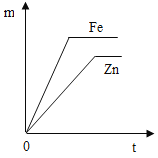
C.
 D.
D. 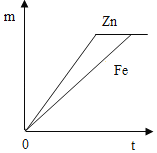
-
科目: 来源: 题型:
查看答案和解析>>【题目】(4分)对比、分析、归纳是学习化学的重要方法。
(1)已知H2、CO、C是初中化学常见的还原剂,请分析下列反应:
H2+ CuO
 Cu + H2O 3CO + Fe2O3
Cu + H2O 3CO + Fe2O3 2Fe + 3CO2C + O2
2Fe + 3CO2C + O2  CO2
CO2得出的结论是:物质(如H2、CO、C)作还原剂时,所含元素中,一定有元素的化合价在反应后 (选填“升高”或“降低”或“不变”)。
(2)依据上述结论,则在反应SO2+ 2H2S = 3S + 2H2O中作为还原剂的物质是 ;
该还原剂中所含元素化合价的变化是:由 价变为 价。
相关试题

