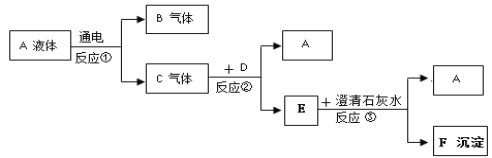
【题目】A、B、C、D、E、F、G是初中化学常见的物质,A在常温下是一种无色液体,D俗称为酒精,F是大理石的主要成分。它们之间的转化关系如图所示:
请回答:
(1)F的化学式为________ 。
(2)反应①的化学反应类型是________ 反应。
(3)写出反应②化学方程式:__________ 。
参考答案:
【答案】CaCO3 分解 C2H5OH+3O2 ![]() 2CO2+3H2O
2CO2+3H2O
【解析】
D俗称为酒精,F是大理石的主要成分,故D是C2H5OH,F是CaCO3。A通电能生成气体B和C,故A是过氧化氢,BC分别是氢气和氧气,C能与酒精反应生成二氧化碳,故C是氧气,B是氢气,E是二氧化碳,经分析推理正确。
(1)由以上 的分析可知,F的化学式为CaCO3。
(2)反应①是水通电生成氢气和氧气,是由一种物质反应生成多种物质,故是分解反应。
(3)反应②是酒精与氧气在点燃的条件下反应生成二氧化碳和水,反应的方程式为:C2H5OH+3O2 ![]() 2CO2+3H2O。
2CO2+3H2O。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(1)现有下列四物种质:A.氢气 B氮气 C. 二氧化碳 D.金刚石
请用合适的物质字母代号填空:
①属于氧化物的是______。
②被认为是理想的清洁、高能燃料的是_______。
③可用来切割玻璃的是________。
④燃烧红磷测定空气中氧气含量的实验中,集气瓶内剩余的气体主要是_____。
(2)据下列粒子结构示意图,回答问题。
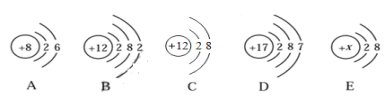
①A、B、C、D所示粒子共表示______种元素(填数字)。
②B元素的化合价为_________ 。
③氟原子的结构示意图为:
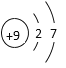 ,上图中与其化学性质相似的元素是____(填元素符号)。
,上图中与其化学性质相似的元素是____(填元素符号)。④若E中x=8 时,则该粒子属于____(填“原子”、 “阳离子” 或“阴离子”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】碳及其化合物与人类的生活和社会发展密切相关。
(1)目前,人类以化石燃料为主要能源。常见的化石燃料包括煤、石油和_____。
(2)人类目前所消耗的能量主要来自化石能源,化石能源的大量使用会产生SO2、CO、NO2、CO2等气体和粉尘,其中在大气中的含量不断上升,导致温室效应增强,全球气候变暖的是___,能形成酸雨的主要是____。
(3)观察下图所示的实验。如图,当将玻璃杯罩住燃着的蜡烛,观察到的现象是:一会儿高的蜡烛先熄灭,低的蜡烛后熄灭,同时还观察到玻璃杯内壁变黑。由实验现象提示我们,在楼房着火时正确的逃生的方法有 ____(填字母序号)。
①打开窗户跳出 ②成站立姿势跑出 ③用湿毛巾捂住鼻子 ④沿墙角伏低身子迅速爬向门外
A.只有② B. ②和③ C. ③和④ D.①、②和③
(4)为减少污染,提高煤的利用率,可将其转化为可燃性气体,此过程可认为是碳与水的反应,其微观示意图如下所示:
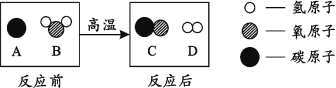
①该反应的化学方程式为________。
②根据上述示意图,你能得到哪些化学变化的信息?(请写一条)___。
(5)为减少温室气体排放,人们积极寻找不含碳元素的燃料。经研究发现NH3燃烧的产物没有污染,且释放大量能量,有一定应用前景。将NH3燃烧反应的化学方程式补充完整:4NH3 +3O2
 6H2O + ____。
6H2O + ____。 -
科目: 来源: 题型:
查看答案和解析>>【题目】水是一种重要的资源,保护水资源从我做起。
(1)电解水的实验如图所示,收集到氧气的试管是____(填“A”或“B”)。

(2)水能与多种物质反应。氧化钙与水激烈反应,并放出大量的热,该反应的化学方程式为_____。
(3)下列实验中,水用来隔绝空气的是______(填字母序号)。

(4)生活中,人们常采用_______的方法,既降低水的硬度,又杀菌消毒。
(5)一些特殊情况下,可向水中加入Ca(ClO)2 进行杀菌和消毒,其中氯元素的化合价是____。常用过滤的方法除去水中难溶固体,举出一个生活中应用过滤原理的实例______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】根据下图回答问题
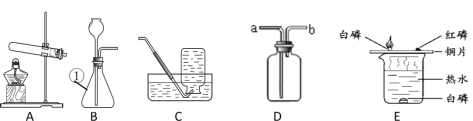
(1)仪器①的名称是__________。
(2)B与C连接制取气体,反应的化学方程式为________。
(3)实验室需少量甲烷气,可用加热无水醋酸钠与碱石灰的固体混合物制得。制甲烷气的发生装置应选用____(填字母)装置;收集甲烷气可选用C装置,由此推断甲烷气具有的物理性质是_______。
(4)用图D的装置排水法收集氧气。瓶中装入水的量应为___(选:“少量”、“多量”或“满瓶”),进气口为____(选“a”或“b”)。
(5)E装置用来探究燃烧的条件,由铜片上白磷燃烧而红磷不燃烧得出的结论______。
(6)在实验室制取二氧化碳的研究中,进行了如下实验:

药品
甲
乙
丙
丁
大理石
2g,块状
2g,块状
2g,粉末状
2g,粉末状
盐酸(过量)
20g,10%盐酸
20g,20%盐酸
20g,10%盐酸
20g,20%盐酸
Ⅰ、若要研究盐酸浓度大小对反应的影响,可选择实验甲与______对照(选填实验编号)。
Ⅱ、研究发现酸的浓度越大,产生气体的速度越快,与甲比较,对丁分析正确的是_____(填字母序号)
①反应更为剧烈 ②最终剩余溶液的质量更小
③产生的二氧化碳的质量更大 ④粉末状大理石利用率更高
A.① B.①④ C.①③④ D.①②③④
-
科目: 来源: 题型:
查看答案和解析>>【题目】天然气的主要成分是甲烷(CH4),我校化学兴趣小组的同学对甲烷在氧气中燃烧的产物产生了兴趣,请你参与:
(提出问题):甲烷燃烧后生成哪些物质?
(查阅资料):含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;白色无水CuSO4遇水变蓝。
(猜想与假设):
甲 CO2 H2O ; 乙 CO H2O; 丙 NH3 CO2 H2O;丁 CO2 CO H2O
你认为_______同学的猜想是错误的,理由是________。
(实验探究):为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列装置:
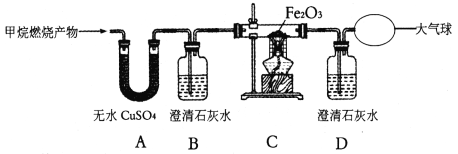
(1)A、B装置的顺序能否颠倒?(填“能"或“否”,并说明原因)_____。
(2)实验中观察到A中无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中红色粉末变成黑色,由此推断________同学猜想成立。
(3)请写出C中黑色粉末变成红色的化学方程式:_______。
-
科目: 来源: 题型:
查看答案和解析>>【题目】(1)用化学用语表示:
①3个氧原子____________;②2个钠离子_________;
③2个二氧化硫分子__________;④标出氧化铝中铝元素的化合价________。
(2)写出下列符号中数字“2”的含文
①SO2中“2”表示________;
②Mg2+中“2”表示_______。
相关试题

