【题目】某化学实验小组实验结束时,将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,为回收有关金属和盐,同学们设计了如下实验方案:
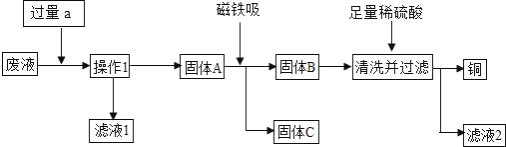
试回答:
(1)操作1是__,固体A的成分__,固体C是__,滤液1和滤液2中溶质相同,该溶质是__.
(2)加入物质a必须过量的原因是__.
(3)要检验加入的稀硫酸是否足量的方法是__.
(4)若实验过程中的物质损失可以忽略,最终所得硫酸锌的质量__(填“>”、“<”或“=”)原废液中硫酸锌的质量.要计算该废液中硫酸铜质量,必须要称量__ 的质量.
参考答案:
【答案】 过滤 Cu、Zn、Fe 铁粉 ZnSO4 将废液中的Cu2+和Fe2+全部置换出来 取步骤④的滤渣于试管中,加入少量稀硫酸,若有气泡产生,则酸不足量(或若无气泡产生,则酸已足量) > 固体D(或铜)
【解析】由题意和实验方案可知该实验的目的是回收金属铁、铜和硫酸锌,故加入的a是金属锌;为了使铁和铜完全置换出来,故加入的锌要过量:锌和硫酸铜反应能生成硫酸锌和铜,锌和硫酸亚铁反应能生成硫酸锌和铁,故固体A是铜、铁和锌,滤液1是硫酸锌;铁能被磁铁吸引,故固体C是铁,那么固体B是锌和铁的混合物;向锌和铜的混合物中加入稀硫酸,稀硫酸能与锌反应生成硫酸锌和氢气,铜不能反应,故通过过滤可分别得到铜,那么滤液2是硫酸锌。(1)通过操作1分别得到了固体和液体,故操作1是过滤;锌能将硫酸铜中的铜、硫酸亚铁中的铁置换出来,由于加入的锌是过量的,故固体A是铜、铁和锌的混合物;铁能被磁铁吸引,故固体C是铁;锌和硫酸铜反应能生成硫酸锌和铜,锌和硫酸亚铁反应能生成硫酸锌和铁,故滤液1中的溶质是硫酸锌;稀硫酸能与锌反应生成硫酸锌和氢气,故滤液2 的溶质是硫酸锌,即滤液1和滤液2中溶质相同均是硫酸锌;(2)步骤①中锌粉必须过量的原因是:将废液中的Cu2+和Fe2+全部置换出来;(3)加入稀硫酸的目的是将铜锌混合物中的锌除去,故检验加入的稀硫酸是否足量的方法是取步骤④的滤渣于试管中,加入少量稀硫酸,若有气泡产生,则酸不足量;(4)若实验过程中的物质损失忽略,因为锌与硫酸铜反应生成铜和硫酸锌,锌与硫酸亚铁反应生成铁和硫酸锌,生成了很多的硫酸锌,最终所得硫酸锌的质量大于原废液中硫酸锌的质量;要计算该废液中硫酸铜质量,必须要称量铜的质量,利用化学方程式,根据铜与硫酸铜的质量比即可计算出硫酸铜的质量。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列方法中能鉴别出空气、氧气、二氧化碳三瓶无色气体的是
A.分别加入澄清石灰水 B.闻气体的气味
C.分别将燃着的小木条伸入三瓶气体中 D.观察气体的颜色
-
科目: 来源: 题型:
查看答案和解析>>【题目】如图中甲、乙、丙、丁、戊分别为下述五种物质中的一种:CuSO4、H2SO4、Fe、Na2CO3、和Ca(OH)2,且图中相连两个环对应的物质(或其溶液)在常温条件下能发生化学反应.

(1)上述五种物质中:
①可用于农业生产改良酸性土壤的是__.
②能发生置换反应的一个化学方程式为__.
(2)若图中乙为H2SO4:
①甲或丙能否为CuSO4?答:__(填“可以”或“不可以”).
②若乙与丁能发生中和反应,则丙为__.
(3)若丙为铁,则甲与戊反应的化学方程式为__.
-
科目: 来源: 题型:
查看答案和解析>>【题目】向装有等量水的A、B、C烧杯中分别加入10g、25g、25gNaNO3固体,充分溶解后,现象如图一所示.

(1)烧杯中的溶液一定属于饱和溶液的是__(填序号);
(2)图二能表示NaNO3溶解度曲线的是__(填“甲”或“乙”);
(3)由图二分析,若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的__(填序号).
A.甲、乙都是饱和溶液 B.所含溶剂质量:甲<乙
C.溶液质量:甲>乙 D.溶质质量分数:甲>乙.
-
科目: 来源: 题型:
查看答案和解析>>【题目】葡萄糖属于
A. 单质 B. 氧化物 C. 有机物 D. 酸
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列化学用语中既能表示一种物质,也表示组成这种物质的元素,还能表示该元素的一个原子的是
A.2N B.Ag C.H Mg2+
-
科目: 来源: 题型:
查看答案和解析>>【题目】某兴趣小组的同学们以“稀硫酸与氢氧化钠溶液能否发生反应”为课题进行了科学探究.同学们在烧杯中加入10mL稀硫酸.滴入几滴酚酞试液,接着分两次向烧杯中滴入氢氧化钠溶液.第一次滴加几滴氢氧化钠溶液后,不断搅拌,第二次继续滴加氢氧化钠溶液至过量.则第一次滴加氢氧化钠溶液时,溶液中溶质(不考虑酚酞)的质量变化情况是__:第二次滴加氢氧化钠溶液时观察到的现象是__.由上述实验同学们得出了稀硫酸与氢氧化钠溶液能发生反应的结论.
[提出问题]是否可以用其他试剂证明稀硫酸与氢氧化钠溶液能发生反应呢?
[甲组实验]实验过程如图所示:现象:向a试管中滴加氢氧化钠溶液时无明显现象,再滴加几滴硫酸铜溶液时出现蓝色沉淀.结论:用硫酸铜溶液可以证明稀硫酸与氢氧化钠溶液能发生反应.
[乙组实验]实验过程如图所示:现象:向b试管中滴加氢氧化钠溶液时无明显现象,再滴加几滴氯化钡溶液时出现白色沉淀.结论:用氯化钡溶液可以证明稀硫酸与氢氧化钠溶液能发生反应.
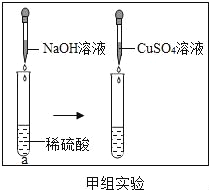
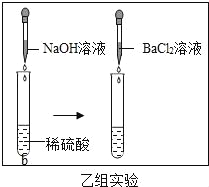
[交流评价]请你评价甲、乙两组同学由实验现象获得的结论是否正确,并说明理由.
正确或错误
理 由
甲组
__
__
乙组
__
__
相关试题

