【题目】对稀硫酸的化学性质进行如下研究。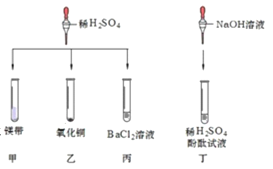
请回答下列问题:
①甲中观察到的现象是_____ ,反应的化学方程式为_________ ; 乙中反应的现象是 __________;
丙中反应的化学方程式为_____;丁中溶液由无色变成红色。
②当甲、乙试管内的固体完全溶解后,将两试管内的物质混合并加入过量的锌片、过滤,则滤渣的成分 是_________,滤液中溶质的化学式为___________。
③请设计能说明 NaOH 与H2SO4是否恰好中和的实验方案。(本题中所用过的试剂不能再用)
_______ | 实验步骤 | 实验现象 | 实验结论 |
_________ | _________ | _________ |
④实验结束后,将乙(其中固体全部溶解)、丁两个实验的废液倒入同一个干净的废液缸中,静置,最终看到上层清液呈红色,废液下层有沉淀。由此推断上层清液的成分有酚酞、水和_____。 写出生成下层沉淀物的化学方程式_____________。
通过上述实验可知,进行化学实验研究,除需要考虑生成什么物质外,还需要考虑_______。
参考答案:
【答案】 镁带逐渐减小,冒气泡 Mg+H2SO4 =MgSO4 +H2↑ 黑色固体逐渐消失,溶液呈蓝色 BaCl2 +H2SO4 =BaSO4 ↓+2HCl Zn,Cu MgSO4,ZnSO4 酚酞 逐渐滴加氢氧化钠溶液,并不断震荡 溶液稍微变红 恰好中和 氯化钡 BaCl2 +Na2SO4=BaSO4+2NaCl 反应物是否过量
【解析】根据所学知识和题中信息知,①甲中观察到的现象是镁带逐渐减小,冒气泡,反应的化学方程式为Mg+H2SO4 =MgSO4 +H2↑;乙中反应的现象是黑色固体逐渐消失,溶液呈蓝色,氧化铜呈黑色,与硫酸反应生成硫酸铜,硫酸铜溶液呈蓝色;丙中反应的化学方程式为BaCl2 +H2SO4 =BaSO4 ↓+2HCl;丁中溶液由无色变成红色,酚酞试液遇碱变红。②当甲、乙试管内的固体完全溶解后,将两试管内的物质混合并加入过量的锌片、过滤,则滤渣的成分是Zn,Cu,锌片过量,锌片与硫酸铜反应置换出铜,锌比铜活泼,滤液中溶质的化学式为MgSO4,ZnSO4。③设计说明 NaOH 与 H2SO4 是否恰好中和。
酚酞 | 实验步骤 | 实验现象 | 实验结论 |
逐渐滴加氢氧化钠溶液,并不断震荡 | 溶液稍微变红 | 恰好中和,酚酞遇酸变红。 |
④实验结束后,将乙(其中固体全部溶解)、丁两个实验的废液倒入同一个干净的废液缸中,静置,最终看到上层清液呈红色,废液下层有沉淀。由此推断上层清液的成分有酚酞、水和氯化钡。生成下层沉淀物的化学方程式是BaCl2 +Na2SO4=BaSO4+2NaCl。进行化学实验研究,除需要考虑生成什么物质外,还需要考虑反应物是否过量。
点睛∶进行化学实验研究时,不仅要考虑反应物和生成物,反应条件,还要考虑到反应物是否过量等因素。酚酞试液遇酸不变色,与碱变红。
-
科目: 来源: 题型:
查看答案和解析>>【题目】2018 年世界环境日的主题是“人人参与,创建绿色家园”,我们需要:
①清新的空气。绿色植物光合作用产生_____气,使人类生生不息:口罩中填充活性炭是利用其_____性。以减少污染物的吸入; 美丽的霓虹灯中填充的气体是_____。
②洁净的水源。天然水通过蒸发、沙滤、氧化等得到净化,其中蒸发属于_____ 变化(填”物理”或”化学”),自来水生产加入液氯的作用是_____。水在通电条件下反应的化学方程式_____,生成氢气和氧气的体积比是_____,0.5mol水中约含_____个氢原子。
③清洁的能源。化石燃料煤、石油、甲烷(CH4) 中,写出甲烷燃烧的化学方程式_____。
-
科目: 来源: 题型:
查看答案和解析>>【题目】下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g 水)。
温度(℃)
0
20
40
60
80
100
KNO3
13.3
31.6
63.9
110
169
246
NaCl
35.7
36.0
36.6
37.3
38.4
39.8
①20℃时溶解度较大的物质是_________ ;
②除去KNO3晶体中混有的少量 NaCl,通过溶解、蒸发浓缩、______、过滤、洗涤、干燥得到比较纯净的KNO3晶体。滤液中溶质的成分有___________。
③用 4 只小烧杯取 T℃时的水各 50 克,进行实验并记录数据如下:
实验编号
1
2
3
4
KNO3 质量/g
40
50
60
70
H2O质量/g
50
50
50
50
溶液质量/g
90
100
105
X
Ⅰ.实验 1 所得溶液的质量分数为_______ ,实验 4 中 X 的值为 _________,
Ⅱ. T℃时KNO3 的溶解度是 _________ g/100g 水。
-
科目: 来源: 题型:
查看答案和解析>>【题目】烧杯中有一些久置的氢氧化钠溶液 A,为确定其变质情况,进行如下实验。
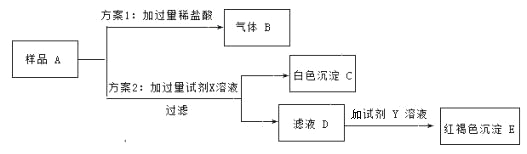
(1)生成气体 B 的化学方程式______________。
(2)试剂 X 是______________(选填“硝酸钡”或“氢氧化钡”)溶液。
(3)若所加试剂 Y 是氯化铁溶液,则生成红褐色沉淀 E 的化学方程式______________ 。
(4)滤液 D 中溶质的成分有______________。
(5)结论:由方案 2 可知,烧杯中氢氧化钠溶液是______________(填“部分变质”或“完全变质”)。
-
科目: 来源: 题型:
查看答案和解析>>【题目】利用如图装置探究物质的性质(部分固定装置略)。
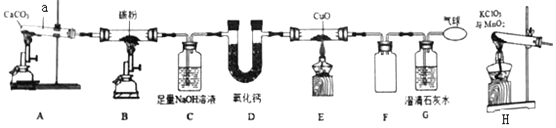
①仪器a的名称_____;装置A中反应的化学方程式_____;
②装置C 的作用_____; 装置D中反应的化学方程式为_____;
③装置E中固体由黑色变成亮红色,反应化学方程式为_____;
④装置F是安全瓶,其作用是_____;
⑤把装置A中换成酒精灯,可用于氯酸钾与二氧化锰混合制取氧气。试管中固体的质量随反应时间变化的数据见如表。
反应时间/min
0
t1
t2
t3
固体质量/g
26.0
20.2
16.4
16.4
Ⅰ.共制得氧气的质量是_____g;
Ⅱ.参加反应的氯酸钾的物质的量是_____mol(通过化学方程式列式计算)
-
科目: 来源: 题型:
查看答案和解析>>【题目】下列图像与实验表述一致的是
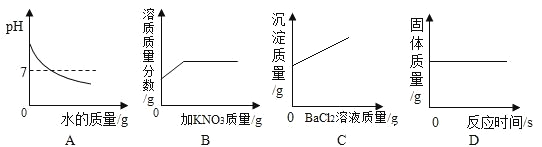
A. 加水稀释 NaOH 溶液
B. 一定温度下,向不饱和 KNO3 溶液中加入 KNO3固体
C. 向一定量的 Na2SO4 溶液中滴加 BaCl2
D. 在密闭容器中,镁帯燃烧前后固体质量的变化
-
科目: 来源: 题型:
查看答案和解析>>【题目】地壳中元素含量由高到低依次是氧、硅、铝、铁等。下图是硅元素在元素周 期表中的信息和铝元素的原子结构示意图。请回答
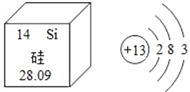
硅原子的核外电子数是_____;铝离子的符号是_____;地壳中含量最多的金属元素和非金属元素组成物质的化学式是_____。
相关试题

